é„Įy(t©»ng)╬█╦«╠Ä└Ē╝╝ągČÓ×ķĪ░ęį─▄║─ōQ╦«┘|Ī▒Ż¼ć°ļH╬█╦«╠Ä└ĒąąśI(y©©)š²ą╬│╔╬█╚Š╬’Ž„£p╣”─▄▀Mę╗▓ĮÅŖ╗»ĪóĄ═╠╝╠Ä└Ē║═─▄į┤ķ_░l(f©Ī)╝╝ąg╩šĄĮųžęĢĪóīŹ¼F(xi©żn)╠Ä└Ē▀^│╠┼c┘Yį┤╗ž╩š═¼▓ĮĄ╚3éĆ├„’@Ą─░l(f©Ī)š╣æB(t©żi)ä▌ĪŻ╬ęć°ęč├„┤_╠ß│÷Ī░╠╝▀_ĘÕĪ▒║═Ī░╠╝ųą║═Ī▒æ(zh©żn)┬į─┐ś╦Ż¼į┌╣Ø(ji©”)─▄Ą═╠╝║═┘Yį┤─▄į┤╗ž╩šĄ─╬█╦«╠Ä└Ēą┬ąĶŪ¾Ž┬Ż¼ę▓├µ┼R╬█╦«╠Ä└Ē╝╝ągĄ─Ė’ą┬ĪŻ
ģÆ觎¹╗»─▄īóėąÖC╬█╚Š╬’▐D╗»×ķŪÕØŹ─▄į┤╝ū═ķŻ¼Š▀ėą▀\ąą─▄║─Ą═Īó─▄į┤╗ž╩šą¦┬╩Ė▀Īóš╝Ąž├µĘeąĪĄ╚ā×(y©Łu)ä▌Ż¼┐╔×ķų„┴„│Ū╩ą╬█╦«╠Ä└ĒīŹ¼F(xi©żn)┐╔│ų└m(x©┤)░l(f©Ī)š╣╠ß╣®ą┬╦╝┬ĘĪŻ╚╗Č°Ż¼į┌ģÆ觎¹╗»▀^│╠ųąŻ¼ėąÖC╬’║¼ėąĄ─Ą¬ūŅĮK▒╗▐D╗»×ķ░▒Ą¬(NH+4NH4+-N)Ż¼▀ĆąĶ▀Mę╗▓Į├ōĄ¬╠Ä└ĒęįīŹ¼F(xi©żn)╬█╦«Ą─▀_ś╦┼┼Ę┼ĪŻģÆč§░▒č§╗»(anaerobicammoniumoxidationŻ¼anammox)╩Ūę╗ĘN┘Yį┤╣Ø(ji©”)╝sĪóŁh(hu©ón)Š│ėč║├Ą─╬█╦«├ōĄ¬╝╝ągĪŻģÆč§░▒č§╗»Š·(anaerobicammoniumoxidationbacteriaŻ¼AnAOB)─▄į┌ģÆ觌l╝■Ž┬Ż¼ęįü厧Ą¬(NO−2NO2−-N)×ķļŖūė╩▄¾wīóNH+4NH4+-N▐D╗»×ķN2Ż¼Č°¤oąĶŲžÜŌ║══Ō╝ė╠╝į┤ĪŻų„┴„│Ū╩ą╬█╦«Įø(j©®ng)ģÆ觎¹╗»╠Ä└Ē║¾Ųõ│÷╦«C/NĄ═Ż¼┼canammox±Ņ║Ž┐╔│õĘų░l(f©Ī)ō]Č■š▀Ą─╝╝ągā×(y©Łu)ä▌ĪŻį┌īŹļHæ¬ė├ųąŻ¼anammox╣ż╦ćęč│╔╣”īŹ¼F(xi©żn)ī”╬█─ÓŽ¹╗»ę║Īó└¼╗°ØB×Vę║Ą╚ÅU╦«Ą─╠Ä└ĒĪŻ╚╗Č°Ż¼ī”ė┌░▒Ą¬▌^Ą═(C/N▒╚ęÓ▌^Ą═)Ą─ų„┴„│Ū╩ą╬█╦«╠Ä└ĒĄ─蹊┐ät▌^╔┘Ż¼▀@╩Ūė╔ė┌į┌įōĘ┤款wŽĄā╚(n©©i)Ę┤æ¬╗∙┘|NO−2NO2−-N║▄ļyĘĆ(w©¦n)Č©½@╚ĪĪŻ
─┐Ū░Ż¼Ųš▒ķ▓╔ė├Č╠│╠Ž§╗»(partialnitrificationŻ¼PN)▀^│╠üĒ½@╚ĪNO−2NO2−-NĪŻ╚╗Č°Ż¼anammox╣ż╦ćĄ─└ĒšōūŅĖ▀├ōĄ¬ą¦┬╩āH×ķ89%Ż¼ŪęPNļyęįĘĆ(w©¦n)Č©┐žųŲü厧╦ß¹}č§╗»Š·(nitriteoxidizingbacteriaŻ¼NOB)Ż¼ī¦ų┬│÷╦«Ž§Ą¬(NO3−-N)┘|┴┐ØŌČ╚Ų½Ė▀Ż¼▀@ę▓▀Mę╗▓ĮŽ▐ųŲ┴╦įō▀^│╠Ą─├ōĄ¬ą¦╣¹ĪŻ╗∙ė┌┤╦Ż¼▒ŠčąŠ┐öM═©▀^═Ō╝ė╚╦╣ż║Ž│╔│Ū╩ą╬█╦«üĒ╠ß╣®╠╝į┤Ż¼į┌ęŲäė┤▓╔·╬’─żĘ┤æ¬Ų„(movingbedbiofilmreactorŻ¼MBBR)ųąŻ¼═©▀^š{(di©żo)┐ž▀\ąąģóöĄ(sh©┤)Ż¼īóČ╠│╠Ę┤Ž§╗»(partialdenitritationŻ¼PD)┼cPN/A▀Mąą±Ņ║ŽŻ¼Å─Č°ÅŖ╗»Ųõī”ų„┴„ģÆ觎¹╗»│÷╦«Ą─├ōĄ¬ą¦╣¹Ż¼ęįŲ┌×ķŅÉ╦ŲĄ═C/N▒╚╬█╦«Ą─╠Ä└Ē╠ß╣®ģó┐╝ĪŻ
1Īó▓─┴Ž┼cĘĮĘ©
1.1 īŹ“×čbų├
īŹ“×čbų├╚ńłD1╦∙╩ŠĪŻMBBR×ķėąÖC▓Ż┴¦ųŲ│╔Ż¼Ųõ╣żū„¾wĘe×ķ(2.0~2.3)LĪóā╚(n©©i)ÅĮ×ķ14cmĪó═ŌÅĮ×ķ45cmĪóĖ▀Č╚×ķ20cmĪŻĘ┤æ¬Ų„Ą─═Ō▓┐įOėą╦«įĪīėŻ¼┐╔═©▀^║Ń£ž╦«įĪčbų├īŹĢrīó£žČ╚┐žųŲį┌(25Ī└1)ĪµĪŻĘ┤æ¬Ų„Ą─▀M│÷╦«═©▀^Č©Ģrčbų├┐žųŲ╚õäė▒├(BT100J-1AŻ¼╗█ėŅŻ╗ųąć°)Ą─åóķ]üĒīŹ¼F(xi©żn)ĪŻų„¾wĘ┤æ¬ģ^(q©▒)ā╚(n©©i)▓┐ėą╠Ņ│õ┬╩×ķ20%Ą─╠Ņ┴Žū„×ķ╔·╬’─żĖĮų°╔·ķLĄ─▌d¾wŻ¼ŪęųąķgįOÖCąĄöć░Ķś¬Ż¼▐D╦┘×ķ80rĪżmin−1ĪŻ╠Ņ┴Žė╔╩Ķ╦«ąįŠ█▒¹Ž®śõų¼ųŲ│╔Ż¼×ķųą┐šłAų∙¾wŻ¼Ųõ│▀┤ń×ķ”š4mmĪ┴4mmĪó▒╚ųž×ķ0.98gĪżcm−3Īó▒╚▒Ē├µĘe×ķ1500m2Īżm−3ĪŻĘ┤æ¬Ų„Ąū▓┐ā╚(n©©i)ų├╬ó┐ūŲžÜŌ▒PŻ¼ė╔Č©Ģrčbų├┐žųŲŲõųąĄ─╬óą═šµ┐š▒├(VBY7506-24VŻ¼ÜŌ║ŻŻ╗ųąć°)üĒīŹ¼F(xi©żn)ķgą¬ŲžÜŌŻ¼═¼ĢrŲžÜŌ┴┐ė╔▓Ż┴¦▐DūėÜŌ¾w┴„┴┐ėŗ(LZB-4WBŻ¼ļpŁh(hu©ón)Ż╗ųąć°)┐žųŲŻ╗Ēö▓┐įO╣■ŽŻ▒Ńöy╩ĮČÓ╣”─▄£yČ©āx(HQ30dŻ¼HACHŻ╗├└ć°)ė├ė┌£žČ╚ĪópH║═DOĄ─īŹĢr▒O(ji©Īn)£yŻ╗é╚▒┌įO╚Īśė┐┌▒Ńė┌┼┼─Ó╝░śėŲĘ▓╔╝»ĪŻ
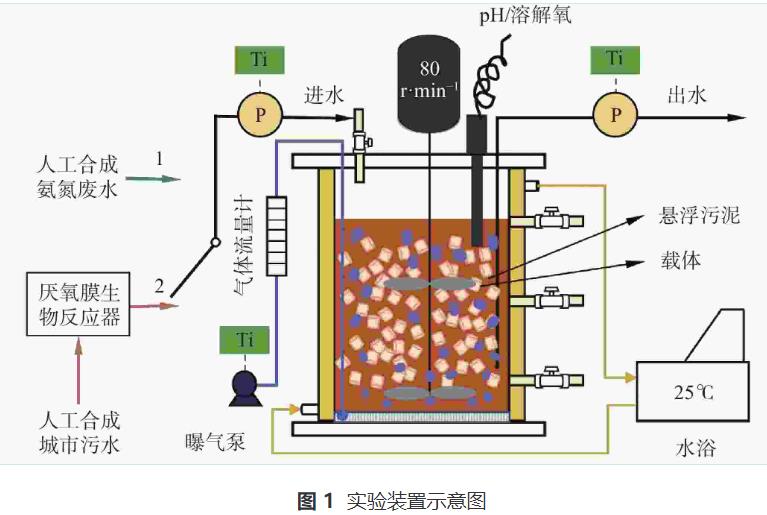
ūóŻ║Ti×ķĢrķg┐žųŲčbų├Ż¼ęįīŹ¼F(xi©żn)▀M╦«║═ŲžÜŌĄ─ūįäėåóķ]Ż╗P×ķ╚õäė▒├ĪŻ
1.2 ĮėĘN╬█─Ó┼cīŹ“×▀M╦«
ĮėĘN╬█─Ó╚Īūį╬„░▓╩ąĄ┌╦─╬█╦«ÅSę╗Ų┌A2O╚▒č§│ž─®Č╦(║¼AnAOB)ĪŻĮėĘN║¾Ę┤æ¬Ų„ųą╬█─ÓĄ─╗ņ║Žę║æęĖĪ╣╠¾w(mixedliquorsuspendedsolidŻ¼MLSS)║═╗ņ║Žę║ō]░l(f©Ī)ąįæęĖĪ╣╠¾w(mixedliquorvolatilesuspendedsolidŻ¼MLVSS)┘|┴┐ØŌČ╚Ęųäe×ķ2.64║═1.44gĪżL−1Ż¼Č°MLVSS/MLSS×ķ0.55ĪŻį┌īŹ“×Ū░Ų┌Ż¼▀M╦«×ķ╚╦╣ż║Ž│╔░▒Ą¬ÅU╦«Ż¼ęįNH4HCO3×ķNH4+-NüĒį┤Ż¼═Č╝ė800mgĪżL−1 NaHCO3Īó21.9mgĪżL−1 KH2PO4(5.00mgĪżL−1 PO43--P)Īó36.0mgĪżL−1 CaCl2Īż2H2OĪó25.0mgĪżL−1 MgCl2Īż6H2OĪó0.5mLĪżL−1╬ó┴┐į¬╦žó±(5.00gĪżL−1 Na2ĪżEDTAĪż2H2OĪó5.00gĪżL−1 FeSO4Īż7H2O)║═0.5mLĪżL−1╬ó┴┐į¬╦žó“(3.30gĪżL−1 Na2ĪżEDTAĪż2H2OĪó0.215gĪżL−1 ZnSO4Īż7H2OĪó0.120gĪżL−1 CoCl2Īż6H2OĪó0.495gĪżL−1 MnCl2Īż4H2OĪó0.125gĪżL−1 CuSO4Īż5H2OĪó0.110gĪżL−1 Na2MoO4Īż2H2OĪó0.095gĪżL−1 NiCl2Īż6H2OĪó0.078gĪżL−1 Na2SeO3Īó0.007gĪżL−1 H3BO4)ū„×ķĀIB(y©Żng)╬’┘|ĪŻį┌Ę┤æ¬Ų„ĘĆ(w©¦n)Č©▀\ąą║¾Ż¼▀M╦«▓╔ė├ų„┴„ģÆ觎¹╗»│÷╦«Ż©üĒūį╠Ä└Ē╚╦╣ż║Ž│╔│Ū╩ą╬█╦«Ą─ģÆč§─ż╔·╬’Ę┤æ¬Ų„│÷╦«Ż®Ż¼Ųõ[NH4+-N]×ķ(51.0Ī└2.3)mgĪżL−1ĪóCOD×ķ(24.9Ī└2.8)mgĪżL−1ĪóēAČ╚(ęįCaCO3ėŗ)×ķ(370Ī└10)mgĪżL−1ĪópH×ķ(7.58Ī└0.16)ĪŻ╚╦╣ż║Ž│╔│Ū╩ą╬█╦«Ą─COD×ķ(500Ī└50)mgĪżL−1Ż¼TN×ķ(50.0Ī└5.0)mgĪżL−1ĪŻ
1.3 Ę┤æ¬Ų„Ą─▀\ąą╣żør
MBBRęįą“┼·╩Į─Ż╩Į▀B└m(x©┤)▀\ąą68dŻ¼Ųõ▀\ąąģóöĄ(sh©┤)╝░š{(di©żo)┼õ▓▀┬į╚ń▒Ē1╦∙╩ŠĪŻīŹ“×Ęų×ķ2éĆļAČ╬Ż║ļAČ╬ó±ų„ę¬═©▀^╠Ä└Ē╚╦╣ż║Ž│╔░▒Ą¬ÅU╦«▀Mąą╬█─Ó±Z╗»Ż╗ļAČ╬ó“Ęųā╔▓┐ĘųŻ¼Ū░Ų┌═©▀^═Ō╝ė110~160mL╚╦╣ż║Ž│╔│Ū╩ą╬█╦«ęįš{(di©żo)š¹▀mę╦Ą─C/NŻ¼║¾Ų┌ät╠Ä└Ēų„┴„ģÆ觎¹╗»│÷╦«▓óĮY║Ž═Ō╝ė╠╝į┤▓▀┬įÅŖ╗»├ōĄ¬ąį─▄ĪŻ
1.4 Ęų╬÷ĒŚ─┐┼cÖz£yĘĮĘ©
╦«śė▓╔ė├0.45”╠m×V─ż▀^×V║¾£yČ©Ųõ╦«┘|ųĖś╦Ż║NH4+-N▓╔ė├╝{╩Žįćä®Ęų╣Ō╣ŌČ╚Ę©ĪóNO2−-N▓╔ė├N-(1-▌┴╗∙)-ęęČ■░ĘĘų╣Ō╣ŌČ╚Ę©ĪóNO3−-N▓╔ė├ūŽ═ŌĘų╣Ō╣ŌČ╚Ę©ĪóCOD▓╔ė├┐ņ╦┘Ž¹ĮŌĘų╣Ō╣ŌČ╚Ę©(╣■ŽŻ┐ņ╦┘Ž¹ĮŌāx)ĪŻ▓╔ė├¤ß╠ßĘ©╠ß╚Ī╬█─Ó╗ņ║Žę║░¹═ŌŠ█║Ž╬’(extracellularpolymericsubstancesŻ¼EPS)Ż¼▓óĘųäe▓╔ė├▒ĮĘė-┴“╦ßĘ©║═ĖŻ┴ų-ĘėĘ©£yČ©Ą░░ū┘|║═ČÓ╠ŪĄ─║¼┴┐ĪŻMLSSĪóMLVSS▓╔ė├ųž┴┐Ę©£yČ©Ż¼ė├ĄĮ105Īµ║Ń£ž║µŽõĪó600Īµ±RĖźĀt╝░├Ę╠ž└š╠ņŲĮĄ╚įOéõĪŻ
1.5 Ą¬▐D╗»╗ŅąįĄ─£yČ©
Ą¬▐D╗»╗Ņąįų„ę¬░³└©░▒č§╗»╗Ņąį(specificammoniaoxidationactivityŻ¼SAOA)Īóü厧╦ß¹}č§╗»╗Ņąį(specificnitriteoxidationactivityŻ¼SNOA)ĪóģÆč§░▒č§╗»╗Ņąį(specificanammoxactivityŻ¼SAA)║═Ę┤Ž§╗»╗Ņąį(specificdenitrificationactivityŻ¼SDA)ĪŻį┌īŹ“×ķ_╩╝Ū░Ż¼Ęųäe£yČ©ą§¾w╬█─Ó║═╔·╬’─żĄ─MLSS║═MLVSSŻ¼Ūę┼·īŹ“׊∙įOų├ŲĮąąīŹ“×ĪŻ
1)SAOA║═SNOAĄ─£yČ©ĪŻ╚ĪĘ┤æ¬Ų„ųą╬█─Ó╗ņ║Žę║160mLŻ¼Įø(j©®ng)5Īļ┬╚╗»Ōc╠įŽ┤║¾Ęųäeų├ė┌2éĆ250mLÅV┐┌Ų┐ųąŻ╗Ė„╝ė╚ļ200mL╗∙┘|(Ųõųą║¼ėą50.0mgĪżL−1 NH4+-NĪó50.0mgĪżL−1 NO2−-N)Ż¼ė┌25Īµ║Ń£ž┤┼┴”öć░Ķ╦«įĪųą│ų└m(x©┤)│õĘųŲžÜŌŻ¼į┘ķgĖ¶20min╚ĪśėĪŻĮY╩°║¾£yČ©NH4+-NĪóNO2−-NĪóNO3−-NĄ─┘|┴┐ØŌČ╚▓óėŗ╦ŃSAOA║═SNOAĪŻ
2)SAA║═SDAĄ─£yČ©ĪŻ╚ĪĘ┤æ¬Ų„ųą╬█─Ó╗ņ║Žę║80mLŻ¼Įø(j©®ng)5Īļ┬╚╗»Ōc╠įŽ┤║¾Ęųäeų├ė┌2éĆ120mLč¬ŪÕŲ┐ųąŻ¼Ė„╝ė╚ļ80mL╗∙┘|(SAA£yČ©║¼25.0mgĪżL−1 NH4+-N║═25.0mgĪżL−1 NO2−-NŻ¼SDA£yČ©║¼50.0mgĪżL−1 NO3−-N║═225mgĪżL−1 COD)Ż¼į┘ė├Ą¬ÜŌ┤ĄÆ▀č¬ŪÕŲ┐Ēö┐š▀Mąą│²č§▓ó├▄ĘŌų├ė┌25Īµ║Ń£ž╦«įĪōu┤▓ųąŻ¼├┐ķgĖ¶1h╚ĪśėŻ¼ĮY╩°║¾£yČ©NH4+-NĪóNO2−-NĪóNO3−-NØŌČ╚▓óėŗ╦ŃSAA║═SDAŻ╗╚Ī50Ņw▌d¾w£yČ©╔·╬’─żĄ─SAAŻ¼▓Į¾E═¼╔ŽĪŻ
1.6 Ą¬▐D╗»╚½ų▄Ų┌īŹ“×
Ę┤æ¬Ų„▀\ąą╚½ų▄Ų┌▀^│╠ųąŻ¼į┌ŲžÜŌĪóģÆč§öć░ĶļAČ╬├┐ķgĖ¶5~8min╚Īśė£yČ©NH4+-NĪóNO2−-N║═NO3−-NĄ─┘|┴┐ØŌČ╚Ż¼▓óĘų╬÷±Ņ║ŽŽĄĮy(t©»ng)ųąĄ¬Ą─╚ź│²┬ĘÅĮĪŻ
1.7 ╬ó╔·╬’Š·╚║Ęų▓╝Ęų╬÷
▓╔ė├¤╔╣ŌįŁ╬╗ļsĮ╗╝╝ąg(fluorescenceinsituhybridizationŻ¼FISH)ė^▓ņ╬ó╔·╬’Š·╚║Ęų▓╝ĪŻŽ╚ė├┴ū╦ß¹}ŠÅø_╚▄ę║Ž┤£ņą§¾w╬█─Ó║═▌d¾w╔·╬’─żśėŲĘŻ¼▓óīóŲõė┌4ĪµĄ─4%ČÓŠ█╝ū╚®╚▄ę║ųą╣╠Č©4hŻ╗į┘īóą§¾w╬█─Ó═┐Ų¼Ż¼▌d¾w╔·╬’─ż░³┬±▓ó▓╔ė├▒ĪŲ¼ŪąŲ¼ÖC(CM1950Ż¼ÅŲ┐©Ż╗Ą┬ć°)Ęų│╔30”╠m║±Č╚Ą─ŪąŲ¼║¾╣╠Č©į┌▌d▓ŻŲ¼╔ŽŻ╗īóŲõĘųäeļsĮ╗║¾═©▀^╝ż╣Ō╣▓Š█Į╣’@╬óńR(TCSSP8Ż¼ÅŲ┐©Ż╗Ą┬ć°)▀Mąąė^▓ņ▓ó▓╔╝»łDŽ±Ż¼╩╣ė├ImageJ▄ø╝■ėŗ╦Ń╣”─▄Š·Ą──┐ś╦╔·╬’┴┐ĪŻīŹ“×╦∙ė├╠ĮßśŻ║┐銷▓╔ė├EUBmix(EUB338ĪóEUBó“ĪóEUB338ó¾ĪóEUB338ó¶)Ż╗░▒č§╗»╝ÜŠ·(ammoniaoxidizingbacteriaŻ¼AOB)▓╔ė├Nso1225Ż╗AnAOB▓╔ė├Amx820Ż╗NOB▓╔ė├NOBmix(NIT3║═CNIT3)ĪŻ
2ĪóĮY╣¹┼cėæšō
2.1 ±Ņ║ŽŽĄĮy(t©»ng)ī”╬█╚Š╬’Ą─╚ź│²ą¦╣¹
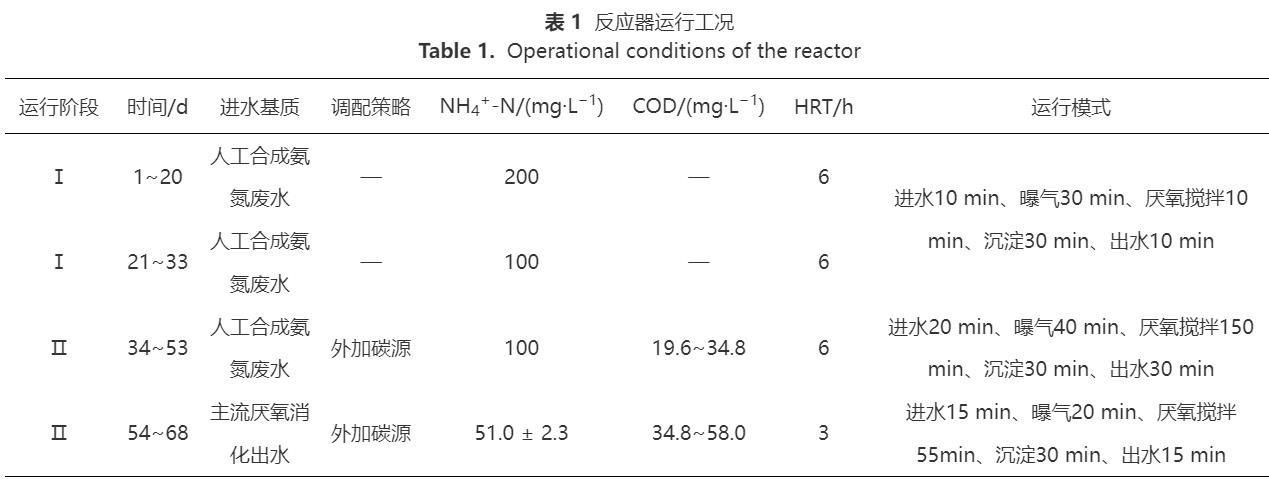
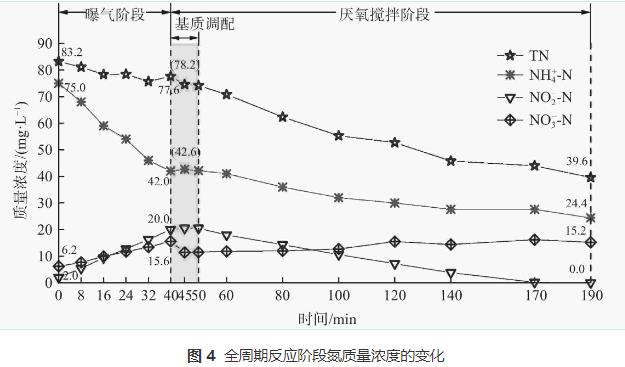
į┌▀B└m(x©┤)▀\ąąĄ─68d└’Ż¼MBBRī”▓╗═¼ļAČ╬╬█╚Š╬’Ą─╚ź│²ą¦╣¹╚ńłD2╦∙╩ŠĪŻļAČ╬I(1~33d)×ķ╬█─Ó±Z╗»┼ÓB(y©Żng)ļAČ╬ĪŻŲõųąŻ¼į┌▀\ąą│§Ų┌(1~20d)Ż¼Ę┤æ¬Ų„ųąĄ¬žō║╔(NLR)×ķ0.80kgĪż(m3Īżd)−1Īó╚▄ĮŌč§(DO)ĘĆ(w©¦n)Č©į┌(0.21Ī└0.02)mgĪżL−1ĪóŲžÜŌ/ģÆč§Ģrķg▒╚×ķ3®s1Ż¼ąĶ═©▀^ŠS│ų▌^ķLĄ─ŲžÜŌĢrķgüĒīŹ¼F(xi©żn)AOB╗ŅąįĄ─┐ņ╦┘╠ßĖ▀ĪŻį┌┤╦ļAČ╬Ż¼│÷╦«[NH4+-N]ė╔148.0mgĪżL−1ų▓ĮĮĄų┴(76.3Ī└9.0)mgĪżL−1Īó[NO2−-N]║═[NO3−-N]Ęųäe×ķ(77.0Ī└6.2)mgĪżL−1║═(28.4Ī└5.6)mgĪżL−1(łD3(a))Ż¼Č°NO2−-N/NO3−-N×ķ2.71▒Ē├„┴╦NOB┐╔▒╗ėąą¦ęųųŲĪŻ▀@┼c▀M╦«▌^Ė▀ØŌČ╚Ą─NH4+-N«a(ch©Żn)╔·Ė▀ė╬ļx░▒(FA)ØŌČ╚ėąĻP(FA×ķ1.71~4.20mgĪżL−1)ĪŻ[NOx−-N]/[NH4+-N]Īó[NO2−-N]/[NH4+-N]Ęųäeė├ė┌▒Ēš„ŽĄĮy(t©»ng)░▒č§╗»║═ü厧Ą¬└█Ęeąį─▄ĪŻį┌┤╦Ų┌ķg,[NOx−-N]/[NH4+-N]ųØuį÷┤¾Ż¼NH4+-N▐D╗»┬╩(ARE)ė╔29.5%į÷ų┴(67.2Ī└3.2)%Ż¼┤╦ĢrĄ─[NO2−-N]/[NH4+-N]▀_ĄĮ(1.13Ī└0.06)Ż¼▒Ē├„Ė▀ą¦Ą─PNŽĄĮy(t©»ng)ęčśŗĮ©═Ļ│╔ĪŻ▀\ąąų┴Ą┌21~33╠ņŻ¼īóNLRĮĄų┴0.40kgĪż(m3Īżd)−1Ż¼┤╦Ģr”ż[NO3−-N]/”ż[NH4+-N]į÷ų┴0.56Ż¼▀hĖ▀ė┌└ĒšōųĄ0.11ĪŻ▀@╩Ūė╔ė┌▀M╦«[NH4+-N]ĮĄĄ═Ż¼ī¦ų┬│÷╦«FAĮĄų┴(0.68~1.34)mgĪżL−1Ż¼╣╩NOBī”FAĄ─ęųųŲū„ė├£p╚§ĪŻ
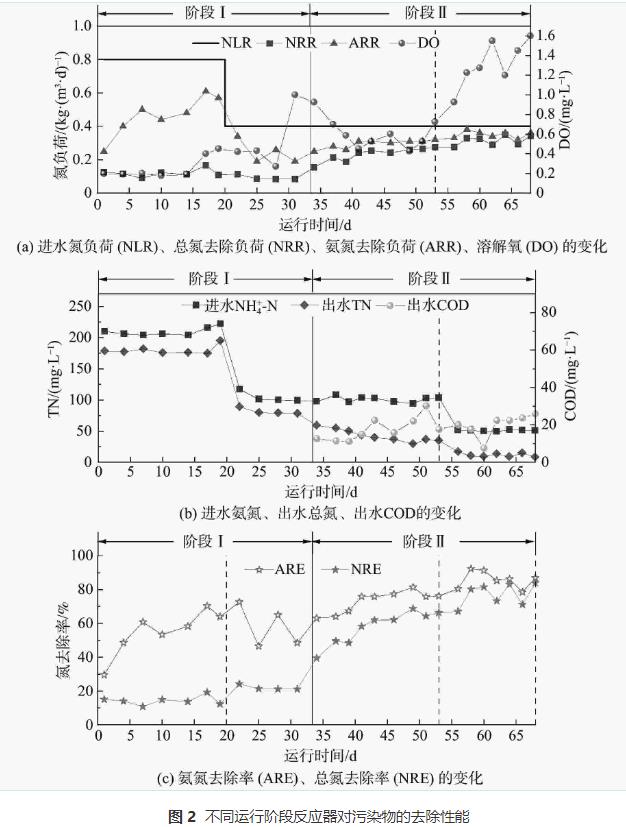
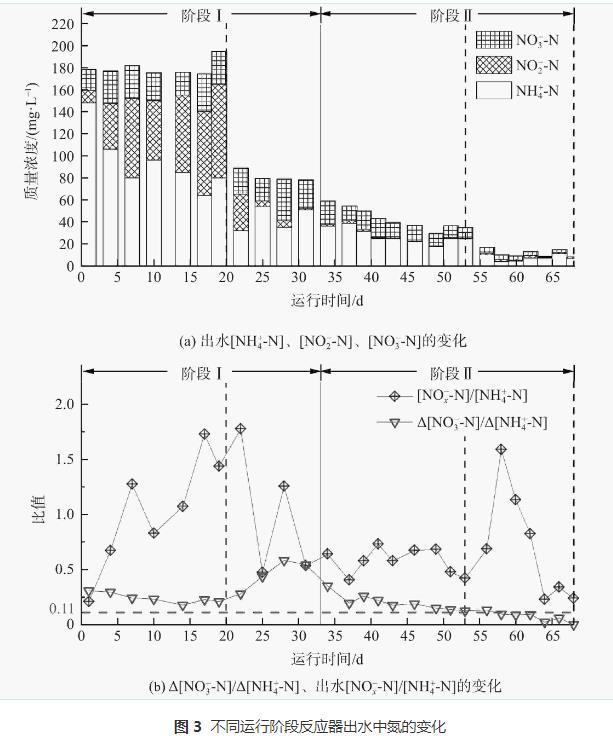
ļAČ╬ó“(34~68d)×ķš{(di©żo)š¹▀\ąą─Ż╩ĮļAČ╬ĪŻį┌┤╦ļAČ╬Ż¼═©▀^į÷╝ėģÆč§öć░ĶĢrķL║═ĮĄĄ═ŲžÜŌ/ģÆč§Ģrķg▒╚Ż¼┐╔ā×(y©Łu)╗»AnAOB╔·┤µŚl╝■ęįÅŖ╗»AnAOBī”NO2−-NĄ─ĖéĀÄĪŻ┤╦═ŌŻ¼×ķĮĄĄ═│÷╦«[NO3−-N]Ż¼ÅŖ╗»├ōĄ¬ąį─▄Ż¼ŲžÜŌĮY╩°║¾īŹ╩®═Ō╝ė╠╝į┤▓▀┬įŻ¼╝┤Ė∙ō■(j©┤)[NO3−-N]║═Ę┤Ž§╗»╗»īWėŗ┴┐ĻPŽĄėŗ╦Ńī”CODĄ─ąĶŪ¾┴┐Ż¼ųØu═∙MBBRā╚(n©©i)╠Ē╝ė110~160mL╚╦╣ż║Ž│╔│Ū╩ą╬█╦«Ż¼īóC/Nš{(di©żo)š¹×ķ0.25~0.34ęį┤┘▀MNO3−-NĄ─Ę┤Ž§╗»ĪŻį┌ļAČ╬ó“Ū░Ų┌(34~53d)Ż¼×ķ▒ŻūCŲžÜŌļAČ╬NH4+-NĄ─▐D╗»┬╩Ż¼īóŲžÜŌ┴┐Å─0.65LĪżmin−1ųØuį÷ų┴1.05LĪżmin−1Ż¼┤╦ĢrĄ─DOŠS│ųį┌(0.52Ī└0.06)mgĪżL−1Ż¼Č°│÷╦«[NH4+-N]ė╔37.4mgĪżL−1ĮĄų┴22.3mgĪżL−1Īó[NO3−-N]ė╔21.6mgĪżL−1ĮĄų┴9.8mgĪżL−1Īó”żNO3−-N/”żNH4+-Nė╔0.35ĮĄų┴0.12Ż¼Ūę?gu©®)ū║§¤oNO2−-NÜł┴¶(łD3)ĪŻĮY╣¹▒Ē├„Ż¼NH4+-N▐D╗»┬╩║═TN╚ź│²┬╩(NRE)ūŅĖ▀Ęųäe▀_81.4%║═68.8%Ż¼TN╚ź│²žō║╔(NRR)į÷ų┴0.27kgĪż(m3Īżd)−1ĪŻį┌┤╦ŽĄĮy(t©»ng)ųąŻ¼Ą═┘|┴┐ØŌČ╚Ą─ėąÖC╬’Ģ■šTī¦ŽĄĮy(t©»ng)ųą«ÉB(y©Żng)Ę┤Ž§╗»Š·(denitrifyingbacteriaŻ¼DB)═©▀^Č╠│╠Ę┤Ž§╗»║═/╗“Ę┤Ž§╗»ū„ė├▒▄├ŌNO3−-NĄ─▀^┴┐Ęe└█Ż¼▀Ć┐╔▒▄├ŌėąÖC╬’ī”AOB║═AnAOB╗ŅąįĄ─Øōį┌ęųųŲŻ¼ęį╠ßĖ▀ŽĄĮy(t©»ng)├ōĄ¬ąį─▄ĪŻį┌ļAČ╬II║¾Ų┌(54~68d)Ż¼Ę┤æ¬Ų„▀M╦«▓╔ė├ų„┴„ģÆ觎¹╗»│÷╦«ĪŻ┤╦ĢrŻ¼┐sČ╠HRTęį▒Ż│ųNLR▓╗ūāĪŻėąčąŠ┐▒Ē├„Ż¼į┌╠Ä└Ēų„┴„ģÆ觎¹╗»│÷╦«▀^│╠ųąŻ¼Ą═DOŁh(hu©ón)Š│▓ó▓╗─▄ķLŲ┌▒Ż│ųAOBĄ─╗ŅąįŻ¼ę“┤╦×ķ▒ŻšŽNH4+-N▐D╗»Ż¼ąĶę¬į÷╝ėŲžÜŌ┴┐╩╣DO▀Mę╗▓Į╠ßĖ▀Ż¼ūŅĮK▀_ĄĮ(1.45Ī└0.15)mgĪżL−1ĪŻį┌Ą┌58~68╠ņŻ¼NH4+-NĄ─▐D╗»┬╩╠ßĖ▀ų┴(86.8Ī└4.5)%Ż¼NH4+-N╚ź│²žō║╔(ARR)▀_ĄĮ0.35Ī└0.02kgĪż(m3Īżd)−1Ż╗│÷╦«ųąTNĄ═ų┴(10.7Ī└2.4)mgĪżL−1ĪóŲĮŠ∙TN╚ź│²┬╩×ķ(78.9Ī└4.9)%ĪóūŅĖ▀▀_84.0%Ż¼TN╚ź│²žō║╔▀_ĄĮ0.38kgĪż(m3Īżd)−1ĪŻ”ż[NO3−-N]/”ż[NH4+-N]▀hĄ═ė┌0.11ĪŻ▀@▒Ē├„ŽĄĮy(t©»ng)ųąAnAOB║═Ę┤Ž§╗»Š·─▄ĘĆ(w©¦n)Č©╣▓┤µ▓óģf(xi©”)═¼Ė▀ą¦ū„ė├ĪŻųĄĄ├ūóęŌĄ─╩ŪŻ¼ųąĖ▀DO▀\ąąĄ─MBBR▓╗āH─▄▒ŻūC▌^Ė▀Ą─NH4+-N▐D╗»┬╩Ż¼Č°ŪęŲõųą▌d¾wī”AnAOBĄ─ėąą¦│ų┴¶║═▒ŻūoĢ■╩╣ŽĄĮy(t©»ng)Š▀ėą▌^ÅŖĄ─┐╣ø_ō¶žō║╔─▄┴”Ż¼▓óĘĆ(w©¦n)Č©├ō│²ų„┴„ģÆ觎¹╗»│÷╦«ųąĄ─Ą¬ĪŻ
2.2 ±Ņ║ŽŽĄĮy(t©»ng)ųąĄ¬Ą─╚ź│²┬ĘÅĮ
į┌MBBR▀\ąąĄ┌43╠ņķ_╩╝▀Mąą╚½ų▄Ų┌īŹ“ׯ¼ęį╠ĮŠ┐ŽĄĮy(t©»ng)Ą─Ą¬╚ź│²▀^│╠╝░┬ĘÅĮĪŻš¹éĆ▀^│╠ųąNĄ─ūā╗»Ūķør╚ńłD4╦∙╩ŠĪŻŲžÜŌļAČ╬¤oėąÖC╠╝į┤╠Ē╝ėŻ¼╣╩▓╗┐╝æ]«ÉB(y©Żng)Ę┤Ž§╗»ū„ė├ĪŻį┌š¹éĆ▀^│╠ųąŻ¼[NH4+-N]ĮĄĄ═33.0mgĪżL−1Ż¼[NO2−-N]Īó[NO3−-N]Ęųäeį÷╝ė18.0mgĪżL−1Īó9.4mgĪżL−1Ż¼ę“┤╦Ż¼ŽĄĮy(t©»ng)Ą─├ōĄ¬ą¦┬╩×ķ6.7%Ż¼╚½▓┐üĒį┤ė┌ģÆč§░▒č§╗»▀^│╠ĪŻį┘ė╔╗»īWėŗ┴┐ĻPŽĄĘų╬÷ŽĄĮy(t©»ng)ā╚(n©©i)░l(f©Ī)╔·Ą─Č╠│╠Ž§╗»ĪóŽ§╗»ĪóģÆč§░▒č§╗»Ę┤æ¬ĪŻŽĄ┴ąĘ┤æ¬░³└©Ż║▓┐ĘųNH4+-N░l(f©Ī)╔·PNĘ┤æ¬▐D╗»×ķNO2−-NŻ¼╩ŻėÓ▓┐Ęųģó┼canammoxĘ┤æ¬╔·│╔NO3−-NŻ╗ŽĄĮy(t©»ng)ųąĄ─NO2−-NüĒūį│§╩╝NO2−-N║═PN▀^│╠Ż¼Ųõ▓┐Ęųģó┼canammoxĘ┤æ¬Ż¼Č°┴Ēę╗▓┐Ęų░l(f©Ī)╔·Ž§╗»Ę┤æ¬▐D╗»×ķNO3−-NŻ¼╩ŻėÓ▓┐Ęų×ķÜł┴¶ĪŻįō▀^│╠ųąĄ¬Ą─▐D╗»ĻPŽĄģóęŖ╩Į(1)Ī½(3)ĪŻ
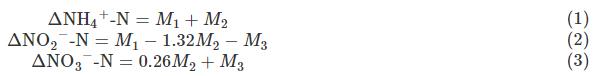
╩ĮųąŻ║M1×ķPNŽ¹║─Ą─NH4+-NŻ╗M2×ķanammoxŽ¹║─Ą─NH4+-NŻ╗M3×ķŽ§╗»Ž¹║─Ą─NO2−-NĪŻ
ęį╔Žėŗ╦ŃĮY╣¹▒Ē├„Ż║91.8%Ą─NH4+-Nģó┼c┴╦PN▀^│╠Īó╩ŻėÓ8.2%ģó┼c┴╦anammoxĘ┤æ¬Ż╗11.9%NO2−-Nģó┼canammoxĘ┤æ¬Īó28.7%ė╔NOB▐D╗»×ķNO3−-NŻ¼▓óĘe└█59.4%×ķ║¾└m(x©┤)Ę┤æ¬╠ß╣®╗∙┘|ĪŻ▀@šf├„ŲžÜŌļAČ╬ęįPNĘ┤æ¬×ķų„Ż¼░ķļS╔┘┴┐anammoxĘ┤æ¬ĪŻ
į┌ģÆč§öć░Ķķ_╩╝Ą─10minā╚(n©©i)(40~50min)Ż¼ų▓ĮŽ“Ę┤æ¬Ų„ā╚(n©©i)╝ė╚ļ╣▓ėŗ160mL╚╦╣ż║Ž│╔│Ū╩ą╬█╦«Ż¼╩╣Ą├COD/NO3−-N×ķ1.40~2.15ĪŻŽĄĮy(t©»ng)ā╚(n©©i)ų„ę¬░l(f©Ī)╔·Ą─ģÆč§░▒č§╗»ĪóČ╠│╠Ę┤Ž§╗»║═/╗“Ę┤Ž§╗»Ę┤æ¬ėąŻ║NH4+-N╚½▓┐ģó┼canammoxĘ┤æ¬Ż¼╣╩anammox▀^│╠Ą─├ōĄ¬┴┐×ķ((1+1.32-0.26)Ī┴”ż[NH4+-N])Ż╗NO2−-NüĒūį│§╩╝NO2−-N╝░PD▀^│╠Ż¼ęÓėą▓┐Ęųģó┼c┴╦anammoxĘ┤æ¬Ż¼ŲõėÓ▓┐ĘųÜł┴¶Ż╗NO3−-NüĒūį│§╩╝NO3−-N╝░anammoxĘ┤æ¬Ż¼ęÓėą▓┐Ęų░l(f©Ī)╔·PD║═/╗“Ę┤Ž§╗»ū„ė├Ż¼ŲõėÓ▓┐ĘųÜł┴¶ĪŻįō▀^│╠ųąĄ¬Ą─▐D╗»ĻPŽĄģóęŖ╩Į(4)Ī½(7)ĪŻ
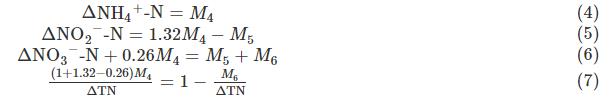
╩ĮųąŻ║M4×ķanammoxŽ¹║─Ą─NH4+-NŻ╗M5×ķPD╔·│╔Ą─NO2−-NŻ╗M6×ķĘ┤Ž§╗»Ž¹║─Ą─NO3−-NĪŻ
«öĘ┤æ¬ĮY╩°ĢrŻ¼”ż[NO2−-N]/”ż[NH4+-N]×ķ1.10Ż¼Ą═ė┌└ĒšōųĄ1.32Ż¼▀@šf├„ėąĄ─NO2−-N((1.32−1.10)Ī┴”ż[NH4+-N])üĒį┤ė┌Č╠│╠Ę┤Ž§╗»Ż¼ėŗ╦ŃĮY╣¹▒Ē├„Ż¼Ž¹║─Ą─NO3−-Nųąėą78.4%▒╗▀ĆįŁ×ķNO2−-NŻ¼Č°╩ŻėÓ21.6%▒╗▀ĆįŁ×ķN2ĪŻō■(j©┤)ł¾Ą└Ż¼COD/NO3−-NĄ═ė┌2.5ėą└¹ė┌īŹ¼F(xi©żn)Ė³Ė▀Ą─NO2−-NĘe└█[25]Ż¼▀@┼c▒ŠčąŠ┐Ą─ĮYšōŽÓ═¼ĪŻģÆč§öć░ĶļAČ╬anammoxĄ─├ōĄ¬žĢ½I┬╩×ķ97.1%Ż¼Č°Ę┤Ž§╗»Ą─├ōĄ¬žĢ½I┬╩×ķ2.9%ĪŻ▀@▒Ē├„═©▀^═Ō╝ė╠╝į┤╠ß╣®ėąÖC╬’║¾Ż¼šTī¦Ę┤Ž§╗»Š·ų„ę¬░l(f©Ī)╔·Č╠│╠Ę┤Ž§╗»Ę┤æ¬Ż¼āH┤µį┌╔┘┴┐Ę┤Ž§╗»├ōĄ¬▀^│╠Ż¼Ųõų„ę¬įŁę“ėąŻ║1)Ė∙ō■(j©┤)Ę┤æ¬▀^│╠Ą─╝¬▓╝╦╣ūįė╔─▄Ż¼NO3−-N▀ĆįŁ×ķNO2−-N▌^NO2−-N▀ĆįŁ×ķN2Ė³╚▌ęū░l(f©Ī)╔·Ż¼Č°Ūęė╔ė┌Ę┤Ž§╗»▀ĆįŁ├ĖĄ─▓Ņ«ÉąįŻ¼NO2−-NĄ─▀ĆįŁ╦┘┬╩▒╚NO3−-NĖ³Ą═Ż¼▀m«ö?sh©┤)─Ę┤æ¬Ģrķg┐╔ę²ŲNO2−-NĄ─Ęe└█Ż╗2)ėąčąŠ┐▒Ē├„Ż¼Ę┤Ž§╗»Š·ī”ļŖūė╩▄¾wĄ─└¹ė├┤µį┌▀xō±ąįŻ¼╝┤į┌ŽÓ═¼Śl╝■Ž┬Ģ■ā×(y©Łu)Ž╚▀xō±NO3−-NČ°«a(ch©Żn)╔·NO2−-N└█ĘeŻ¼į┌╔┘┴┐NO3−-NŪę╠╝į┤│õūŃĢr▓┼Ģ■└¹ė├NO2−-NĪŻ
ŠC╔Ž╦∙╩÷Ż¼ŽĄĮy(t©»ng)├ōĄ¬žĢ½Ių„ę¬üĒį┤ė┌anammoxĘ┤æ¬ĪŻ▒ŠčąŠ┐═©▀^š{(di©żo)┐ž╩╣Č╠│╠Ę┤Ž§╗»į┌ŽĄĮy(t©»ng)├ōĄ¬▀^│╠ųą│ąō·ųžę¬ĮŪ╔½Ż¼┐╔į┌ĮĄĄ═│÷╦«[NO3−-N]Ą─═¼Ģr×ķanammox╗∙┘|Ą─½@╚Ī╠ß╣®═ŠÅĮĪŻ▀@ā╔ĘNū„ė├ŽÓ╗źģf(xi©”)═¼Ż¼┐╔īŹ¼F(xi©żn)Ą═C/NŚl╝■Ž┬ŽĄĮy(t©»ng)Ą─ĘĆ(w©¦n)Č©Ė▀ą¦├ōĄ¬ĪŻ
2.3 ±Ņ║ŽŽĄĮy(t©»ng)╬█─ÓĄ─╠žąį
2.3.1 ī”╬█─Ó╗ŅąįĄ─Ęų╬÷
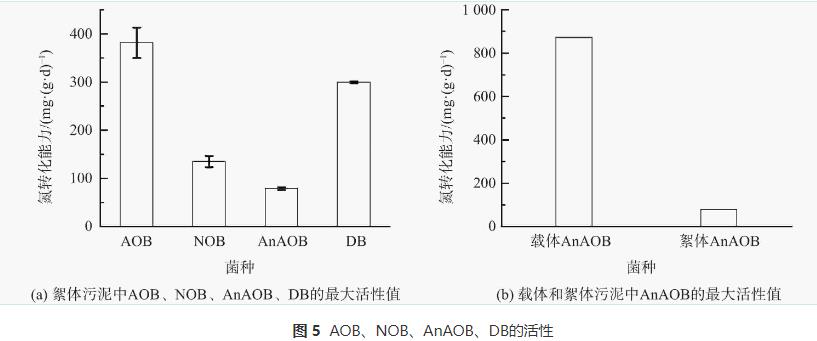
į┌MBBR├ōĄ¬ą¦┬╩│ų└m(x©┤)╠ß╔²Ą─ļAČ╬(Ą┌50╠ņų«║¾)Ż¼Ę┤æ¬Ų„ā╚(n©©i)ą§¾w╬█─ÓMLVSS×ķ1.44gĪżL−1Ż¼┤╦Ģr£yČ©ŽÓĻP╣”─▄Š·╚║AOBĪóNOBĪóAnAOB║═DBĄ─ūŅ┤¾╗ŅąįųĄĪŻ╚ńłD5(a)╦∙╩ŠŻ¼ą§¾w╬█─ÓųąAOB║═NOBĄ─╗Ņąį(ęį├┐┐╦MLVSSųąĄ─Nėŗ)Ęųäe×ķ(381.6Ī└31.8)mgĪż(gĪżd)−1║═(135.0Ī└11.7)mgĪż(gĪżd)−1Ż¼ŪęDBĄ─Č╠│╠Ę┤Ž§╗»╗Ņąį┐╔▀_(299.3Ī└1.7)mgĪż(gĪżd)−1ĪŻ▀@▒Ē├„AOB║═DB┐╔×ķanammoxĘ┤æ¬╠ß╣®ĘĆ(w©¦n)Č©│õūŃĄ─Ąū╬’NO2−-NŻ¼ęį▒ŻūC±Ņ║ŽŽĄĮy(t©»ng)│ų└m(x©┤)īŹ¼F(xi©żn)NH4+-N║═NO3−-NĄ─═¼▓Į╚ź│²ĪŻ╚ńłD5(b)╦∙╩ŠŻ¼▌d¾w║═ą§¾wųąAnAOBĄ─╗ŅąįĘųäe×ķ873.9mgĪż(gĪżd)−1║═79.0mgĪż(gĪżd)−1Ż¼▀@šf├„▌d¾w╔Žęčėąą¦Ė╗╝»┴╦AnAOBĪŻ
2.3.2 ╬█─ÓEPS║¼┴┐╝░╠žąįĘų╬÷
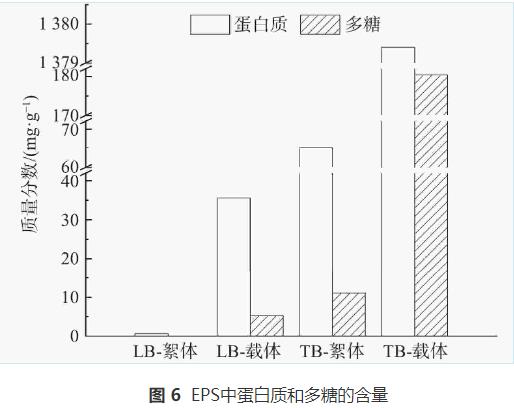
EPS╩Ū╬ó╔·╬’╔·ķL┤·ųxĘų├┌Ą─ę╗ŅÉĖ▀ĘųūėŠ█║Ž╬’Ż¼ų„ꬊ▀ėą╬’┘|─▄┴┐Į╗ōQĪóūį╬ę▒Żūo║═ŽÓ╗źżĖĮĄ─ū„ė├Ż¼─▄┤┘▀MŠ█╝»¾wĄ─ą╬│╔║═│┴ĮĄŻ¼╩Ū╔·╬’─żĄ─ų„ę¬│╔ĘųŻ¼ī”╬ó╔·╬’Ą─│ų┴¶ėąųžę¬ęŌ┴xĪŻEPSĘų×ķ╦╔╔óĮY║Žą═EPS(LB-EPS)║═Šo├▄ĮY║Žą═EPS(TB-EPS)ĪŻLB-EPS═©│Ż┤µį┌ė┌═ŌīėŻ¼Č°TB-EPSį┌ā╚(n©©i)īė[28]ĪŻį┌MBBR▀\ąąĄ─Ą┌50╠ņ£yČ©EPSųąĄ░░ū┘|(╬█─Óą╬│╔Ą─╣Ū╝▄)║═ČÓ╠Ū(┤┘╩╣╬█─Óą╬│╔ĘĆ(w©¦n)Č©ĮYśŗ)Ą─║¼┴┐Ż¼ĮY╣¹╚ńłD6╦∙╩ŠĪŻTB-▌d¾wĪóTB-ą§¾wĄ─║¼┴┐(ęį├┐┐╦MLVSSųąĄ─┘|┴┐ėŗ)Ęųäe×ķ1554.4mgĪżg−1Īó76.1mgĪżg−1Ż¼Ęųäeš╝┐éEPSĄ─97.4%║═99.2%ĪŻ▀@▒Ē├„TB-EPS╩ŪEPSĄ─ų„ę¬│╔ĘųŻ¼╩╣Ą├╬█─ÓĮYśŗŠo£ÉĪŻTB-▌d¾w╔ŽĄ░░ū┘|Ą─┘|┴┐ĘųöĄ(sh©┤)(1374.3mgĪżg−1)╩ŪTB-ą§¾wĄ─21▒ČŻ¼ėą└¹ė┌╝ėÅŖ╬ó╔·╬’Ą─żĖĮ╩╣ŲõŠ█╝»ĄĮ▌d¾w▒Ē├µą╬│╔╔·╬’─żŻ╗ČÓ╠ŪĄ─┘|┴┐ĘųöĄ(sh©┤)(180.4mgĪżg−1)╩Ūą§¾wĄ─16▒ČŻ¼ätėą└¹ė┌╔·╬’─żĄ─ĮYśŗĘĆ(w©¦n)Č©ĪŻ
2.4 ╬ó╔·╬’╚║┬õĘų╬÷
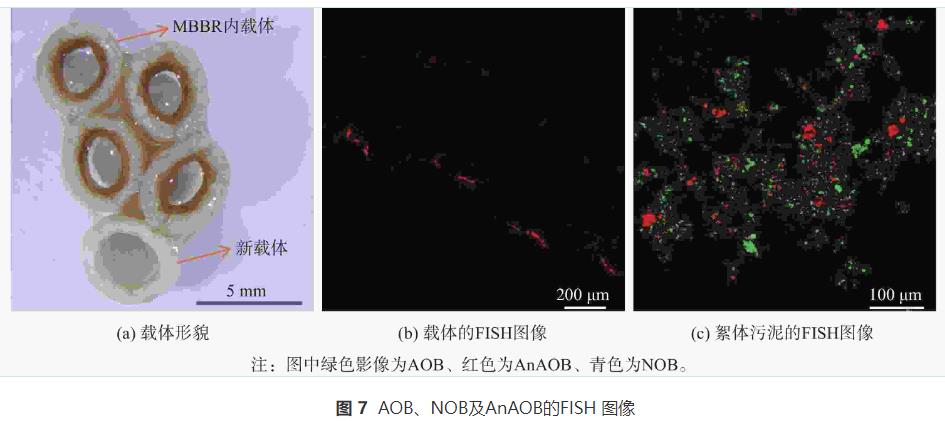
AnAOB╩Ūę╗ĘNĖ╗║¼č¬╝t╦žĄ─Š·╚║Ż¼Š▀ėą§r├„Ą─═Ōė^╠žš„ĪŻį┌MBBRŽĄĮy(t©»ng)ųąŻ¼▌d¾wą╬├▓╚ńłD7(a)╦∙╩ŠĪŻļSų°ŽĄĮy(t©»ng)Ą─ķLŲ┌ĘĆ(w©¦n)Č©▀\ąąŻ¼▌d¾wŅü╔½ųØuūā╝tŻ¼▌d¾w╔ŽAnAOBĄ─¤╔╣Ōą┼╠¢╚ńłD7(b)╦∙╩ŠĪŻ▀@▒Ē├„▌d¾w┐╔×ķAnAOB╠ß╣®╩▄▒ŻūoĄ─ĖĮų°▒Ē├µŻ¼AnAOBį┌▌d¾w╔Žęį╔·╬’─żĄ─ą╬╩ĮĄ├ĄĮėąą¦Ė╗╝»║═▒Ż┴¶Ż¼▓óį┌DOĖ▀▀_(1.45Ī└0.15)mgĪżL−1Ą─ŽĄĮy(t©»ng)ųą╔·ķLĘ▒ų│Ż¼╩╣Ą├ŽĄĮy(t©»ng)Š▀ėąę╗Č©Ą─┐╣ø_ō¶─▄┴”ĪŻ└¹ė├ImageJ▄ø╝■ėŗ╦Ńą§¾w╬█─Óųą╬ó╔·╬’Ą─š╝▒╚Ż¼AOBĪóAnAOB║═NOBžSČ╚Ęųäeš╝┐銷Ą─(38.7Ī└5.9)%Īó(29.0Ī└6.4)%Īó(7.8Ī└2.8)%ĪŻ▀@šf├„NOBĄ├ĄĮę╗Č©│╠Č╚Ą─ęųųŲŻ¼ŪęĘ┤æ¬Ų„ā╚(n©©i)AOB║═AnAOB×ķā×(y©Łu)ä▌Š·Ż¼┐╔┤┘▀M±Ņ║ŽŽĄĮy(t©»ng)Ą─ĘĆ(w©¦n)Č©├ōĄ¬ĪŻ
3ĪóĮYšō
1)ę╗Č╬╩ĮČ╠│╠Ž§╗»-ģÆč§░▒č§╗»±Ņ║ŽČ╠│╠Ę┤Ž§╗»╣ż╦ć╠Ä└Ēų„┴„ģÆ觎¹╗»│÷╦«īŹ¼F(xi©żn)┴╦Ė▀ą¦├ōĄ¬ĪŻ
2)▓╔ė├ųąĖ▀DO▀\ąąėą└¹ė┌ķLŲ┌▒Ż│ųAOBĄ─╗ŅąįŻ¼╠ßĖ▀NH4+-NĄ─▐D╗»┬╩Ż¼Ūę▌d¾w╔ŽĄ─╔·╬’─ż─▄ėąą¦│ų┴¶║═▒ŻūoAnAOBŻ¼ęį▒▄├Ō│ų└m(x©┤)ųąĖ▀DOø_ō¶╩╣AnAOB╗Ņąį╩▄ĄĮęųųŲĪŻ
3)Ą═ØŌČ╚ėąÖC╬’┐╔═©▀^┤┘▀MČ╠│╠Ę┤Ž§╗»«a(ch©Żn)╔·NO2−-NŻ¼Å─Č°į÷╝ėanammoxĘ┤æ¬Ą─╗∙┘|½@╚Ī═ŠÅĮŻ¼═¼Ģr£p╔┘NO3−-NĄ─Ęe└█┴┐Ż¼ÅŖ╗»±Ņ║ŽŽĄĮy(t©»ng)Ą─ģf(xi©”)═¼├ōĄ¬ą¦╣¹ĪŻŻ©üĒį┤Ż║╬„░▓Į©ų■┐Ų╝╝┤¾īWŁh(hu©ón)Š│┼c╩ąš■╣ż│╠īWį║Ż¼╬„▒▒╦«┘Yį┤┼cŁh(hu©ón)Š│╔·æB(t©żi)Į╠ė²▓┐ųž³cīŹ“×╩꯮



