¼FėąÅU┼fõćļxūėļŖ│žĄ─╗ž╩š╣ż╦ćųąŻ¼ļŖ│ž╚į╚╗║¼ėąę╗Č©Ņ~╩ŻėÓļŖ┴┐Ż¼×ķ┴╦Ę└ų╣ūį╚╝║═▒ŻšŽ║¾└m╣ż╦ćĄ─░▓╚½ąįŻ¼╩ūŽ╚ąĶę¬ī”ļŖ│ž▀MąąĘ┼ļŖ╠Ä└ĒĪŻ─┐Ū░ūŅ│╔╩ņĪó│Żė├Ą─Ę┼ļŖ╠Ä└Ē╩ŪīóÅU┼fļŖ│žĮ■╚ļ¹}╚▄ę║ųąŻ¼ą╬│╔Č╠┬Ę┐ņ╦┘Ę┼ļŖĪŻ▓╔ė├įōĘ©▀MąąĘ┼ļŖ╠Ä└ĒŻ¼Ģ■«a╔·║¼ėąÖCļŖĮŌę║Ą─ÅU╦«Ż¼įōÅU╦«Š▀ėąÅU╦«┴┐┤¾ĪópHŲ½Ą═Īó¹}Č╚Ė▀ĪóCODŲ½Ė▀Ą╚╠ž³cĪŻŲõųąŻ¼CODŲ½Ė▀Ą─įŁę“╩ŪĮ■┼▌▀^│╠õćļŖ│žųąĄ─ėąÖCļŖĮŌę║ØB┬®ų┴ÅU╦«ųąŻ¼╠╚╚¶▓╗═ū╔Ų╠Ä└ĒŻ¼īóĢ■ī”╚╦¾węį╝░ūį╚╗ŁhŠ│«a╔·╬Ż║”ĪŻõćļŖ│žļŖĮŌę║ųąų„ę¬║¼ėą╠╝╦ßęꎮ§źŻ©ECŻ®Īó╠╝╦ß▒¹Ž®§źŻ©PCŻ®ĪóęęČ■┤╝Č■╝ū├诩DMEŻ®Īó╠╝╦ßČ■ę꧟Ż©DECŻ®Īó╠╝╦ßČ■ę꧟Ż©DECŻ®║═╠╝╦ßČ■╝ū§źŻ©DMCŻ®Ą╚ĪŻ
Ę┼ļŖÅU╦«ųą§źŅÉĘųūėĮYśŗĘĆČ©Ż¼Ūę¹}║¼┴┐▌^Ė▀Ż¼ī┘ė┌╔·╬’ļyĮĄĮŌėąÖCÅU╦«Ż¼é„ĮyĄ─╔·╗»Ę©▓╗─▄ėąą¦ĮĄĮŌÅU╦«ųąĄ─ėąÖC╬’ĪŻę“┤╦Ż¼Ę┼ļŖÅU╦«ųąėąÖC╬█╚Š╬’Ą─ĮĄĮŌ│╔×ķ┴╦ÅU┼fõćļxūėļŖ│ž┘Yį┤╗»└¹ė├Ą─ųž³c║═ļy³cĪŻ
Į³Äū─ĻŻ¼Ė▀╝ēč§╗»╝╝ągŻ©AOPsŻ®ÅVĘ║æ¬ė├ė┌╔·╬’ļyĮĄĮŌėąÖCÅU╦«Ą─╠Ä└ĒŻ¼└²╚ń│Żė├Ą─Fentonįćä®č§╗»Ę©Īó╝ż╗Ņ▀^┴“╦ß¹}č§╗»Ę©Īó╣Ō┤▀╗»č§╗»Ę©Īó│¶č§č§╗»Ę©║═ļŖ╗»īWč§╗»Ę©Ą╚ĪŻŲõųąļŖĘęŅDĘ©ę“ęū▓┘ū„Īó│╔▒ŠĄ═Īó¤o▀xō±ąįĪó▓╗ė├Ņ~═Ō╠Ē╝ė▀^č§╗»ÜõĄ╚ā׳c╩▄ĄĮ┴╦ÅV┤¾čąŠ┐š▀Ą─ĻPūóĪŻļŖĘęŅDų„ę¬ė├ė┌╠Ä└Ē╦«¾wī¦ļŖąį─▄║├Īó╚▄ę║pHĄ═Ą─ėąÖC╬█╚Š╦«¾wŻ¼═©▀^ĻÄśO▓─┴Ž═©ļŖ║¾«a╔·ļpč§╦«Ż¼ļpč§╦«║═╚▄ę║ųąĄ─Fe2+░l╔·ĘęŅDĘ┤æ¬╔·│╔ÅŖč§╗»ąįĄ─┴u╗∙ūįė╔╗∙Ż©HO•Ż®Ż¼Ųõč§╗»ļŖ╬╗EĪŃŻ©HO•/H2OŻ®Ė▀▀_2.80V/SHEŻ¼─▄ĮĄĮŌ┤¾▓┐ĘųĄ─ėąÖC╬█╚Š╬’ĪŻČ°Ę┤欫a╔·Ą─Fe3+ėų─▄į┌ĻÄśO▀ĆįŁ│╔Fe2+▀Mę╗▓Į┤┘▀MĘęŅDĘ┤æ¬▀MąąĪŻ
▒ŠčąŠ┐└¹ė├ļŖĘęŅDĘ©╠Ä└ĒÅU┼fõćļxūėļŖ│žĘ┼ļŖÅU╦«Ż¼╠Į╦„Ųõā×╗»Ę┤æ¬Śl╝■Ż¼ęįŲ┌×ķĮŌøQĘ┼ļŖÅU╦«ųąėąÖC╬█╚Šå¢Ņ}╠ß╣®ą┬Ą─╦╝┬ĘĪŻ
1ĪóīŹ“×▓┐Ęų
1.1 įćä®┼cāxŲ„
╠╝ÜųŻ¼═┐īėļŖśOŻ©╗∙┘|×ķŌüŻ¼═┐īė×ķŃKŻ®Ż¼┤┼┴”öć░ĶŲ„öć░ĶŻ©MYP11-2Ż®Ż¼pHS-3EĄ─pHėŗŻ¼LZB-3WB▓Ż┴¦▐Dūė┴„┴┐ėŗŻ¼ų▒┴„ĘĆē║ļŖį┤Ż©RKS3030DŻ®Ż¼VE40LH-Aą═│¼╝ā╦«ÖCųŲįņŻ¼ÜŌ┘|┬ōė├āxŻ©GC-MSŻ¼7890A-5975CŻ®ĪŻ
┴“╦߯©H2SO4Ż®Ż¼Üõč§╗»ŌcŻ©NaOHŻ®Ż¼Ų▀╦«║Ž┴“╦ßüåĶFŻ©FeSO4•7H2OŻ®Ż¼Ęų╬÷╝āŻ╗ÅUõćļŖ│žĄ─Ę┼ļŖÅU╦«╚Īūį║■─Ž─│╣½╦ŠŻ¼║¼╠╝╦ßęꎮ§źĄ╚Ż¼pH×ķ4.42Ż¼COD×ķ4.48g/LŻ¼Na+ĪóClĄ─┘|┴┐ØŌČ╚Ęųäe×ķ4.148Īó4.021g/LĪŻ
1.2 īŹ“×ĘĮĘ©
īŹ“×čbų├ė├Š∙Š█Š█▒¹Ž®Ż©PPHŻ®▓─┴Žū„ļŖĘęŅDĘ┤æ¬│žĪŻš²śO×ķŌüśO░Õ═┐īėļŖśOŻ¼═┐īė×ķPtŻ¼5cmĪ┴6cmŻ╗žōśO×ķ╠╝ÜųŻ¼5cmĪ┴20cmĪŻš²žōśO═©▀^ī¦ŠĆ┼cų▒┴„ļŖį┤ŽÓĮėĪŻ
Š▀¾w▓┘ū„Ż║īó400mLĄ─ÅU┼fõćļŖ│žĮ■┼▌ÅU╦«Ą╣╚ļĘ┤æ¬│žųąŻ¼╝ė╚ļę╗Č©┴┐Ą─FeSO4•7H2Oū„×ķĶFį┤Ż¼ė├H2SO4║═NaOHš{╣Ø│§╩╝pHĪŻ╚╗║¾Ż¼īó▀BĮė║├Ą─śOŲ¼▓Õ╚ļļŖĮŌ┘|╚▄ę║ųąŻ¼ĻÄśO╠╝ÜųŁh└@į┌Ļ¢śOśO░Õų▄ć·Ż¼┤“ķ_ų▒┴„ļŖį┤ķ_ĻPŻ¼š{╣ØļŖ┴„ÅŖČ╚Ż¼▀Mąą║Ń┴„ļŖĮŌĪŻ┤²ļŖĮŌĮY╩°║¾Ż¼ĻPķ]ļŖį┤Ż¼╚ĪļŖĮŌę║£yČ©ŲõCODĪŻīŹ“×▀^│╠ųą╩╣ė├┤┼┴”öć░ĶŲ„öć░ĶŻ¼╦┘Č╚×ķ300r/minŻ¼£žČ╚×ķ25ĪµŻ¼═¼Ģr×ķ╠ß╣®ūŃē“Ą─č§ÜŌĪŻ═©▀^ÜŌ▒├Ž“Ę┤æ¬čbų├ųąŲžÜŌŻ¼┐šÜŌĄ─ÜŌ┴„¾wĘe┴„┴┐×ķ1L/minĪŻ
1.3 Ęų╬÷ĘĮĘ©
▓╔ė├HJ/T70ŻŁ2001Ė▀┬╚ÅU╦«COD£yČ©ĘĮĘ©£yČ©ÅU╦«CODĪŻ
2ĪóĮY╣¹┼cėæšō
2.1 ļŖ┴„ī”CODĮĄĮŌĄ─ė░Ēæ
ļŖ┴„ų▒Įėė░ĒæĻÄśOļpč§╦«Ą─╔·«aą¦┬╩Ż║
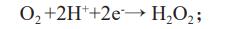
ęį╝░FeļxūėĄ─▀ĆįŁ╦┘┬╩Ż║
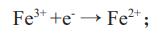
Å─Č°ķgĮė┐žųŲĘęŅDĘ┤æ¬Ż║
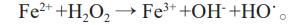
╣╩ļŖ┴„╩Ūė░ĒæĘ┼ļŖÅU╦«CODĮĄĮŌą¦┬╩Ą─ę“╦žų«ę╗ĪŻī”ļŖ┴„┤¾ąĪĘųäe×ķ0.5Īó0.8Īó1.0Īó1.5Īó2.0AĢrĄ─COD╚ź│²┬╩▀Mąą┐╝▓ņŻ¼│§╩╝Fe2+Ą─ØŌČ╚×ķ0.5mmol/LŻ¼pH×ķ3Ż¼│§╩╝COD×ķ4.48g/LŻ¼ĮY╣¹╚ńłD1╦∙╩ŠĪŻ
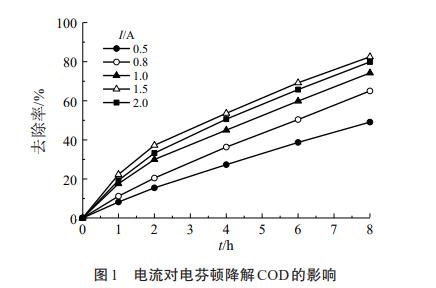
ė╔ė┌ÅU╦«ųą║¼ėą▌^Ė▀║¼┴┐Ą─¹}Ż¼╦«¾wųą▓╗į┘ąĶę¬Ņ~═Ō═Č╝ėļŖĮŌ┘|üĒ╠ßĖ▀ī¦ļŖąįĪŻė╔łD1┐╔ų¬Ż¼į┌ę╗Č©ĘČć·ā╚Ż¼ļSų°ļŖ┴„Ą─╠ßĖ▀Ż¼ĮĄĮŌą¦┬╩ļSų«╔²Ė▀ĪŻ«öļŖ┴„▌^ąĪŻ¼╚ń0.5AĢrŻ¼ĮĄĮŌą¦┬╩▌^Ą═Ż¼8h║¾COD╚ź│²┬╩ų╗ėą49.1%Ż╗═¼śėĄ─ļŖĮŌĢrķgŻ¼ļŖ┴„1AŽ┬COD╚ź│²┬╩┐╔▀_ĄĮ74.2%Ż╗ļSų°ļŖ┴„▀Mę╗▓Įį÷┤¾ĄĮ1.5AŻ¼ļŖĮŌ8hŻ¼COD╚ź│²┬╩▀_ĄĮ82.5%ĪŻČ°«öļŖ┴„▀Mę╗▓Įį÷╝ėĄĮ2.0AĢrŻ¼ĮĄĮŌą¦┬╩Ę┤Č°ĮĄĄ═ĪŻįŁę“▀@╩ŪļŖ┴„į÷┤¾ĢrŻ¼ĻÄśOĄ─╬÷ÜõĖ▒Ę┤æ¬║═Ļ¢śOĄ─H2O2ĘųĮŌķ_╩╝įĮ░l’@ų°Ż¼ī¦ų┬HO•Ą─╔·«aą¦┬╩ĮĄĄ═ĪŻŠC║Ž┐╝æ]Ż¼Ę┤æ¬ā×╗»Ą─ļŖ┴„╩Ū1.5AĪŻ
2.2 Fe2+ī”CODĮĄĮŌĄ─ė░Ēæ
ŽĄĮyųąFe2+─▄┼cļpč§╦«░l╔·ĘęŅDĘ┤欫a╔·HO•üĒč§╗»ĮĄĮŌėąÖC╬█╚Š╬’Ż¼╚▄ę║ųąFe2+║¼┴┐ī”CODĮĄĮŌą¦╣¹ėą▌^┤¾ė░ĒæĪŻĘųäe┐╝▓ņ│§╩╝Fe2+Ą─ØŌČ╚×ķ0.1Īó0.5Īó1.0Īó1.5mmol/LĢrCOD╚ź│²┬╩Ż¼ļŖ┴„×ķ1AŻ¼pH×ķ3Ż¼│§╩╝COD×ķ4.48g/LĪŻīŹ“×ĮY╣¹╚ńłD2╦∙╩ŠĪŻ
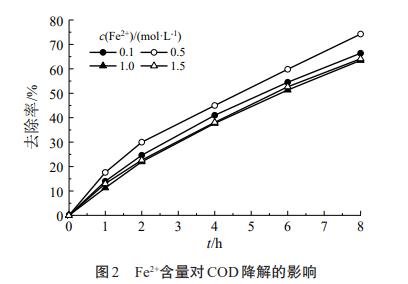
ė╔łD2┐╔ų¬Ż¼Fe2+║¼┴┐ī”COD╚ź│²┬╩Ą─ė░Ēæ▌^×ķÅ═ļsĪŻFe2+Ą─ØŌČ╚×ķ0.5mmol/LĢrŻ¼CODĄ─╚ź│²ą¦╣¹ūŅ║├Ż¼Ę┤æ¬8hŻ¼COD╚ź│²┬╩▀_ĄĮ┴╦74.24%ĪŻČ°«ö│§╩╝Fe2+Ą─ØŌČ╚×ķ0.1mmol/LĢrŻ¼8h║¾COD╚ź│²┬╩×ķ66.38%Ż¼šf├„▀^Ą═Ą─Fe2+▓╗└¹ė┌ĘęŅDĘ┤æ¬Ą─▀MąąŻ¼ĮĄĄ═┴╦HO•Ą─╔·«aą¦┬╩ĪŻ«öFe2+║¼┴┐▀^Ė▀Ģrę▓▓╗└¹ė┌CODĄ─ĮĄĮŌŻ¼Ė▀║¼┴┐Ą─Fe2+Ę┤Č°Ģ■┼cHO•Ę┤æ¬Ż¼Ž¹║─Ą¶╚▄ę║ųą«a╔·Ą─HO•ĪŻ╦∙ęį0.5mmol/L×ķā×╗»═Č╝ė┴┐ĪŻ
2.3 pHī”CODĮĄĮŌĄ─ė░Ēæ
ĶFļxūėĄ─┤µį┌ą╬╩Į╩▄ĄĮpHĄ─┐žųŲŻ¼pH╠½Ė▀ĶFļxūėĢ■«a╔·│┴ĄĒŻ¼pH╠½Ą═┐╔─▄┤┘▀M▀^č§╗»ÜõĄ─Ė▒Ę┤æ¬▒╗Ž¹║─Ą¶Ż║
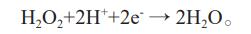
┐╝▓ņ┴╦│§╩╝pHī”ĮĄĮŌCODą¦╣¹Ą─ė░ĒæŻ¼ļŖ┴„×ķ1AŻ¼Fe2+Ą─ØŌČ╚×ķ0.5mmol/LŻ¼│§╩╝COD×ķ4.48g/LĪŻĮY╣¹ęŖłD3ĪŻ
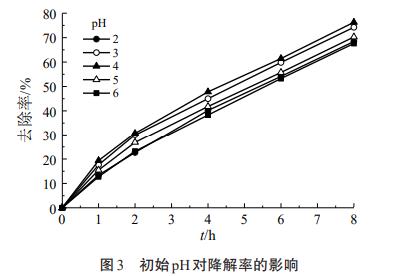
ė╔łD3┐╔ų¬Ż¼«öpH=4Ą─Ģr║“Ż¼╚ź│²┬╩▀_ĄĮūŅĖ▀Ż¼8hļŖĮŌ║¾Ą─COD╚ź│²┬╩▀_ĄĮ76.3%ĪŻÅU┼fõćļŖ│žĄ─Ę┼ļŖÅU╦«pHį┌4ū¾ėęŻ¼Ė∙ō■īŹ“×ĮY╣¹Ż¼▓╗ąĶ꬚{╣ØĘ┤æ¬pHŻ¼▀@ę▓╩ŪļŖĘęŅDĘĮĘ©╠Ä└ĒįōÅU╦«Ą─ā×ä▌ų«ę╗ĪŻ
2.4 ā×╗»Śl╝■Ž┬COD╚ź│²┬╩
Ė∙ō■å╬ę“╦žīŹ“×┤_Č©Ą─ā×╗»Śl╝■Ż║ļŖ┴„×ķ1.5AŻ¼Fe2+═Č╝ė┴┐×ķ0.5mol/LŻ¼pH×ķ4ĪŻį┌įōŚl╝■Ž┬ī”│§╩╝COD×ķ4.48g/LĄ─Ę┼ļŖÅU╦«▀MąąļŖĘęŅD╠Ä└ĒŻ¼ļŖĮŌ8hŻ¼CODĄ─╚ź│²┬╩▀_ĄĮ88.11%ĪŻ
2.5 ĮĄĮŌÖC└Ē╠Įėæ
×ķ▀Mę╗▓Į╠ĮŠ┐ļŖĘęŅDĘĮĘ©╠Ä└ĒĘ┼ļŖÅU╦«COD▀^│╠Ż¼╚ĪįŁę║║═ļŖĮŌ2h║═8hĄ─ÅU╦«Ż¼▓╔ė├┴╦GCMS£yČ©ŲõįŁę║║═ĮĄĮŌ▀^│╠ųąĄ─ÅU╦«ų„ę¬│╔ĘųŻ¼Öz£yĄĮ╦∙ėą╬’┘|┴ą╚ļ▒Ē1ųąĪŻ

ė╔▒Ē1┐╔ų¬Ż¼įŁę║ųąÖz£yĄĮ╠╝╦ßęꎮ§źĪó╠╝╦ß╝ūę꧟║═╠╝╦ßČ■ę꧟Ż¼▀@ų„ę¬╩ŪĮ■┼▌Ę┼ļŖ▀^│╠ųąÅU┼fļŖ│ž└’ĢrėąÖCļŖĮŌ┘|ą╣┬®ĪŻļŖĮŌ2h║¾Ą─╦«¾wųąÖz£yĄĮėą╠╝╦ßęꎮ§źĪóęęČ■┤╝║═ęę╦߯╗ļŖĮŌ8h║¾Ą─╦«¾wųąų╗ėą╠╝╦ßęꎮ§ź║═ęę╦ßĪŻę“┤╦┐╔ęį═Ų£yš¹éĆCODĮĄĮŌ▀^│╠ųąŻ¼╠╝╦ߧźŅÉĄ─╬’┘|Įø▀^č§╗»ĘųĮŌŻ¼Ž╚ą╬│╔ęęČ■┤╝Ż¼═¼Ģr┐╔─▄░ķėąCO2Ą─╔·│╔ĪŻį┘▀Mę╗▓Į▒╗č§╗»ą╬│╔ęę╦߯¼ūŅ║¾═Ļ╚½ĄV╗»│╔H2O║═CO2ĪŻŲõųąÅU╦«ųąĄ─╠╝╦ßęꎮ§ź▌^×ķļy▒╗č§╗»Ż¼į┌ļŖĘęŅDĘ©╠Ä└Ē▀^│╠ųąŻ¼ļm╚╗ę╗ų▒▒╗č§╗»ĘųĮŌŻ¼Ą½╩Ūį┌ļŖĮŌ8h║¾Ą─╦«śėųą▀Ć─▄▒╗Öz£yĄĮĪŻ
3ĪóĮYšō
═©▀^GC-MSĄ─£yČ©Ż¼Ę┼ļŖÅU╦«Ą─ėąÖC│╔Ęųų„ę¬│╔Ęųėą╠╝╦ßęꎮ§źĪó╠╝╦ß╝ūę꧟║═╠╝╦ßČ■ę꧟Ą╚ĪŻ
▓╔ė├╠╝ÜųļŖśOū„ĻÄśOŻ¼═┐īė×ķŃKĄ─Ōü░ÕļŖśOū„Ļ¢śOŻ¼╩ū┤╬░čļŖĘęŅDĘ©æ¬ė├ė┌ÅU┼fõćļŖ│žĘ┼ļŖÅU╦«╠Ä└Ē«öųąĪŻīŹ“×░l¼FļŖĘęŅDĘ©╠Ä└ĒĘ┼ļŖÅU╦«Ż¼¤oąĶį┘╝ė╚ļļŖĮŌ┘|║═š{╣ØpHĪŻ
ÅU╦«│§╩╝COD×ķ4.48g/LĪŻ«öpH×ķ4Ż¼│§╩╝Fe2+×ķ0.5mmol/LŻ¼ļŖ┴„×ķ1.5AĢrŻ¼ėąÖC╬█╚Š╬’ĮĄĮŌą¦┬╩▀_ĄĮ×ķā×ĪŻį┌įōŚl╝■Ž┬Ż¼ĮøļŖĘęŅDĘ©╠Ä└Ē8h║¾Ą─Ę┼ļŖÅU╦«Ż¼COD╚ź│²┬╩ūŅĖ▀┐╔▀_ĄĮ88.11%ĪŻ
į┌š¹éĆļŖĘęŅDĘ©ĮĄĮŌCOD▀^│╠ųąŻ¼ėąÖC╬█╚Š╬’╠╝╦ߧźŅÉ╬’┘|Įø▀^č§╗»ĘųĮŌŻ¼Ž╚ą╬│╔ęęČ■┤╝Ż¼į┘▀Mę╗▓Įč§╗»║¾╔·│╔ęę╦߯¼ūŅ║¾═Ļ╚½ĄV╗»│╔H2O║═CO2Ż¼▀_ĄĮĮĄĄ═CODĄ──┐Ą─ĪŻŻ©üĒį┤Ż║ÅV¢|░ŅŲščŁŁh┐Ų╝╝ėąŽ▐╣½╦ŠŻ®



