╦«ĮŌ╦ß╗»/AOĮM║Ž╣ż╦ć╠Ä└ĒėĪ╚ŠÅU╦«╔½Č╚╚ź│²┼c├ōĄ¬ąį─▄
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2018-11-25 8:10:05
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪė╔ė┌Š▀ėąĘĆČ©Ą─╗»īWĮYśŗĪó║åå╬Ą─╔·«a▀^│╠║═Ą═│╔▒Š, ┼╝Ą¬╚Š┴Ž╩Ū▒╗ÅVĘ║æ¬ė├ė┌ėĪ╚ŠĪóįņ╝ł║═ŲżĖ’Ą╚ąąśIĄ─Ąõą═╗Ņąį╚Š┴Ž.ō■Įyėŗ├┐─Ļ╔·«aĄ─7╚ft╚Š┴Žųą, ┼╝Ą¬╚Š┴Ž╝sš╝70%, ŪęŲõųą10%~15%┐╔─▄į┌╔·«a▀^│╠ųą┼┼Ę┼ų┴╦«¾w.┼╝Ą¬╚Š┴ŽŠ▀ėąų┬░®ąį, ▓╗āHĢ■ī¦ų┬╚╦¾wĖ╬┼K║═─I╩▄ōp, ę▓Ģ■į┌╦«ųąĘe└█▓óęųųŲ╦«╔·╔·╬’Ą─╔·ķL.ę“┤╦, ┼╝Ą¬╚Š┴ŽĄ─ėąą¦┐žųŲ╩Ū╣żśIÅU╦«╠Ä└ĒĄ─ųžę¬ĮM│╔▓┐Ęų.
ĪĪĪĪŽÓ▒╚╗»īW║═╬’└Ē╠Ä└Ē, ┼╝Ą¬╚Š┴ŽĄ─╔·╬’╠Ä└ĒŠ▀ėąŁhŠ│ėč║├ĪóĖ▀ą¦║═╬█─Ó«a┴┐Ą═Ą╚ā×ä▌.║├č§╔·╬’╠Ä└ĒŚl╝■Ž┬, č§ÜŌ▒╚┼╝Ą¬╚Š┴Žā׎╚ū„×ķļŖūė╩▄¾w, ę“┤╦, ģÆč§╔·╬’╠Ä└ĒĖ³▀mė┌┼╝Ą¬╚Š┴ŽĮĄĮŌ. LiĄ╚▓╔ė├ģÆč§╔·╬’╠Ä└Ē╚Š┴Ž╦ßąį│╚7, Ą├ĄĮ├ō╔½┬╩×ķ71.8%║═╗»īWąĶč§┴┐(COD)╚ź│²┬╩×ķ50.6%. ReddyĄ╚▓╔ė├╚▒č§ķgą¬╩ĮĘ┤æ¬Ų„╠Ä└Ē╚Š┴Ž╦ßąį║┌10B, Ą├ĄĮ├ō╔½┬╩×ķ49.5%.╔·╬’ĮĄĮŌ▀^│╠ųą, ┼╝Ą¬╚Š┴Ž└¹ė├╣▓╗∙┘|ĮĄĮŌßīĘ┼Ą─ļŖūėöÓ┴čĪ¬N=NĪ¬, ╔·│╔¤o╔½Ę╝ŽŃ░ĘŅÉ╗»║Ž╬’.Ę╝ŽŃ░ĘŅÉ╗»║Ž╬’ąĶę¬į┌║├觌l╝■Ž┬└¹ė├ĘŪ╠ž«Éąį├ĖīŹ¼F═Ļ╚½ĄV╗».ę“┤╦, ģÆč§/║├č§(AO)╔·╬’╣ż╦ć│Żė├ė┌╠Ä└ĒėĪ╚ŠÅU╦«. BalapureĄ╚▓╔ė├ą“┼·╩ĮģÆč§/╬óč§╣ż╦ć╠Ä└ĒėĪ╚ŠÅU╦«, ├ō╔½┬╩┐╔▀_ĄĮ99%, ŲõųąģÆč§Č╬├ō╔½┬╩×ķ80%. FrindtĄ╚└¹ė├ģÆč§/║├č§╣ż╦ć╠Ä└Ē║¼┼╝Ą¬╚Š┴Ž╗Ņąį│╚107ÅU╦«, ģÆč§├ō╔½┬╩×ķ97%, Č°┼╝Ą¬╚Š┴Ž┤·ųx«a╬’Ę╝ŽŃ░Ę╗»║Ž╬’į┌║├觌l╝■Ž┬Ą├ĄĮĮĄĮŌ.
ĪĪĪĪ┼╝Ą¬╚Š┴ŽĄ─╔·╬’ĮĄĮŌų„ę¬ę└┐┐╬ó╔·╬’├Ėū„ė├īŹ¼F.┼╝Ą¬▀ĆįŁ├Ė║═ŽxŲß├Ė╩Ū┼╝Ą¬╚Š┴ŽĮĄĮŌĄ─ų„ę¬ū„ė├├Ė, ─▄«a╔·┤╦ā╔ĘN├ĖĄ─Š·╚║░³└©Xenophilus azovorans KF46FĪóPigmentiphaga kullae K24ĪóEnterococcus faecalisĪóStaphylococcus aureusĪóEscherichia coliĪóBacillus sp.OY1-2║═Rhodobacter sphaeroidesĄ╚[9].ęį╔Ž║▄ČÓŠ·╚║┐╔│╔×ķ┼╝Ą¬╚Š┴ŽĮĄĮŌĄ─ā×ä▌Š·ĘN. ChenĄ╚▓╔ė├╠Ņ│õ┤▓╔·╬’Ę┤æ¬Ų„╠Ä└Ē║¼ŠSČÓ└¹üå╦{ÅU╦«Ģr, Ą├ĄĮā×ä▌Š·ĘN×ķAeromonas hydrophila. XieĄ╚▓╔ė├╦«ĮŌ╦ß╗»╠Ä└Ē╚Š┴Ž╗Ņąį║┌5║═╗ŅąįŲG╦{19ėĪ╚ŠÅU╦«, ░l¼FKlebsiellaĪóLactococcus║═Desulfovibrio┐╔─▄╩Ū╚Š┴ŽĮĄĮŌĄ─ā×ä▌Š·, ŪęDysgonomonas sp.║═Prevotella sp.┐╔─▄į┌╚Š┴Ž┤·ųx▀^│╠ųąŲųžę¬ū„ė├.
ĪĪĪĪėĪ╚ŠÅU╦«ųą░▒Ą¬(NH4+-N)┐╔═©▀^Ž§╗»Ę┤Ž§╗»╚ź│², ŲõųąŽ§╗»Ę┤æ¬╩ŪŽ▐ųŲ▀^│╠.Ž§╗»▀^│╠ī”ėąČŠ╬’┘|▌^×ķ├¶Ėą, Č°┼╝Ą¬╚Š┴ŽĄ─┤·ųx«a╬’▒Į░Ę╩Ūę╗ĘNėąČŠ╬’┘|, ę“┤╦┐╔─▄Ģ■ė░Ē控╗»ą¦┬╩. KhinĄ╚░l¼F▒Į░ĘØŌČ╚į┌3~250 mgĪżL-1ų«ķg, Ž§╗»Ģ■╩▄ĄĮ▓╗═¼│╠Č╚Ą─ęųųŲ, āH«ö▒Į░ĘØŌČ╚Ą═ė┌0.5 mgĪżL-1Ģr, ▓┼Ģ■░l╔·═Ļ╚½Ž§╗». ThanhĄ╚[12]░l¼F«ö▒Į░ĘØŌČ╚│¼▀^20 mgĪżL-1Ģr, Ž§╗»Ę┤æ¬═Ļ╚½╩▄ĄĮęųųŲ, Ūę▒Į░ĘęųųŲü厧╦ß¹}Ą¬(NO2--N)č§╗»ÅŖė┌NH4+-Nč§╗».Č°JoelĄ╚ūC├„▒Į░ĘĮĄĮŌ║═Ž§╗»┐╔į┌╬█─Ó²g×ķ7 dĄ─╗Ņąį╬█─ÓĘ┤æ¬Ų„ųą═¼Ģr░l╔·, Ž§╗»Š·Ģ■▀mæ¬▒Į░Ę┤µį┌Ą─ŁhŠ│.
ĪĪĪĪ▒ŠčąŠ┐▓╔ė├╦«ĮŌ╦ß╗»/AO╣ż╦ć╠Ä└Ē║¼ėą╚Š┴Ž╗ŅąįŲG╝tX-3B(RR2)Ą─ÅU╦«, ųž³c┐╝▓ņ╣ż╦ć▀\ąąąį─▄.═¼Ģr, ▓╔ė├Ė▀═©┴┐£yą“ĘĮĘ©Öz£y╦«ĮŌ╦ß╗»/AO╣ż╦ćųąĄ─Š·╚║ĘNŅÉ, ęįĮŌ╬÷Ųõį┌╚Š┴Ž╚ź│²╗“├ōĄ¬▀^│╠ųąĄ─ū„ė├.┤╦═Ō, ▒ŠčąŠ┐▀ĆĘų╬÷┴╦╦«ĮŌ╦ß╗»▀^│╠ųąė░Ēæ╔½Č╚╚ź│²Ą─ĻPµIę“╦žęį╝░Ž§╗»▀^│╠ųą╚Š┴Ž╝░Ųõ┤·ųx«a╬’Ą─ė░Ēæ, ęįŲ┌×ķįō╣ż╦ćæ¬ė├ė┌īŹļHėĪ╚ŠÅU╦«╔·╬’╠Ä└Ē╠ß╣®└ĒšōųĖī¦║═╝╝ągų¦│ų.
ĪĪĪĪ1 ▓─┴Ž┼cĘĮĘ© 1.1 įć“×čbų├╝░Ųõ▀\ąą
ĪĪĪĪ╦«ĮŌ╦ß╗»ą“┼·╩ĮĘ┤æ¬Ų„(SBR)¾wĘe×ķ6 L, ▀\ąą▀^│╠ųą£žČ╚×ķ25ĪµĪóō]░ląįæęĖĪ╣╠¾wØŌČ╚(VSS)×ķ(5.17Ī└0.33)gĪżL-1.╦«ĮŌ╦ß╗»SBR▀\ąąų▄Ų┌×ķ6 h, ░³└©5 hģÆč§öć░Ķ(║¼10 min▀M╦«), 50 minņoų├│┴ĄĒ║═10 min│÷╦«. AO SBRĘ┤æ¬Ų„ėąą¦¾wĘe×ķ5 L, ▀\ąą£žČ╚×ķ25ĪµŪęVSS×ķ(2.11Ī└0.28)gĪżL-1. AO SBR▀\ąąų▄Ų┌×ķ6 h, ░³└©2 h╚▒č§Č╬(║¼10 min▀M╦«), 3 h║├č§Č╬, 50 minņoų├│┴ĄĒ║═10 min│÷╦«.Ę┤æ¬Ų„▀M│÷╦«═©▀^Č©ĢrŲ„┐žųŲ╚õäė▒├åóķ]īŹ¼F.
ĪĪĪĪėĪ╚ŠÅU╦«ęįĄ░░ūļ╦ĪóĄĒĘ█║═ęę╦ßŌc×ķ╗ņ║Ž╠╝į┤, ŲõCODØŌČ╚×ķ400 mgĪżL-1(6Ż║3Ż║1);Ųõ╦¹▀M╦«ĮMĘų░³└©114.6 mgĪżL-1NH4Cl, 30 mgĪżL-1┼╝Ą¬╚Š┴ŽRR2, 100 mgĪżL-1 CaCl2Īż2H2O, 100 mgĪżL-1 MgSO4Īż7H2O, 35.2 mgĪżL-1KH2PO4, 200 mgĪżL-1NaHCO3ęį╝░1 mLĪżL-1╬ó┴┐į¬╦ž(1 gĪżL-1 FeCl2Īż4H2O, 100 mgĪżL-1 CoCl2Īż6H2O, 200 mgĪżL-1 NiCl2Īż6H2O, 100 mgĪżL-1 MnCl2Īż4H2O, 100 mgĪżL-1 NaMoO4Īż2H2O, 100 mgĪżL-1 H3BO3, 100 mgĪżL-1 NaWO4Īż2H2O║═100 mgĪżL-1 NaSe2O3).╦«ĮŌ╦ß╗»Ę┤æ¬Ų„├┐éĆ▀\ąąų▄Ų┌▀M╦«3 L, Ųõ│÷╦«ū„×ķAOĘ┤æ¬Ų„▀M╦«, AOĘ┤æ¬Ų„├┐éĆ▀\ąąų▄Ų┌▀M╦«2.5 L.ā╔éĆĘ┤æ¬Ų„Ą─╦«┴”═Ż┴¶ĢrķgŠ∙×ķ12 h.
ĪĪĪĪĘ┤æ¬Ų„±Z╗»ĘĆČ©║¾, £yČ©ā╔éĆĘ┤æ¬Ų„į┌▀\ąąų▄Ų┌ā╚╚Š┴ŽĮĄĮŌ║═Ą¬ØŌČ╚Ą─ūā╗».├┐Ė¶ę╗Č©Ģrķg, Å─╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųą╚Ī╦«śė£yČ©CODĪó╔½Č╚║═NH4+-NØŌČ╚ūā╗», Å─AOĘ┤æ¬Ų„ųą╚Ī╦«śė£yČ©NH4+-NĪóNO2--N║═Ž§╦ß¹}Ą¬(NO3--N)ØŌČ╚ūā╗».
ĪĪĪĪ1.2 ╠╝į┤┼c£žČ╚ī”RR2├ō╔½Ą─ė░Ēæ
ĪĪĪĪ▓╔ė├┼·╠Ä└Ēįć“×, ┐╝▓ņ┴╦╠╝į┤ĘNŅÉĪóCODØŌČ╚║═£žČ╚ī”ģÆč§╦«ĮŌ╦ß╗»ÅŖ╗»RR2╔½Č╚╚ź│²Ą─ė░Ēæ.įć“×╩╣ė├250 mLĄ─Įz┐┌Ų┐, Ę┤款wĘe×ķ200 mL, ╚Ī±Z╗»ĘĆČ©╬█─Ó100 mL┼c100 mLūį┼õ╦«▀Mąą╗ņ║Ž.╠╝į┤ĘNŅÉįć“×ųąūį┼õ╦«ĘųäeęįĄ░░ūļ╦ĪóĄĒĘ█║═ęę╦ßŌc×ķ╠╝į┤, CODØŌČ╚Š∙×ķ400 mgĪżL-1. CODØŌČ╚ė░Ēæįć“×▓╔ė├╗ņ║Ž╠╝į┤, įć“×ųąĄ░░ūļ╦ĪóĄĒĘ█║═ęę╦ßŌc▒╚└²×ķ6Ż║3Ż║1, CODØŌČ╚Ęųäe×ķ200Īó400║═800 mgĪżL-1.Ųõ╦¹ĮMĘųŠ∙┼cūį┼õÅU╦«ĮMĘųŽÓ═¼.ęį╔Ž╠╝į┤ØŌČ╚║═ĘNŅÉė░Ēæįć“×▓╔ė├Ą─£žČ╚Ęųäe×ķ25Īµ║═35Īµ.
ĪĪĪĪįć“×ķ_╩╝Ū░, Ž“Ę┤æ¬Ų┐ųą═©Ą¬ÜŌ4 minęį▒ŻūCĘ┤æ¬╠Äė┌ģÆč§ĀŅæB.įć“×ķ_╩╝║¾, ▓╔ė├ōu┤▓š±╩Ä, Ųõ╦┘Č╚×ķ170 rĪżmin-1.Ę┤æ¬Ģrķg×ķ12 h, Ęųäeį┌Ę┤æ¬Ą─0Īó1Īó2Īó3Īó4Īó6Īó8Īó10║═12 hĢr╚Ī╦«śė, £yČ©Ę┤æ¬▀^│╠ųąĄ─CODØŌČ╚║═╔½Č╚.├┐éĆįć“׌l╝■įOėŗā╔ĮMŲĮąąįć“×, ╚ĪŲĮŠ∙ųĄū„×ķįć“×ĮY╣¹.
ĪĪĪĪ1.3 ╚Š┴Ž╝░Ųõųąķg«a╬’ī”AOŽ§╗»▀^│╠Ą─ęųųŲ
ĪĪĪĪī”ė┌Ž§╗»įć“×, ųž³c┐╝▓ņ┴╦╚Š┴ŽRR2╝░ŲõĄõą═ųąķg«a╬’▒Į░Ęī”AOŽ§╗»ą¦┬╩Ą─ė░Ēæ.įć“×╩╣ė├250 mLĄ─ÕFą╬Ų┐, Ę┤款wĘe×ķ200 mL.╚Ī±Z╗»ĘĆČ©╬█─Ó100 mL┼c100 mL▓╗║¼ėą╠╝į┤Ą─ūį┼õ╦«▀Mąą╗ņ║Ž.╚Š┴ŽęųųŲAOŽ§╗»įć“×ųą╚Š┴ŽØŌČ╚Ęųäe×ķ0Īó4Īó8Īó16Īó32║═64 mgĪżL-1, ▒Į░ĘęųųŲAOŽ§╗»įć“×ųą▒Į░ĘØŌČ╚Ęųäe×ķ0Īó0.75Īó1.5Īó3.0Īó4.5Īó6.0║═7.5 mgĪżL-1, Ųõ╦¹ĮMĘųŠ∙┼c╦«ĮŌ╦ß╗»Ę┤æ¬Ų„│÷╦«ĮMĘųŽÓ═¼.
ĪĪĪĪįć“×▓╔ė├┤┼┴”öć░ĶŲ„(╔Ž║Żš±śs┤┼┴”öć░ĶŲ„90-1)öć░Ķ, ▒ŻūC─Ó╦«╗ņ║ŽŠ∙ä“.ŲžÜŌ▓╔ė├┐╔š{╩ĮÜŌ▒├(║Ż└¹ļp┐ū9602), ŲžÜŌ┴„┴┐×ķ4.0 LĪżmin-1, ▒ŻūC╚▄ĮŌč§(DO)┤¾ė┌4 mgĪżL-1.Ę┤æ¬Ģrķg×ķ120 min, Ę┤æ¬ķ_╩╝║¾├┐Ė¶10 min╚Ī╦«śė, 40 min║¾├┐Ė¶20 min╚Ī╦«śė.£yČ©Ę┤æ¬▀^│╠ųąDOĪóNH4+-NĪóNO2--N║═NO3--NØŌČ╚Ą─ūā╗».
ĪĪĪĪ1.4 Ęų╬÷ĘĮĘ©
ĪĪĪĪCODĪóNH4+-NĪóNO2--NĪóNO3--NĪóæęĖĪ╣╠¾wØŌČ╚(SS)║═VSSę└ō■ć°╝ęęÄČ©Ą─ś╦£╩ĘĮĘ©£yČ©[14].═©▀^╚½▓©ķLÆ▀├Ķ┤_Č©╚Š┴ŽRR2į┌512 nm╠Ä╬³╣ŌČ╚ūŅĖ▀, ę“┤╦ė├┤╦▓©ķL╠ÄĄ─╬³╣ŌČ╚▒Ēš„╔½Č╚, ▓óė├üĒėŗ╦Ń╔½Č╚╚ź│²┬╩.▒Į░Ę£yČ©ĘĮĘ©ę└ššGB 11889-89ųąN-(1-▌┴╗∙)ęęČ■░Ę┼╝Ą¬Ęų╣Ō╣ŌČ╚Ę©.Ęų╣Ō╣ŌČ╚ėŗ×ķ╣■ŽŻDR3900.
ĪĪĪĪ╚Ī╦«ĮŌ╦ß╗»Ę┤æ¬Ų„║═AOĘ┤æ¬Ų„ųą╬█─Ó, ▓╔ė├PowerSoil DNA Isolation Kit (Laboratories Inc., CA, USA)╠ß╚ĪDNA.╠ß╚Ī║¾Ą─DNAśėŲĘį┌V4ģ^▀Mąą╠ž«ÉąįöUį÷, └¹ė├Illumina Miseq 2500£yą“ŲĮ┼_, ▓╔ė├ļp─®Č╦£yą“Paire-endĘĮĘ©▀MąąĖ▀═©┴┐£yą“.└¹ė├fastqc▄ø╝■▀Mąą┘|┴┐įuār║¾, ▀Mę╗▓Į└¹ė├perl─_▒Š▀Mąą┘|┴┐┐žųŲ.└¹ė├Flash╗“MothurīóįŁ╩╝öĄō■Ų┤Įė│╔═Ļš¹Ą──┐ś╦Ų¼Č╬, ▓ó▀Mąą┘|┴┐įuār║═┐žųŲ.į┌ŽÓ╦Ųąį×ķ97%Śl╝■Ž┬, īó▀^×V║¾Ą──┐ś╦Ų¼Č╬Š█ŅÉ│╔▓┘ū„ĘųŅÉå╬į¬(OTU), ▓ó▀x╚Ī┤·▒ĒąįĄ─ą“┴ą┼cöĄō■Äņ▒╚ī”, ▀MąąOTU╬’ĘNūóßī.Ė∙ō■OTUĄ─Į^ī”žSČ╚╝░ūóßīą┼Žó, ĮyėŗśėŲĘį┌Ė„ĘųŅÉīW╦«ŲĮ╔Žą“┴ąśŗ│╔Ūķør.
ĪĪĪĪ2 ĮY╣¹┼cėæšō 2.1 ╦«ĮŌ╦ß╗»/AO╣ż╦ć▀\ąąąį─▄Ęų╬÷
ĪĪĪĪ╦«ĮŌ╦ß╗»/AO╣ż╦ćĘĆČ©▀\ąąŚl╝■Ž┬╦«┘|ĻPµIģóöĄęŖ▒Ē 1.▀M╦«COD×ķ389.5 mgĪżL-1, │÷╦«COD×ķ30.4 mgĪżL-1, Ųõ┐é╚ź│²┬╩×ķ92.2%.▀M╦«╚Š┴ŽØŌČ╚×ķ30 mgĪżL-1, ╬³╣ŌČ╚×ķ0.445ū¾ėę, │÷╦«╬³╣ŌČ╚×ķ0.129, ╔½Č╚┐é╚ź│²┬╩×ķ71.0%.▀M╦«NH4+-NØŌČ╚×ķ31.74 mgĪżL-1, ╦«ĮŌ╦ß╗»│÷╦«ųąNH4+-NØŌČ╚×ķ37.42 mgĪżL-1; AOĘ┤æ¬Ų„│÷╦«NH4+-NĪóNO2--N║═NO3--NØŌČ╚Ęųäe×ķ5.23Īó11.03║═4.39 mgĪżL-1, │÷¼F┴╦├„’@Ą─NO2--NĘe└█¼FŽ¾.
ĪĪĪĪ▒Ē 1 ╦«ĮŌ╦ß╗»-AO╣ż╦ćĘĆČ©ĀŅæB▀\ąąąį─▄
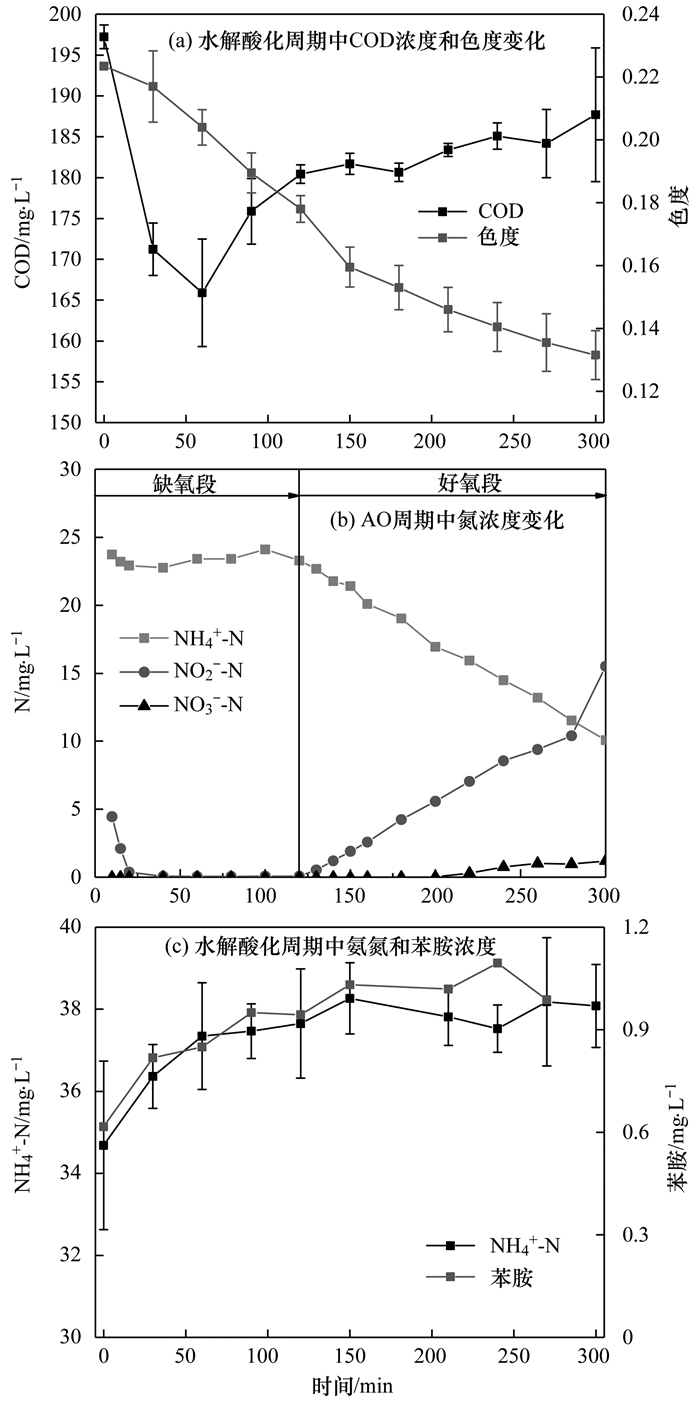
ĪĪĪĪ╣ż╦ćĘĆČ©▀\ąąŚl╝■Ž┬, ╦«ĮŌ╦ß╗»Ę┤æ¬Ų„│÷╦«COD×ķ195.8 mgĪżL-1(▒Ē 1), COD╚ź│²┬╩×ķ49.7%.Ųõ╦¹ŽÓĻP蹊┐ę▓Ą├ĄĮģÆč§Č╬COD╚ź│²┬╩×ķ50%ū¾ėęĄ─ĮYšō.į┌╦«ĮŌ╦ß╗»ų▄Ų┌ųąCODØŌČ╚ūā╗»▓╗├„’@[łD 1(a)]; AO▀^│╠ųą┤µį┌Ž§╗»Ę┤Ž§╗», Ę┤Ž§╗»║═║├č§▀^│╠Š∙─▄Ž¹║─╠╝į┤, ę“┤╦AO▀^│╠╩ŪCOD╚ź│²Ą─ų„ę¬▀^│╠. TomeiĄ╚ę▓░l¼FģÆč§/║├č§╣ż╦ć╠Ä└ĒīŹļHėĪ╚ŠÅU╦«Ģr, ģÆč§ļAČ╬COD╚ź│²┬╩āH×ķ11%~14%, ║├č§ļAČ╬ĮY╩°║¾COD╚ź│²┬╩×ķ59%~75%, šf├„CODų„ę¬═©▀^║├č§▀^│╠╚ź│². Ba©║taĄ╚░l¼FģÆč§/║├č§╣ż╦ć╠Ä└ĒėĪ╚ŠÅU╦«Ģr, ║├č§▀^│╠┐╔ėąą¦╚ź│²ģÆč§▀^│╠ųąļyĮĄĮŌĄ─ėąÖC╬’ĪóģÆč§▀^│╠ųą╔·│╔Ą─ō]░l╦ß(VFAs)║═╚Š┴Ž┤·ųx«a╬’Ę╝ŽŃ░ĘĄ╚╬’┘|.ę“┤╦, ║├č§▀^│╠COD╚ź│²┬╩├„’@Ė▀ė┌ģÆč§▀^│╠.
ĪĪĪĪłD 1
łD 1 ╦«ĮŌ╦ß╗»║═AOų▄Ų┌ųąCODĪó╔½Č╚ĪóĄ¬║═▒Į░ĘØŌČ╚ūā╗»ĪĪĪĪÅ─▒Ē 1Ą├ĄĮ╦«ĮŌ╦ß╗»ļAČ╬╔½Č╚╚ź│²┬╩×ķ72.3%, šf├„╦«ĮŌ╦ß╗»/AO╣ż╦ćųą╦«ĮŌ╦ß╗»▀^│╠╩Ū╚Š┴ŽRR2ĮĄĮŌĄ─ų„ę¬▀^│╠.╦«ĮŌ╦ß╗»▀^│╠ųą╔½Č╚╚ź│²Ę¹║Žę╗╝ēĘ┤æ¬äė┴”īW[łD 1(a)], ╚Š┴ŽĮĄĮŌ╦┘┬╩╝s×ķ2.55 mgĪż(LĪżh)-1. JonstrupĄ╚ę▓░l¼FėĪ╚ŠÅU╦«├ō╔½ų„ę¬░l╔·ė┌ģÆč§▀^│╠, «ö£žČ╚×ķ37Īµ, ╦«┴”═Ż┴¶Ģrķg×ķ3 d, ┼╝Ą¬╚Š┴ŽØŌČ╚×ķ100~2 000 mgĪżL-1Ģr, ģÆč§▀^│╠├ō╔½┬╩┐╔ęį▀_ĄĮ98%ęį╔Ž.▒ŠčąŠ┐╦«ĮŌ╦ß╗»▀^│╠├ō╔½┬╩×ķ72.3%, ┐╔─▄ė╔ė┌╦«ĮŌ╦ß╗»£žČ╚×ķ25Īµ, ╦«┴”═Ż┴¶Ģrķg×ķ12 h, ė╔┤╦ī¦ų┬├ō╔½┬╩Ą═ė┌JonstrupĄ╚Ą─98%.
ĪĪĪĪĖ∙ō■łD 1(b)ųąNO2--N║═NO3--NØŌČ╚ūā╗», AOĘ┤æ¬▀^│╠ųąį┌20 minā╚═Ļ│╔Ę┤Ž§╗»; Ž§╗»▀^│╠ųą, NO3--NØŌČ╚▌^Ą═, │÷¼F├„’@Ą─NO2--NĘe└█, ü厧╗»┬╩×ķ73.8%.ė╔łD 1(c)┐╔ų¬, ▒Į░ĘØŌČ╚ļS╚Š┴ŽĮĄĮŌČ°į÷╝ė, ę“┤╦╚Š┴Ž╝░Ųõ┤·ųx«a╬’▒Į░ĘĄ╚┐╔─▄ī”Ž§╗»Š·╗ŅąįėąęųųŲū„ė├, ī¦ų┬NO2--NĘe└█, ┐饬Ą─╚ź│²┬╩āH×ķ34.9%.Ė∙ō■SinghĄ╚Ą─蹊┐, ╦«ĮŌ╦ß╗»├ō╔½┬╩×ķ72.3%, ┐╔ęį═Ų£y└Ēšō╔Ž▒Į░ĘĄ─╔·│╔┴┐×ķ3.28 mgĪżL-1.į┌ŽxŲß├ĖĄ╚├ĖĄ─ū„ė├Ž┬, ┼╝Ą¬╚Š┴Ž▓╗─▄═Ļ╚½ĮĄĮŌ×ķ▒Į░Ę, ę“┤╦£y│÷Ą─▒Į░ĘØŌČ╚╝s×ķ1 mgĪżL-1.Ģxė±┴┴Ą╚Ą─蹊┐░l¼Fį┌▀M╦«▒Į░ĘØŌČ╚│¼▀^3 mgĪżL-1Ģr, ╗Ņąį╬█─ÓĄ─Ž§╗»─▄┴”å╩╩¦, Ūę▒Į░Ęī”Ž§╗»Ą─ęųųŲ╩Ū┐╔╗ųÅ═Ą─; «ö▒Į░ĘØŌČ╚Ą═ė┌0.5 mgĪżL-1Ģr, NH4+-N╚ź│²┬╩┐╔ęį╗ųÅ═ų┴š²│Ż╦«ŲĮ.
ĪĪĪĪ2.2 Š·╚║Ęų╬÷
ĪĪĪĪ╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąų„ꬥ─ķT╝ēŠ·╚║, ░³└©ŽÓī”žSČ╚×ķ50.98%Ą─öMŚUŠ·ķTBacteroidetesĪó15.27%Ą─SR1Īó10.78%Ą─OP11║═5.57%Ą─║±▒┌Š·ķTFirmicutes[łD 2(a)].ģÆč§╚Š┴ŽĮĄĮŌ╣ż╦ćųą, Bacteroidetes║═FirmicutesČÓ×ķā×ä▌Š·ĘN, ŲõųąBacteroidetes┐╔ĮĄĮŌÅ═ļsĮYśŗ┼╝Ą¬╚Š┴ŽėąÖC╬’. BacteroidetesķTųąĄ─Paludibacter╩Ūę╗ĘN╠╝╦«╗»║Ž╬’░lĮ═Š·. Paludibacter╩Ū╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąŽÓī”žSČ╚ūŅĖ▀Ą─Š·ĘN, ŲõžSČ╚×ķ39.18%[łD 2(b)].▀@šf├„Paludibacter╩Ū╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąų„ę¬╠╝į┤┤·ųxŠ·ĘN. FirmicutesķTųąĄ─Clostridia┐╔└¹ė├ęę╦ßĪóęę┤╝║═ČĪ╦ߥ╚╔·│╔ÜõÜŌ, į┌╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąŽÓī”žSČ╚×ķ3.75%. SR1Ą─ēA╗∙ą“┴ą┼cProsthecobacter algae strain EBTL04║═Prosthecobacter dejongeii strain FC1ŽÓ╦ŲČ╚×ķ97%, OP11Ą─ēA╗∙ą“┴ą┼cVictivallis vadensis strain CelloŽÓ╦ŲČ╚×ķ87%, Ą½▀@ā╔ŅÉŠ·╚║Ą─ū„ė├╔ą▓╗├„╬·.į┌╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąŽÓī”žSČ╚Ū░10Ą─Š·╚║ųą, Ųõ╦¹Š·ĘNø]ėąčąŠ┐ūC├„Š▀ėą┼╝Ą¬╚Š┴ŽĮĄĮŌ─▄┴”, ų╗ėąProteobacteriaķTųąĄ─Desulfovibrioė╔ė┌║¼ėą┼╝Ą¬▀ĆįŁ├Ė, ┐╔īó┼╝Ą¬╚Š┴ŽĮĄĮŌ│╔Ę╝ŽŃ░ĘŅÉ╬’┘|. Desulfovibrioį┌╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąŽÓī”žSČ╚×ķ2.23%, ▀@šf├„Desulfovibrio╩Ū╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąų„ꬥ─┼╝Ą¬╚Š┴ŽĮĄĮŌŠ·.Š▀¾w┬ōŽĄ╬█╦«īÜ╗“ģóęŖhttp://www.jianfeilema.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
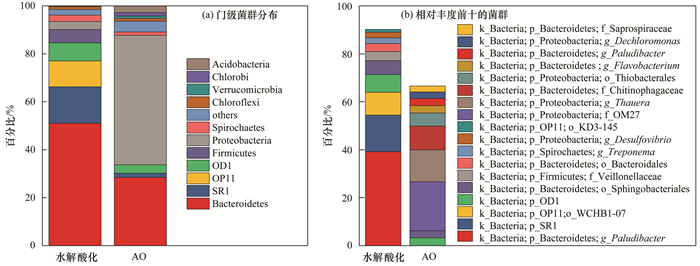
ĪĪĪĪłD 2
łD 2 ╦«ĮŌ╦ß╗»║═AOĘ┤æ¬Ų„ųąĄ─Š·╚║Ęų▓╝ĪĪĪĪAOĘ┤æ¬Ų„ųąų„ꬥ─ķT╝ēŠ·╚║×ķŽÓī”žSČ╚×ķ54.0%Ą─ProteobacteriaĪó28.4%Ą─BacteroidetesĪóęį╝░į┌1%~3.5%ų«ķgĄ─OD1ĪóAcidobacteriaĪóSR1ĪóSpirochaetesĪóChlorobiĪóChloroflexi║═Verrucomicrobia. AOĘ┤æ¬Ų„ųąų„ꬥ─Ž§╗»Š·×ķNitrospira, ŽÓī”žSČ╚×ķ0.28%, ╩Ūę╗ĘN│ŻęŖĄ─Ž§╗»Š·.▒ŠčąŠ┐Ę┤Ž§╗»Š·ųąŽÓī”žSČ╚ūŅĖ▀Ą─×ķRhodocyclaceaeųąThauera, ŽÓī”žSČ╚×ķ13.35%. Thauera▓╗āH╩Ū│ŻęŖĄ─Ę┤Ž§╗»Š·, ▀ĆŠ▀ėąĮĄĮŌĘ╝ŽŃ░ĘŅÉ╬’┘|Ą──▄┴”.į┌NO2--NĘe└█Śl╝■Ž┬, Thauera┐╔│╔×ķĘ┤Ž§╗»Š·ųąā×ä▌Š·ĘN; ▀@┼cAOĘ┤æ¬Ų„ųą│÷¼FNO2--NĘe└█¼FŽ¾ę╗ų┬.ė╔ė┌AO▀M╦«×ķ╦«ĮŌ╦ß╗»│÷╦«, ę“┤╦║¼ėąRR2┤·ųx«a╬’Ę╝ŽŃ░ĘĄ╚╬’┘|, ┐╔▒╗ThaueraĮĄĮŌ.═¼ī┘ė┌RhodocyclaceaeĄ─DechloromonasŽÓī”žSČ╚×ķ2.73%, ę▓╩Ūę╗ĘNĖ▀ą¦Ą─Ę┤Ž§╗»Š·. AOĘ┤æ¬Ų„ųąÖz£yĄĮĄ─ŽÓī”žSČ╚▌^Ė▀Ą─OD1, ŲõēA╗∙ą“┴ą┼cLactobacillus paracollinoides strain DSM 15502║═Lactobacillus collinoides strain JCM1123ėą95%Ą─ŽÓ╦ŲČ╚, ę“┤╦┐╔─▄Š▀ėą╚ķ╦ߊ·Lactobacillus░lĮ═Ą─╣”─▄, ┐╔īó╠╝į┤ĮĄĮŌė├ė┌Ę┤Ž§╗».
ĪĪĪĪ2.3 ╠╝į┤╝░£žČ╚ī”RR2├ō╔½Ą─ė░Ēæ
ĪĪĪĪ┼╝Ą¬╚Š┴ŽĄ─ĮĄĮŌ╩Ū═©▀^Ī¬N=NĪ¬Ą─öÓ┴čīŹ¼FĄ─.┼╝Ą¬╚Š┴Žū„×ķļŖūė╩▄¾wĢr, ┼╝Ą¬µIĪ¬N=NĪ¬öÓ┴čąĶę¬4éĆļŖūė, Ą┌ę╗▓ĮąĶę¬2éĆļŖūė╩╣┼╝Ą¬µIöÓ┴č×ķĪ¬NĪ¬NĪ¬, Ą┌Č■▓ĮąĶę¬2éĆļŖūė╩╣┼╝Ą¬µI═Ļ╚½öÓ┴č.ĄĒĘ█║═Ą░░ūļ╦Ą╚╠╝į┤ū„×ķļŖūė╣®¾w, į┌ĮĄĮŌ▀^│╠ųą┐╔ęį╠ß╣®┼╝Ą¬╚Š┴ŽĮĄĮŌ╦∙ąĶļŖūė.Įø▀^ŅAįć“×░l¼Fęę╦ßŌcū„×ķ╠╝į┤Ģr, ╚Š┴ŽRR2ĮĄĮŌ╦┘┬╩ūŅ┬², āH×ķĄĒĘ█ĮĄĮŌ╦┘┬╩Ą─1/3ū¾ėę, ▒Ē├„ęę╦ßŌc▓╗╩ŪRR2├ō╔½Ą─ų„ę¬╠╝į┤.ęįĄ░░ūļ╦ĪóĄĒĘ█║═╗ņ║Ž╠╝į┤×ķ╠╝į┤, į┌▓╗═¼Śl╝■Ž┬╚Š┴ŽRR2ĮĄĮŌįć“×ĮY╣¹╚ńłD 3, ėŗ╦ŃĄ├ĄĮĖ„Śl╝■Ž┬RR2Ą─ĮĄĮŌę╗╝ēĘ┤æ¬äė┴”īWģóöĄ╚ń▒Ē 2.
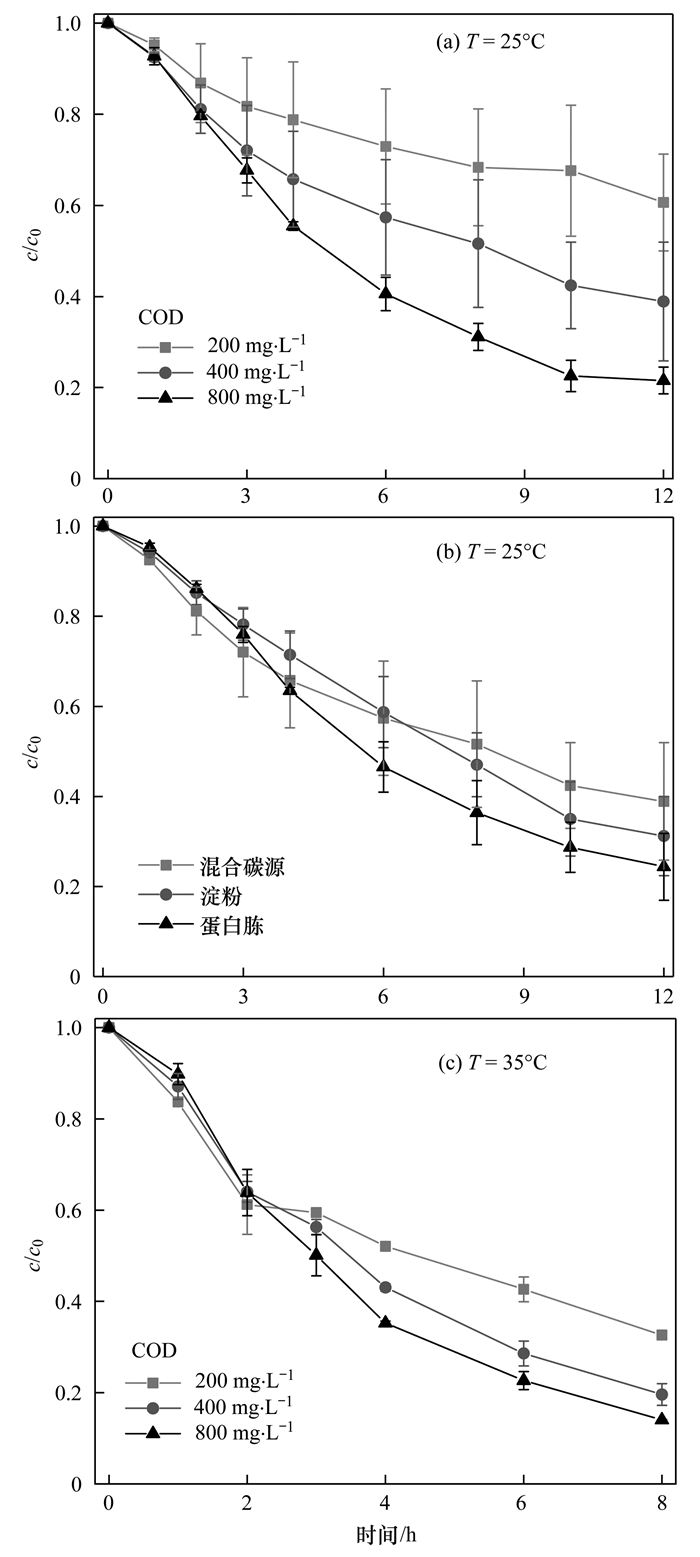
ĪĪĪĪłD 3
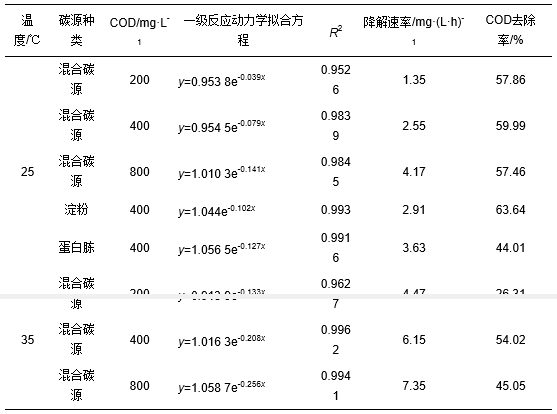
łD 3 ▓╗═¼CODØŌČ╚║═╠╝į┤ĘNŅÉŚl╝■Ž┬RR2ØŌČ╚ūā╗»ĪĪĪĪĪĪ▒Ē 2 ╚Š┴ŽĮĄĮŌįć“×ę╗╝ēĘ┤æ¬äė┴”īWöM║ŽĘĮ│╠╝░ĮĄĮŌ╦┘┬╩
ĪĪĪĪį┌COD=400 mgĪżL-1Īó25ĪµŚl╝■Ž┬, ęįĄ░░ūļ╦×ķ╠╝į┤Ģr, RR2Ą─ĮĄĮŌ╦┘┬╩ūŅ┐ņ, ×ķ3.63 mgĪż(LĪżh)-1, Ųõ┤╬×ķĄĒĘ█2.91 mgĪż(LĪżh)-1, Č°╗ņ║Ž╠╝į┤Śl╝■Ž┬ūŅ┬², āH×ķ2.55 mgĪż(LĪżh)-1(łD 3).ę“┤╦, ęįĄ░░ūļ╦║═ĄĒĘ█×ķå╬ę╗╠╝į┤Ģr╚Š┴ŽRR2ĮĄĮŌ╦┘┬╩Ė▀ė┌╗ņ║Ž╠╝į┤. RasoolĄ╚蹊┐┴╦ęį╚ķ╦ßĪóŲŽ╠č╠Ū║═ęę┤╝×ķ╠╝į┤ĢrėĪ╚ŠÅU╦«╠Ä└Ēą¦╣¹, ĮY╣¹▒Ē├„┼cęįŲŽ╠č╠Ū×ķ╠╝į┤ŽÓ▒╚, ęį╚ķ╦ß║═ŲŽ╠č╠Ūū„×ķ╠╝į┤Ģr╔½Č╚╚ź│²┬╩╠ßĖ▀. CirikĄ╚╠Ä└Ē║¼ėąCrĄ─ėĪ╚ŠÅU╦«Ģrę▓░l¼F, ęę┤╝ū„×ķ╠╝į┤Ģr╔½Č╚╚ź│²┬╩▒╚ŲŽ╠č╠Ūū„×ķ╠╝į┤ĢrĖ▀.ę“┤╦╠╝į┤ĘNŅÉė░Ēæ┼╝Ą¬╚Š┴ŽĮĄĮŌĄ─ą¦╣¹.
ĪĪĪĪė╔▒Ē 2ųąRR2ĮĄĮŌ╦┘┬╩┐╔ų¬į┌▒ŠčąŠ┐ųą, 25ĪµŚl╝■Ž┬, CODØŌČ╚ė╔200 mgĪżL-1╠ßĖ▀ų┴400 mgĪżL-1║═800 mgĪżL-1, RR2ĮĄĮŌ╦┘┬╩Ęųäe╠ßĖ▀┴╦88.9%║═208.9%.į┌35ĪµŚl╝■Ž┬, CODØŌČ╚ė╔200 mgĪżL-1╠ßĖ▀ų┴400 mgĪżL-1║═800 mgĪżL-1, RR2ĮĄĮŌ╦┘┬╩Ęųäe╠ßĖ▀┴╦37.6%║═64.4%. RasoolĄ╚╠Ä└Ē║¼ėą┼╝Ą¬╚Š┴Žų▒Įė╝t80Ą─ÅU╦«, ░l¼FĘųäeīó╠╝į┤╚ķ╦ß¹}ĪóŲŽ╠č╠Ū║═ęę┤╝CODØŌČ╚Å─3000 mgĪżL-1ĮĄų┴500 mgĪżL-1Ģr, ╔½Č╚╚ź│²┬╩Å─98.23%ĮĄų┴78.46%Īó63.37%║═69.10%, ųĖ│÷Ė▀CODØŌČ╚─▄ē“╠ß╣®│õūŃļŖūė, ėą└¹ė┌┼╝Ą¬╚Š┴ŽĮĄĮŌ. CuiĄ╚ę▓░l¼FĮĄĮŌ╚Š┴Ž╦ßąį│╚7, «öęę╦ß¹}║═ŲŽ╠č╠Ū×ķ╠╝į┤ĢrļŖūė╣®¾w▓╗ūŃĢ■ī¦ų┬├ō╔½┬╩ĮĄĄ═.ę“┤╦«öCODØŌČ╚╠ßĖ▀Ģr, ļŖūė╣®¾wöĄ┴┐│õūŃ, ┼╝Ą¬╚Š┴ŽĮĄĮŌ╦┘┬╩├„’@Ė▀ė┌ļŖūė╣®¾w▓╗ūŃŚl╝■.
ĪĪĪĪ«öCODØŌČ╚Ęųäe×ķ200Īó400║═800 mgĪżL-1Ģr, £žČ╚ė╔25Īµ╠ßĖ▀ĄĮ35Īµ, RR2ĮĄĮŌ╦┘┬╩Ęųäe╠ßĖ▀┴╦231.1%Īó141.2%║═76.25%, Ė▀£žŽ┬╚Š┴ŽRR2ĮĄĮŌ╦┘┬╩╠ßĖ▀Ą─▒╚└²▀hĖ▀ė┌CODØŌČ╚į÷╝ėĢrĮĄĮŌ╦┘┬╩╠ßĖ▀Ą─▒╚└², šf├„CODØŌČ╚ī”RR2ĮĄĮŌ╦┘┬╩Ą─ė░Ēæø]ėą£žČ╚Ą─ė░Ēæ├„’@.ę“┤╦, ŠS│ųę╗Č©£žČ╚╩ŪÅŖ╗»┼╝Ą¬╚Š┴ŽRR2ĮĄĮŌĄ─ĻPµIę“╦žų«ę╗.
ĪĪĪĪ2.4 ╚Š┴Ž╝░Ųõųąķg«a╬’ī”Ž§╗»╗ŅąįĄ─ė░Ēæ
ĪĪĪĪłD 4(a)’@╩Š╚Š┴ŽRR2ØŌČ╚į┌0~64 mgĪżL-1ĘČć·ā╚, NO3--N╔·│╔╦┘┬╩╗∙▒Šę╗ų┬, ŪęļS╚Š┴ŽØŌČ╚į÷╝ė, NO3--N╔·│╔╦┘┬╩ø]ėąūā╗», šf├„╚Š┴ŽRR2ī”Ž§╗»▀^│╠ø]ėąė░Ēæ, į┌0~64 mgĪżL-1ØŌČ╚ĘČć·ā╚▓╗ė░Ē控╗»Š·Ą─╗Ņąį. SarvajithĄ╚[30]Ą─蹊┐░l¼FŽÓ▌^ė┌║├觌l╝■, ╬óč§(DO<0.5 mgĪżL-1)Śl╝■Ž┬└¹ė├Ņw┴Ż╬█─Ó╠Ä└Ē║¼ėą╗Ņąį³S15Ą─ÅU╦«Ģr, ┐╔ęįėąą¦╠ßĖ▀NH4+-N╚ź│²┬╩, Ūęį┌8 hā╚│÷¼FNO2--NĘe└█.▒ŠčąŠ┐ųą╚Š┴ŽRR2ī”Ą¬╚ź│²┬╩ø]ėąė░Ēæ, ┐╔─▄╩Ūė╔ė┌įć“×▀^│╠ųąDO×ķ7 mgĪżL-1, ę“┤╦RR2ī”Ž§╗»▀^│╠ė░Ēæ▓╗┤¾.
ĪĪĪĪłD 4
łD 4 ╚Š┴Ž║═▒Į░ĘęųųŲŽ§╗»įć“×ĪĪĪĪė╔łD 4(b)┐╔ų¬, ▒Į░ĘØŌČ╚Å─0 mgĪżL-1į÷╝ėĄĮ7.5 mgĪżL-1Ģr, NO3--N╔·│╔╦┘┬╩£pąĪ, šf├„▒Į░Ęī”Ž§╗»▀^│╠ėąęųųŲū„ė├. ShabbirĄ╚Ą─蹊┐▒Ē├„«ö▀M╦«▒Į░ĘØŌČ╚Ė▀ė┌250 mgĪżL-1Ģr, ü厧╦ß¹}Ą¬č§╗»Š·(NOB)╗Ņąį▒╗═Ļ╚½ęųųŲŪę▓╗─▄╗ųÅ═; «ö│§╩╝▒Į░ĘØŌČ╚×ķ100 mgĪżL-1Ģr, Ž§╗»Š·╗ŅąįĢ■▒╗ęųųŲ, Ą½īó▒Į░ĘØŌČ╚ĮĄų┴4 mgĪżL-1ęįŽ┬Ģr, Ž§╗»Š·╗Ņąį┐╔ęį╗ųÅ═.
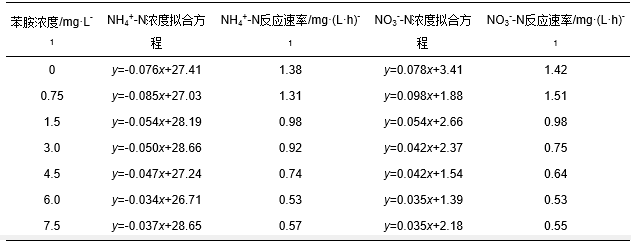
ĪĪĪĪĖ∙ō■Ę┤æ¬╦┘┬╩ėŗ╦ŃĮY╣¹(▒Ē 3), «ö▒Į░ĘØŌČ╚Å─0 mgĪżL-1į÷╝ėĄĮ6 mgĪżL-1Ģr, ░▒Ą¬č§╗»╦┘┬╩Å─1.38 mgĪż(LĪżh)-1£pąĪĄĮ0.53 mgĪż(LĪżh)-1, NO3--N╔·│╔╦┘┬╩║═░▒Ą¬č§╗»╦┘┬╩┌ģä▌ę╗ų┬, Ūęø]ėą│÷¼FNO2--NĘe└█, šf├„▒Šįć“×ųą▒Į░Ęų„ę¬ī”░▒Ą¬č§╗»Š·(AOB)╗ŅąįėąęųųŲū„ė├, Č°ī”NOB╗Ņąįø]ėąęųųŲū„ė├.«ö▒Į░ĘØŌČ╚į÷╝ėĄĮ7.5 mgĪżL-1Ģr, ░▒Ą¬č§╗»╦┘┬╩ø]ėą▀Mę╗▓ĮĮĄĄ═, šf├„▒Į░ĘØŌČ╚│¼▀^6 mgĪżL-1Ģr, Ž§╗»Ę┤æ¬▒╗ęųųŲĄĮūŅĄ═Ę┤æ¬╦┘┬╩, ×ķ0.53 mgĪż(LĪżh)-1ū¾ėę.įōĮY╣¹┼cķLŲ┌▀\ąą▀^│╠ųąNOB╗Ņąį▒╗ęųųŲ▓╗ę╗ų┬, ┐╔─▄╩Ūė╔ė┌įć“×ĮėĘN╬█─Ó×ķAOĘ┤æ¬Ų„ķLŲ┌±Z╗»╬█─Ó, NOB╗Ņąį▌^Ą═, ę“┤╦╝ė╚ļĄ═ØŌČ╚▒Į░Ę║¾, AOB╩ūŽ╚│÷¼F┴╦├„’@Ą─ęųųŲū„ė├.įć“×ųąĄ─Ę┤æ¬ĢrķgāH×ķ2 h, Ę┤æ¬Ģrķg▌^Č╠, ę“┤╦ø]ėą│÷¼FNOBęųųŲū„ė├. KhinĄ╚Ą─蹊┐ųąę▓░l¼Fų▄Ų┌įć“×ųą, Ę┤æ¬8 hū¾ėę║¾ęųųŲNOB╗Ņąį, Ūę▀M╦«▒Į░ĘØŌČ╚│¼▀^250 mgĪżL-1║¾NOB╗Ņąį▓╗─▄╗ųÅ═.
ĪĪĪĪ▒Ē 3 ▒Į░ĘęųųŲŽ§╗»įć“×Ę┤æ¬╦┘┬╩
ĪĪĪĪ3 ĮYšō
ĪĪĪĪ(1) ╦«ĮŌ╦ß╗»/AO╣ż╦ć╠Ä└Ē║¼ėąRR2Ą─ėĪ╚ŠÅU╦«Ģr, ┐╔ęįėąą¦╚ź│²╔½Č╚ĪóCOD║═NH4+-N, ╚ź│²┬╩Ęųäe×ķ71.0%Īó92.2%║═83.5%.
ĪĪĪĪ(2) ╦«ĮŌ╦ß╗»Ę┤æ¬Ų„ųąų„ę¬┼╝Ą¬╚Š┴ŽĮĄĮŌŠ·×ķDesulfovibrio, AOĘ┤æ¬Ų„ųąŽ§╗»Š·ų„ę¬×ķNitrospira, Ę┤Ž§╗»Š·×ķThauera║═Dechloromonas.
ĪĪĪĪ(3) ╦«ĮŌ╦ß╗»▀^│╠ųąCODØŌČ╚×ķ400 mgĪżL-1Ģr, £žČ╚ė╔25Īµ╠ßĖ▀ų┴35Īµ, ╔½Č╚╚ź│²┬╩╠ßĖ▀141.2%;£žČ╚×ķ25ĪµĢr, CODØŌČ╚Å─200 mgĪżL-1╠ßĖ▀ų┴800 mgĪżL-1, ╔½Č╚╚ź│²┬╩╠ßĖ▀208.9%.
ĪĪĪĪ(4) AOĘ┤æ¬Ų„ųą▒Į░ĘØŌČ╚×ķ1 mgĪżL-1Ģr, │÷¼FNO2--NĘe└█, ü厧╗»┬╩×ķ73.8%.╚Š┴ŽRR2ī”Ž§╗»▀^│╠ø]ėąęųųŲū„ė├, ▒Į░Ęī”Ž§╗»▀^│╠ėąęųųŲū„ė├.▒Į░ĘØŌČ╚│¼▀^6 mgĪżL-1Ģr░▒Ą¬č§╗»╦┘┬╩▀_ĄĮūŅĄ═ųĄ0.53 mgĪż(LĪżh)-1.