╬█╚Š╦«¾w╝{├ūĶFą▐Å═╝╝ąg蹊┐
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2017-6-2 9:36:28
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪ╝{├ū╝ē┴ŃārĶF(nano zero-valent iron, NZVI)ū„×ķę╗ĘNÅŖ▀ĆįŁä®, ─▄ē“į┌╚§╦ߣhŠ│Ž┬ĮĄĮŌųžĮī┘ĪóŽ§╦ß║═¹u┤·ėąÖC╬█╚Š╬’.╝{├ū╝ē┴ŃārĶFŽÓ▒╚Ųš═©┴ŃārĶFŠ▀ėąĖ³┤¾Ą─▒╚▒Ē├µĘe, Š▀ėąĖ³Ė▀Ą─Ę┤æ¬╗Ņąį, į┌ĄžŽ┬╦«ą▐Å═ŅIė“ęčĮøĄ├ĄĮŲš╝░.Ž“╦«¾wųąūó╚ļ╝{├ū┴ŃārĶFęčĮø▒╗ūCīŹ╩Ūę╗ĘNėąą¦Ą─╠Ä└Ē╬█╚ŠĄ─ĘĮĘ©, ╠žäe╩Ūī”ė┌╬█╚Šį┤ģ^ė“Ą─ų╬└Ē.Ą½╩Ūė╔ė┌╝{├ūŅw┴Żūį╔ĒĄ─┤┼┴”║═ĘČĄ┬╚A┴”Ą─ū„ė├, ┴ŃārĶFŅw┴Ż║▄╚▌ęūą╬│╔łFŠ█, Å─Č°ė░ĒæŲõį┌ČÓ┐ūĮķ┘|ųąĄ─▀węŲé„▌öŠÓļx.į┌▒ŖČÓ蹊┐ųą, NZVIæęĖĪę║▒╗ūó╚ļĄĮĄžŽ┬╦«ųą, 蹊┐Öz£yŲõī”┬╚┤·╚▄ä®║═╚▄ĮŌąį┬╚┤·ėąÖC╗»║Ž╬’Ą─įŁ╬╗╠Ä└Ēą¦╣¹.ėąčąŠ┐▒Ē├„, NZVIÅ─ūó╚ļ³cķ_╩╝ų╗ėą║▄Č╠Ą─▀węŲŠÓļx, Å─Č°Ž▐ųŲ┴╦╦³į┌╬█╚ŠĄžģ^Ą─Ęų▓╝ęį╝░ą▐Å═─▄┴”.═¼Ģrė╔ė┌╝{├ū╝ē┴ŃārĶFĄ─ęūč§╗»╩¦╗Ņ╠žąį, ┤¾┤¾Ž▐ųŲ┴╦╦³Ą─æ¬ė├║═░lš╣.
ĪĪĪĪ┬╚ĘėŅÉėąÖC╬’(CPs)ī”╔·╬’¾wėąČŠ║”ū„ė├, į┌╔·«a▀^│╠ųąĢ■▀M╚ļŁhŠ│, ī”╦«¾w║══┴╚└įņ│╔ć└ųž╬█╚Š.┬╚Ęėė╔ė┌Ųõ▒Š╔ĒĘ╝ŁhĮYśŗ║═┬╚┤·įŁūėĄ─┤µį┌Č°Š▀ėą║▄ÅŖĄ─┐╣ĮĄĮŌ─▄┴”, į┌Įo╦«╠Ä└Ēųą, ė├│ŻęÄ╣ż╦ć║═╔·╬’╠Ä└ĒļyęįĮĄĮŌ, ą┬ą═Ą─ļŖ╗»īWč§╗»Ę©, Ė▒«a╬’ųą┤µį┌ėąę╗ą®║¼┬╚Ą─ųąķg«a╬’, ų┬╩╣┬╚┤·ėąÖCÅU╦«Ą─ČŠąįę└╚╗║▄Ė▀, ╠Ä└Ē│╔▒Šę▓▌^Ė▀. GillhamĄ╚╠ß│÷┴ŃārĶF┐╔ė├ė┌ĄžŽ┬╦«Ą─įŁ╬╗ą▐Å═, ┬╚┤·ėąÖC╬’┐╔ęįėąą¦Ąž▒╗Įī┘ĶF▀ĆįŁ├ō┬╚.╦∙ęį╝{├ū┴ŃārĶF│╔×ķ┴╦ė├ė┌╠Ä└ĒĄžŽ┬╦«ųą┬╚ĘėŅÉėąÖC╬’Ą─¤ßķT▓─┴Ž, ×ķ┴╦▒▄├Ō╝{├ū╝ē┴ŃārĶFĄ─łFŠ█║═ęūč§╗»ū„ė├, į┌▒ŻūCŲõ╗ŅąįŽ┬▓╔ė├ę╗Č©Ą─Ė─ąįĘĮĘ©╠ßĖ▀╝{├ūĶFŅw┴ŻĄ─Ęų╔ó│╠Č╚ęį▒ŻūC╗»īWĘ┤欚²│Ż▀Mąą╩ŪĘŪ│Żųžę¬Ą─.
ĪĪĪĪĮ³Äū─Ļ╚╦éā蹊┐┴╦▌^ČÓĄ─░³Ė▓▓─┴Ž, ╚ńŠ█▒¹Ž®╦ß(PAA)ĪóŠ█ęꎮ┤╝(PVA)Īó¶╚╝ū╗∙└wŠS╦ž(CMC)ĪóÜżŠ█╠Ūęį╝░Ųõ╦¹ŅÉą═Ą─░³Ė▓▓─┴Ž, ▀@ą®╬’┘|▓╗āH─▄ėąą¦ūĶų╣╝{├ūĶFĄ─Š█╝»║═│┴ĮĄ, ╩╣Ųõį┌╦«ųą▒Ż│ų┴╝║├Ą─Ęų╔óąį, Č°Ūęī”╝{├ūĶFĄ─╗Ņąįė░Ēæ▌^ąĪ.ė╔ė┌īŹļHĄžŽ┬╦«Įķ┘|▒Ē├µČÓĦžōļŖ, ╦∙ęįĮø│ŻĢ■▀xė├ĦėąžōļŖ║╔Ą─īŹ“×▓─┴Ž, ┴ŅæęĖĪĄ─NZVIė╔ė┌ņoļŖ│Ō┴”Č°▒Ż│ųĘų╔ó, ę▓▓╗Ģ■į┌ĦžōļŖĄ─═┴╚└Ņw┴Ż▒Ē├µ╬³ĖĮ.Ųõųą, ¶╚╝ū╗∙ĄĒĘ█Ōc(CMS)╩Ūę╗ĘNŁhŠ│ėč║├ą═▓─┴Ž, ┐╔ė├ė┌╩│ŲĘĪóßt╦ÄĄ╚╣żśIųą, ▓óŪęārĖ±Ą═┴«.─▄ē“ŲĄĮą▐’Ś╝{├ūĶF▓óĮŌøQłFŠ█¼FŽ¾Ą─ū„ė├.į┌ę╗Č©Ą─▒╚└²Ž┬, ─▄ē“ūī╝{├ūĶF▒Ż│ų┴╝║├Ą─Ęų╔óąį, ▓óŪęį┌▒Ż│ųĘų╔óąįĄ─Ū░╠ߎ┬, ▀Ć─▄ē“Š▀ėą▌^Ė▀Ą─╗Ņąį, ┤╦ŅÉ蹊┐▀Ć╬┤ęŖł¾Ą└.
ĪĪĪĪę“┤╦, ▒ŠčąŠ┐ė├▓╗═¼▒╚└²Ą─CMS▀Mąą╝{├ūĶFĄ─Ė─ąį░³Ė▓, ═©▀^│┴ĮĄīŹ“×ī”▒╚ŲõĘų╔óąį║═æęĖĪąį, ═¼Ģr▀Mąą░³Ė▓▓─┴Žī”2, 4-Č■┬╚▒ĮĘėĄ─╚ź│²īŹ“×, Ęų╬÷ŲõĘ┤æ¬╗Ņąį, įōĮY╣¹ī”ė┌æ¬ė├╝{├ūĶFą▐Å═╬█╚Š╦«¾wŠ▀ėąųžę¬Ą─ęŌ┴x, ×ķ╝{├ūĶFį┌ĄžŽ┬╦«ŁhŠ│įŁ╬╗ą▐Å═Ą─▀\ė├ĄņČ©┴╦└Ēšō╗∙ĄA.
ĪĪĪĪ1 ▓─┴Ž┼cĘĮĘ©1.1 ▓─┴Ž┼cįćä®
ĪĪĪĪ▒ŠīŹ“ץ─įćä®ų„ę¬×ķ¶╚╝ū╗∙ĄĒĘ█Ōc(╔Ž║Ż¹£┐╦┴ų╔·╗»┐Ų╝╝ėąŽ▐╣½╦Š, Ęų╬÷╝ā)Īó┴“╦ßüåĶF(╠ņĮ“╩ąĖŻ│┐╗»īWįćä®ÅS, Ęų╬÷╝ā)Īó┼Üõ╗»Ōc(╠ņĮ“╩ąĖŻ│┐╗»īWįćä®ÅS, Ęų╬÷╝ā).Ųõ╦¹įćä®×ķ¤o╦«ęę┤╝(▒▒Š®╗»╣żÅS, Ęų╬÷╝ā)ĪóĄ¬ÜŌ(╣żśI╝ē).
ĪĪĪĪ1.2 ¶╚╝ū╗∙ĄĒĘ█Ōc░³Ė▓║═╬┤░³Ė▓╝{├ūĶFĄ─║Ž│╔
ĪĪĪĪĘQ╚Īę╗Č©┴┐Ą─¶╚╝ū╗∙ĄĒĘ█Ōc(CMSš╝┐é┘|┴┐Ą─┘|┴┐ĘųöĄ×ķ0.00%Īó66.67%Īó75.00%Īó80.00%Īó83.33%, ╝┤┘|┴┐▒╚CMS:Fe0×ķ0:1Īó2:1Īó3:1Īó4:1Īó5:1) ų├ė┌1 000 mLĄ─╚²┐┌¤²Ų┐ųą, ╝ė╚ļ250 mL├ōč§╚źļxūė╦«, │ų└m═©╚ļĄ¬ÜŌ15 min┤_▒Ż├ōč§, ═¼Ģr▓╗öÓöć░Ķų┴═Ė├„ż│ĒĀŅ.ĘQ╚Īę╗Č©┴┐Ą─┴“╦ßüåĶF(FeSO4ĪżH2O)╝ė╚ļCMS╚▄ę║ųą▓ó▓╗öÓöć░Ķ═©Ą¬ÜŌ, ┤²FeSO4ĪżH2O╚½▓┐╚▄ĮŌ║¾ė├╚õäė▒├ęį4 000 ”╠LĪżmin-1Ą─╦┘┬╩Ą╬╚ļ┼Üõ╗»Ōc╚▄ę║(NaBH4┼cFe2+─”Ā¢▒╚╝s×ķ2.2:1) 250 mLų┴╚▄ę║═Ļ╚½╚õ╚ļ╚²┐┌¤²Ų┐ųą.Ę┤æ¬ĘĮ│╠×ķŻ║
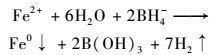
ĪĪĪĪĘ┤æ¬▀^│╠╩╝ĮK═©╚ļĄ¬ÜŌ├ōč§, Ą╬╝ė═Ļ«ģ║¾└^└möć░Ķ15 minęį▒Ń╔·│╔Ą─ÜõÜŌ═Ļ╚½┼┼│÷, ┤╦ĢrųŲéõ│÷Ą─╝{├ūĶF╚▄ę║╝┤╩ŪĘĆČ©ą═╝{├ū┴ŃārĶF╚▄ę║.ė├╚▄ä®▀^×VŲ„īóųŲéõ║├Ą─CMS-FeŅw┴Ż▀Mąą│ķ×V, ▓óė├╚źļxūė╦«║═ęę┤╝ŪÕŽ┤3┤╬, ╚ź│²ļs┘|ļxūė, ×ķ▒ŻūCŅw┴Ż▓╗▒╗č§╗», į┌│ķ×V▀^│╠ųąŽ“╚▄ę║│ų└m═©Ą¬ÜŌ├ōč§, │ķ×V═Ļ│╔║¾čĖ╦┘Ę┼╚ļšµ┐šĖ╔į’Žõųą, ┐žųŲ£žČ╚×ķ70Īµ, Ģrķg×ķ600 min, ▀MąąĖ╔į’╠Ä└Ē, éõė├.
ĪĪĪĪīóĖ╔į’║├Ą─╝{├ūŅw┴Ż▀Mąą═Ė╔õļŖńR(TEM)▒Ēš„(JEOL JEM-2100) ║═X╔õŠĆč▄╔õ(XRD)Ęų╬÷(D8ADVANCE).
ĪĪĪĪ1.3 ▓╗═¼░³Ė▓▒╚└²╝{├ūĶFĄ─│┴ĮĄīŹ“×╝░ŲõĘų╔óąį
ĪĪĪĪīó▓╗═¼ØŌČ╚┼õ▒╚Ą─CMSĖ─ąįĄ─ĘĆČ©ą═╝{├ū┴ŃārĶF╚▄ę║ęį╝░╬┤Ė─ąįĄ─╝{├ū┴ŃārĶF╚▄ę║ØŌČ╚┐žųŲį┌1 gĪżL-1, ╬³╚Ī╗ņ║ŽŠ∙ä“Ą─æęØßę║ė┌▒╚╔½├¾ųą, īó▒╚╔½├¾ūóØM(▒╚╔½├¾╔Ž▀ģŠēą╬│╔═╣ę║├µ), ╔w╔Ž╦▄┴Ž╔w, ōu╗╬╩╣ā╚▓┐╚▄ę║Ęų╔óŠ∙ä“, čĖ╦┘Ę┼╚ļūŽ═Ō┐╔ęŖĘų╣Ō╣ŌČ╚ėŗ(ė╚─ß┐┬2082S UV/VIS)ųą, Æ▀├Ķ▓©ķL×ķ508 nm, Æ▀├ĶĢrķg×ķ5 400 s, ▀Mąąäė┴”īW£yįć.
ĪĪĪĪ1.4 ▓╗═¼░³Ė▓▒╚└²╝{├ūĶF╚ź│²╦«ųą2, 4-Č■┬╚ĘėĄ─īŹ“×
ĪĪĪĪį┌┴ŃārĶF▒Ē├µÕā╔Ž┴Ēę╗ĘN▀ĆįŁļŖ╬╗Ė▀Ą─Įī┘, ą╬│╔ļpĮī┘▓─┴Ž┐╔╝ė┐ņ┴ŃārĶFĖ»╬g╦┘Č╚, ╠ßĖ▀┴ŃārĶFĄ─Ę┤æ¬╗Ņąį, Å─Č°┤¾┤¾╠ßĖ▀ī”┬╚┤·¤NĄ─▀ĆįŁ├ō┬╚╦┘┬╩.×ķ╩╣Ę┤æ¬─▄ē“┐ņ╦┘▀Mąą, į┌īŹ“×ųą╝ė╚ļ▓╗┼c2, 4-DCPĘ┤æ¬Ą─µć(Ni)ū„×ķ┤▀╗»ä®, ą╬│╔Fe/NiļpĮī┘.Åłąl╚AĄ─蹊┐▒Ē├„, ļpĮī┘ųąNiĄ─┘|┴┐ĘųöĄė╔2%╠ßĖ▀ĄĮ5%Ģr, ├ō┬╚ą¦╣¹’@ų°į÷╝ė.«öNi┘|┴┐ĘųöĄ└^└mį÷╝ėĄĮ10%Ģr, ├ō┬╚ą¦╣¹ļm╚╗ę▓└^└mį÷╝ė, Ą½ø]ėąŪ░š▀├„’@.╦∙ęį, ▒Šų°ĮøØ·įŁät, ▒ŠīŹ“×ļpĮī┘ųąNiĄ─┘|┴┐ĘųöĄ▀xė├5%.ĘQ╚Ī┘|┴┐ĘųöĄš╝Fe0×ķ5%┴“╦ßµć(NiSO4Īż6H2O)Ņw┴Ż, ╝ė╚ļĄĮCMSĖ─ąįĄ─ĘĆČ©ą═╝{├ū┴ŃārĶF╚▄ę║ųą, öć░Ķ15 min, ╩╣ĶF║═µćĘ┤æ¬═Ļ╚½.ė╔ė┌║═µćĘ┤æ¬╔·│╔Ą─Fe2+Ģ■▒╗╚▄ę║ųą▀^┴┐Ą─NaBH4▀ĆįŁ│╔Fe0.Ę┤æ¬ĘĮ│╠╩Į╚ńŽ┬Ż║
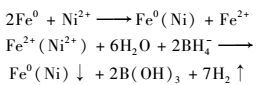
ĪĪĪĪīó300 mLę╗Č©ØŌČ╚Ą─2, 4-Č■┬╚▒ĮĘė(2, 4-DCP)╚▄ę║ų├ė┌500 mLįćä®Ų┐ųą, ▒Ż│ų╚▄ę║×ķųąąįŚl╝■, ╝ė╚ļę╗Č©┴┐Ą─Ė─ąį╝{├ūĶF, į┌20Īµ║Ń£žŚl╝■Ž┬, ęį150 rĪżmin-1Ą─š±╩Ä╦┘Č╚Ę┤æ¬.į┌▓╗═¼Ģrķg(1 minĪó5 minĪó10 minĪó20 minĪó30 minĪó60 minĪó90 minĪó2 hĪó3 hĪó4 hĪó5 hĪó6 hĪó7 h)ė├ūó╔õŲ„╚Īśė▓ó═©▀^0.45 ”╠m║═0.22 ”╠mĄ─Š█├čĒ┐╦«ŽĄ×VŅ^▀Mąą▀^×V, ▀_ĄĮ╬█╚Š╬’┼cĖ─ąį╝{├ū┘NĶFŅw┴ŻĄ─Ęųļxū„ė├, └¹ė├Ė▀ą¦ę║ŽÓ╔½ūVāxī”2, 4-DCP╝░ŲõĮĄĮŌ«a╬’2-┬╚Ęė(2-cp)Īó4-┬╚Ęė(4-cp)Īó▒ĮĘė(p)Ą─ØŌČ╚▀Mąą£yČ©, īŹ“×▓╔ė├C18╔½ūVų∙, ┴„äėŽÓ×ķ╝ū┤╝(60%)║═╚źļxūė╦«(40%)Ą─╗ņ║Žę║, ┴„╦┘×ķ1 mLĪżmin-1, ų∙£ž30Īµ, į┌┤╦Śl╝■Ž┬2, 4-DCPĄ─▒Ż┴¶Ģrķg┤¾╝sį┌8minū¾ėę.═©▀^▒╚ī”ĘÕ├µĘe/ØŌČ╚ś╦ŠĆ, ėŗ╦Ń│÷▓╗═¼Ģr┐╠╦«ųą2, 4-DCPĪó2-cpĪó4-cpĪópĄ─ØŌČ╚.
ĪĪĪĪ2 ĮY╣¹┼cėæšō2.1 Ė─ąį║═╬┤Ė─ąį╝{├ūĶFĄ─╬óė^ĮYśŗ
ĪĪĪĪĖ∙ō■TEM▒Ēš„┐╔ęį░l¼F, ═©▀^ę║ŽÓ▀ĆįŁĘ©ųŲéõ│÷Ą─╝āNZVIŅw┴Ż[łD 1(a)], Ņw┴Żą╬ĀŅ×ķŪ“ą╬, ┴ŻÅĮ═©│Żį┌40~80 nm, ×ķ╝{├ū╝ē▓─┴Ž.Ą½╝āNZVIŅw┴Żų«ķgŽÓ╗ź╬³ę², łFŠ█, Ęų╔óą¦╣¹▌^▓Ņ.Č°▒╗Ė─ąį▀^Ą─NZVIŅw┴Ż, ŲõųąCMS╦∙š╝▒╚└²×ķ80%, ╚ńłD 1(b)║═1(c)╦∙╩Š, ┴ŻÅĮ├„’@į÷┤¾, ┤¾╝sį┌80~100 nmū¾ėę, ▀@╩Ūė╔ė┌═Ōć·░³Ė▓┴╦¶╚╝ū╗∙ĄĒĘ█Ōc, ═¼ĢrNZVIĄ─łFŠ█¼FŽ¾ėą┴╦║▄┤¾Ą─Ė─╔Ų, ×ķĘų╔óŅw┴Ż╗“š▀µ£ĀŅĘų▓╝.
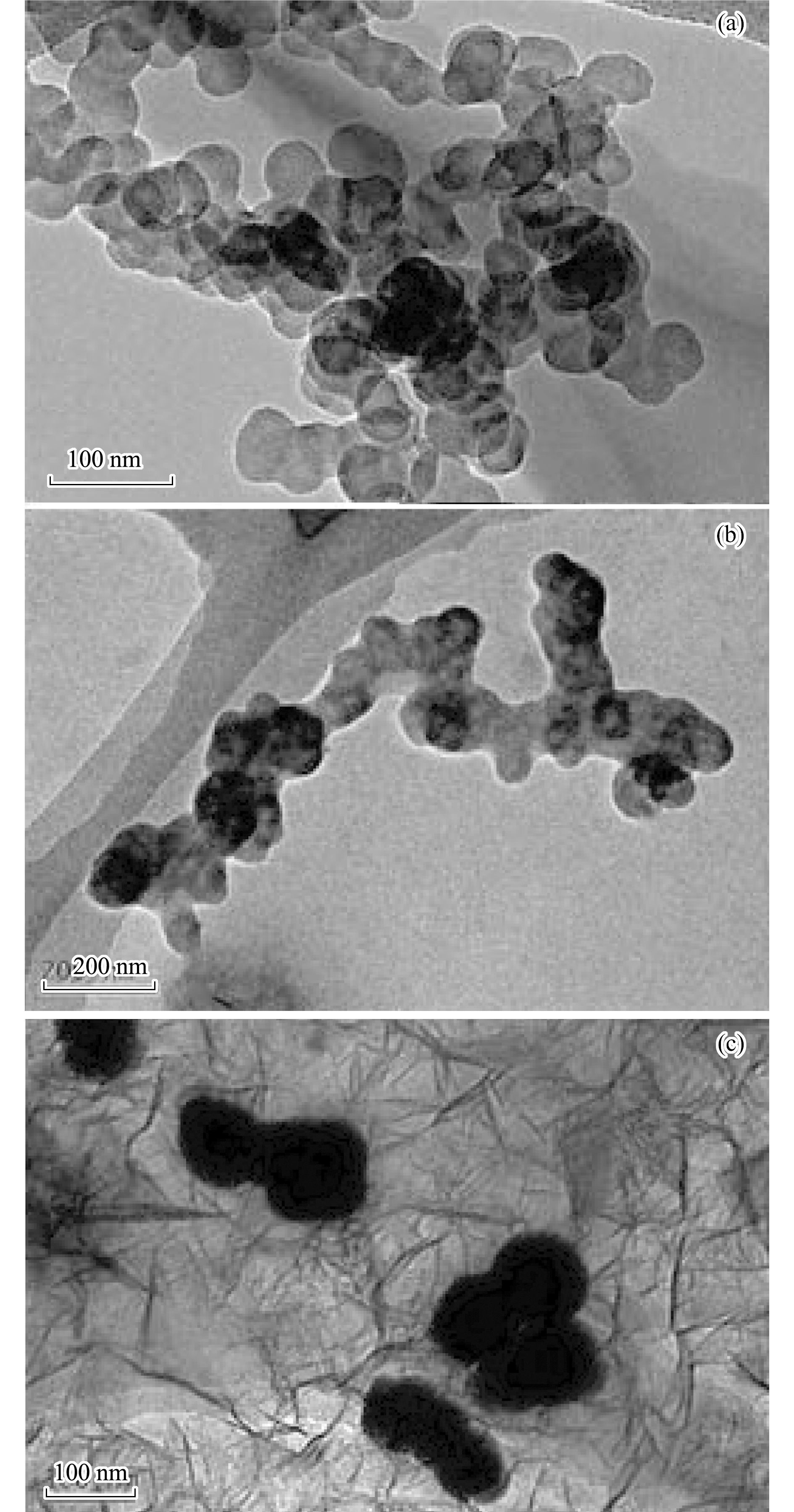
łD 1 ųŲéõ╝{├ūĶFĄ─═Ė╔õļŖńRłDŽ±
ĪĪĪĪ╝{├ūŅw┴ŻĄ─╬óė^ĮYśŗ╚ńłD 2╦∙╩Š, CMS┤¾ĘųūėųąĄ─¶╚╗∙µI─▄ē“╬³ĖĮĮī┘ļxūė▓óŪęŠ▀ėą┴╝║├Ą─ÖCąĄąį─▄, ┐╔═©▀^ļp²Xć¦║Ž╗“╝▄ś“ū„ė├╩╣ŲõĖĮų°į┌╝{├ūĶFŅw┴Ż▒Ē├µ, ┴Ņ╝{├ūŅw┴Żų▒ÅĮūā┤¾.ė╔ė┌▒Ē├µĄ─CMS┤¾Ęųūė┤µį┌, ╝{├ūĶFŅw┴Żų«ķgĄ─┤┼ąįę²┴”£pąĪ, CMSųą╦∙║¼Ą─┴u╗∙ę▓─▄ē“Ōg╗»╝{├ūĶFŅw┴ŻĄ─▒Ē├µ, Å─Č°ėąą¦ūĶų╣┴╦Ņw┴ŻłFŠ█.╝{├ūĶFŅw┴Żį┌CMSĄ─ū„ė├Ž┬ęįĘų╔óą═Ņw┴Ż╗“š▀Ślµ£ĀŅæB┤µį┌.
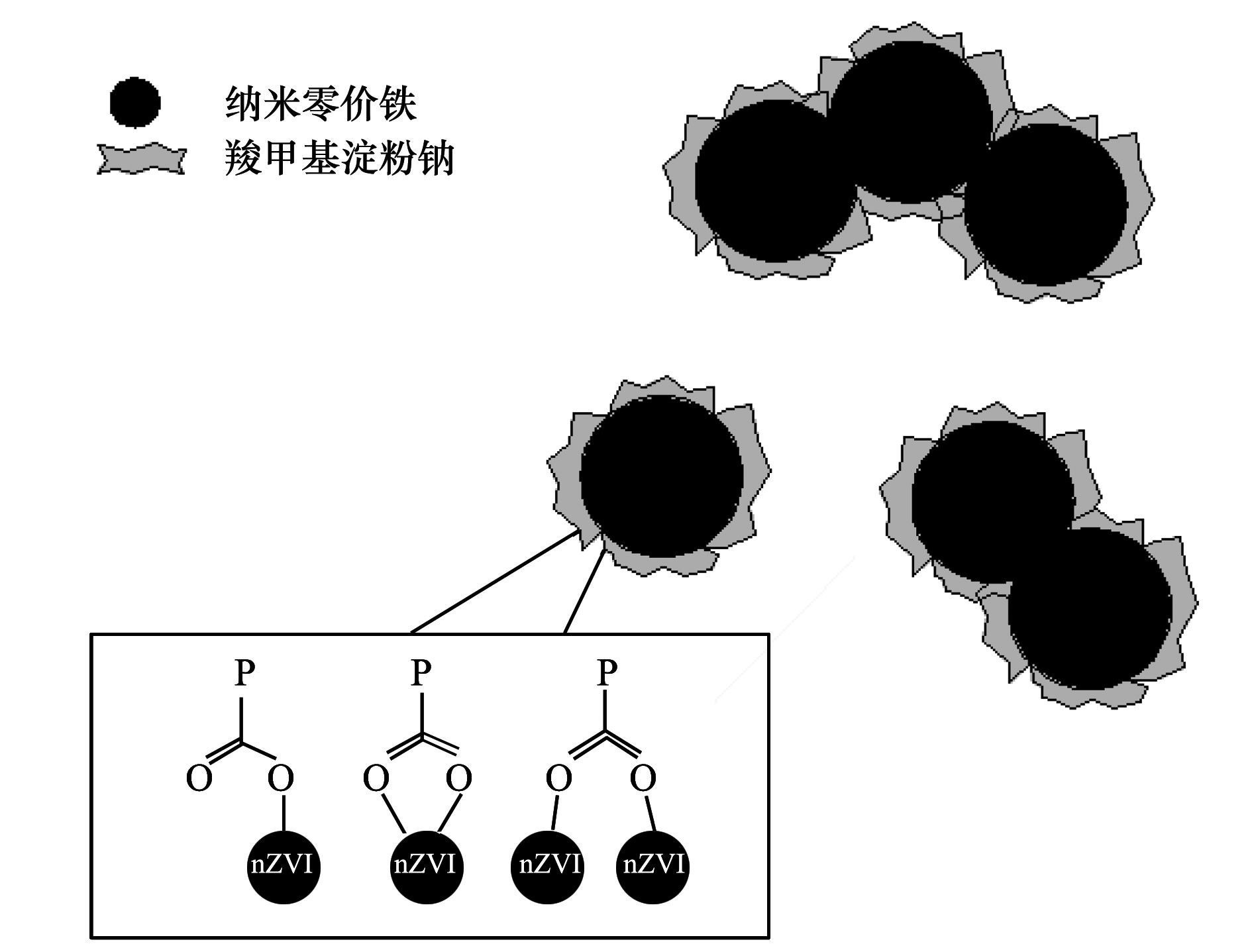
łD 2 Ė─ąį╝{├ū┴ŃārĶF╬óė^ĮYśŗĖ┼─Ņ
ĪĪĪĪłD 3Ą─XRD╠žš„łDūVšf├„īŹ“×╩ęųŲéõĄ─CMSĖ─ąį╝{├ūĶF×ķ┴ŃārĶF, ▓óŪęŠ▀ėą║▄Ė▀Ą─▀ĆįŁąį.Å─ųą┐╔ęį┐┤ĄĮč▄╔õĘÕ┼cś╦£╩┴óĘĮŠ¦ŽĄą═Fe0║═š²Į╗Š¦ŽĄą═CMSę╗ų┬, ▒Ē├„Ą─┤_ųŲéõ│÷─┐ś╦«a╬’, Č°ŪęĘÕą═╝ŌõJ, č▄╔õÅŖČ╚Ė▀, šf├„«a╬’Š¦ą═┴╝║├.Ųõųą╝t╔½ś╦ūRĄ─╠žš„ĘÕ╩Ū┴óĘĮŠ¦ŽĄą═Fe0Ą─╠žš„č▄╔õĘÕ.ŠG╔½ś╦ūRĄ─╠žš„ĘÕ╩Ūš²Į╗Š¦ŽĄą═CMSĄ─╠žš„č▄╔õĘÕ, │²┤╦ų«═Ō▓ó╬┤░l¼FŲõ╦¹╬’┘|Ą─č▄╔õĘÕ, šf├„╦∙ųŲéõĄ─«a╬’╝āš², ¤oļs┘|.
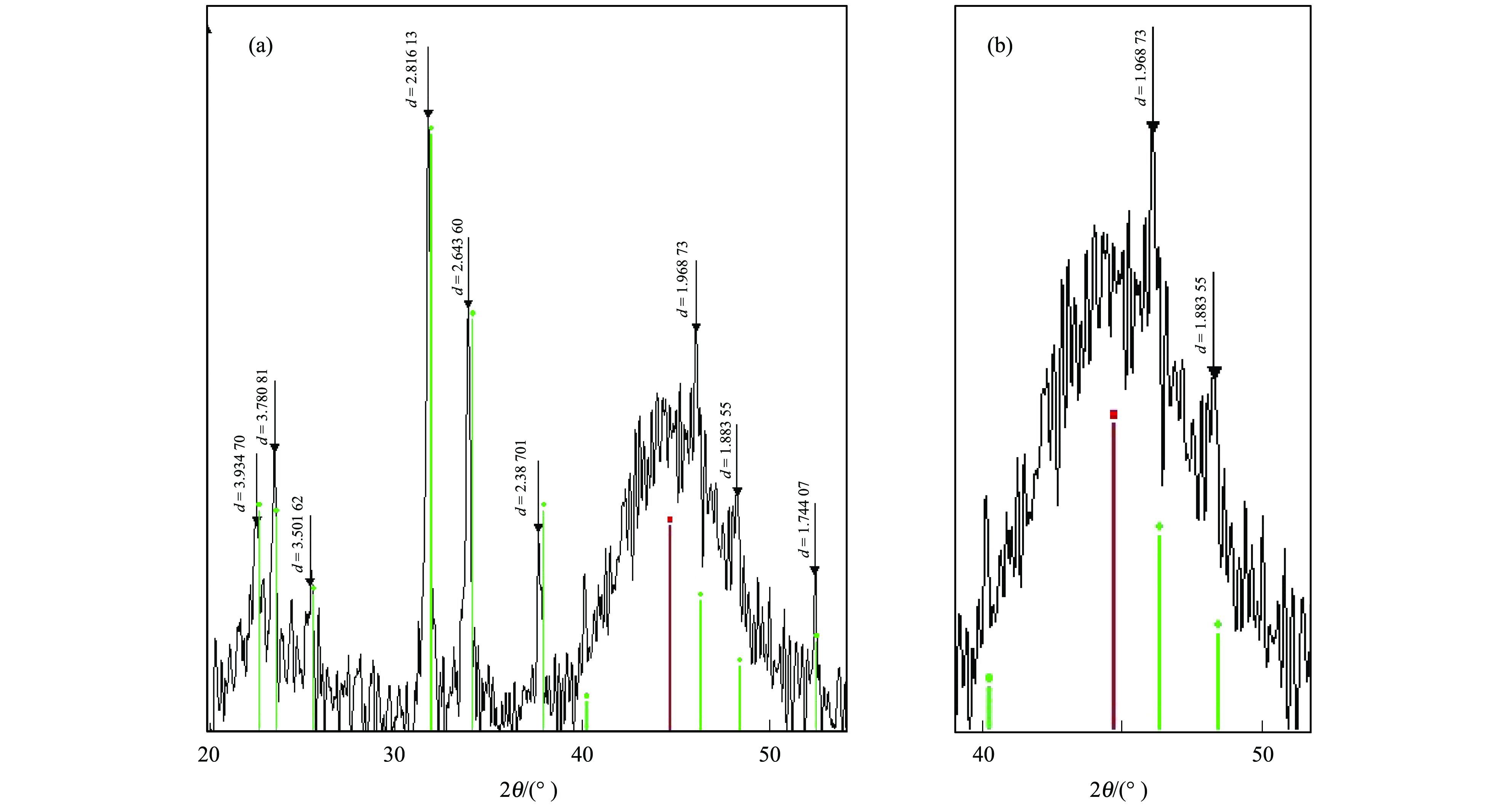
(b)×ķ(a)ųąī”æ¬╬╗ų├Ą─Ę┼┤¾
łD 3 ĄĒĘ█Ė─ąį╝{├ūĶFĄ─XRDūVłD
ĪĪĪĪ2.2 Ė─ąį║═╬┤Ė─ąį╝{├ūĶFĄ─│┴ĮĄ║═Ęų╔óĘĆČ©ąį
ĪĪĪĪę¾Ųõ┴┴Ą─蹊┐▒Ē├„, ī”ė┌nZVI/30%CMCą§─²Ųų„ę¬ū„ė├Īóī”ė┌nZVI/150%CMCĪóZVI/500%CMCät╩ŪĘĆČ©Ųų„ę¬ū„ė├; ļSų°Ė─ąįä®╠Ē╝ė┴┐Ą─į÷╝ėĘĆČ©ąįųØuį÷ÅŖ, ╦∙ęįĘų╔óä®CMS▓╔ė├┘|┴┐▒╚CMS:Fe0×ķ0:1Īó2:1Īó3:1Īó4:1Īó5:1, ╝┤š╝┐é┘|┴┐Ą─┘|┴┐ĘųöĄ×ķ0.00%Īó66.67%Īó75.00%Īó80.00%Īó83.33%. łD 4×ķĄ╚ØŌČ╚▓╗═¼┼õ▒╚CMS-FeĄ─│┴ĮĄŪ·ŠĆ, CMSĘųäeš╝┐é┘|┴┐Ą─┘|┴┐ĘųöĄ×ķ0.00%Īó66.67%Īó75.00%Īó80.00%Īó83.33%, ÖMū°ś╦×ķĢrķg, ┐vū°ś╦×ķ£yČ©Ģr╬³╣ŌČ╚A┼c│§╩╝╬³╣ŌČ╚A0Ą─▒╚ųĄ, ▒Ē╩Š×ķŽÓī”╬³╣ŌČ╚A/A0.ė╔ė┌▒╚╔½├¾╣▄▒┌╔Žę▓Ģ■ĖĮų°╔┘┴┐ĶF, ╦∙ęį╬³╣ŌČ╚╩╝ĮK▓╗×ķ0.Å─ųą┐╔ęį┐┤│÷Ż║┼õ▒╚×ķ75.00%┼c80.00%Ą─CMS-Fe│┴ĮĄŠÅ┬², į┌30 minų«║¾, │┴ĮĄ┌ģė┌ŲĮŠÅ, ŪęĘų╔óą¦╣¹║├, ▀@╩Ūė╔ė┌¶╚╝ū╗∙ĄĒĘ█ŌcĘųūėīėų«ķgĄ─┐šķg╬╗ūĶ║═ņoļŖ│Ō┴”─▄ē“Ąų┐╣╝{├ūĶFŅw┴Żų«ķgĄ─┤┼┴”╬³ę², ┴ŅŲõłFŠ█ą¦╣¹┤¾┤¾£p╚§Å─Č°į÷╝ėŲõĘų╔óąį; ┼õ▒╚×ķ66.67%┼c83.33%Ą─CMS-Fe│┴ĮĄ▌^┐ņ, į┌10 minų«║¾, │┴ĮĄ┌ģė┌ŲĮŠÅ, ŪęĘų╔óą¦╣¹▌^▓Ņ; ╚╗Č°┼õ▒╚×ķ0.00%Ą─NZVI│┴ĮĄ╦┘Č╚ūŅ┐ņ, į┌5 minų«║¾, │┴ĮĄ┌ģė┌ŲĮŠÅ, Ęų╔óą¦╣¹ūŅ▓Ņ, Äū║§═Ļ╚½│┴ĄĒ, ė╔ė┌╝{├ūĶFŅw┴Żų«ķg┤┼ąįĄ─ū„ė├, Ņw┴Ż┼cŅw┴ŻĢ■║▄┐ņŠ█╝»łFŠ█į┌ę╗Ųą╬│╔▌^┤¾Ņw┴Ż, ļSų«ė╔ė┌ųž┴”Ģ■čĖ╦┘Ž┬│┴.═©▀^ī”▒╚▓╗═¼CMS▒╚└²Ą─CMS-FeĄ─│┴ĮĄŪ·ŠĆ, ┐╔ęį┐┤│÷Ż║CMS▒╚└²▀^ąĪ╗“▀^┤¾Š∙▓╗└¹ė┌NZVIį┌╦«ųąĄ─Ęų╔óą¦╣¹, ų╗ėąį┌▀m«öĄ─▒╚└²▓┼─▄╩╣NZVIį┌╦«ųąĄ─Ęų╔óą¦╣¹ūŅ╝č, ┼õ▒╚×ķ80.00% CMS-FeĄ─│┴ĮĄŪ·ŠĆūŅ×ķŲĮŠÅ, ūŅĮKŽÓī”╬³╣ŌČ╚×ķ0.713šf├„ŲõĘų╔óæęĖĪąįūŅ║├.
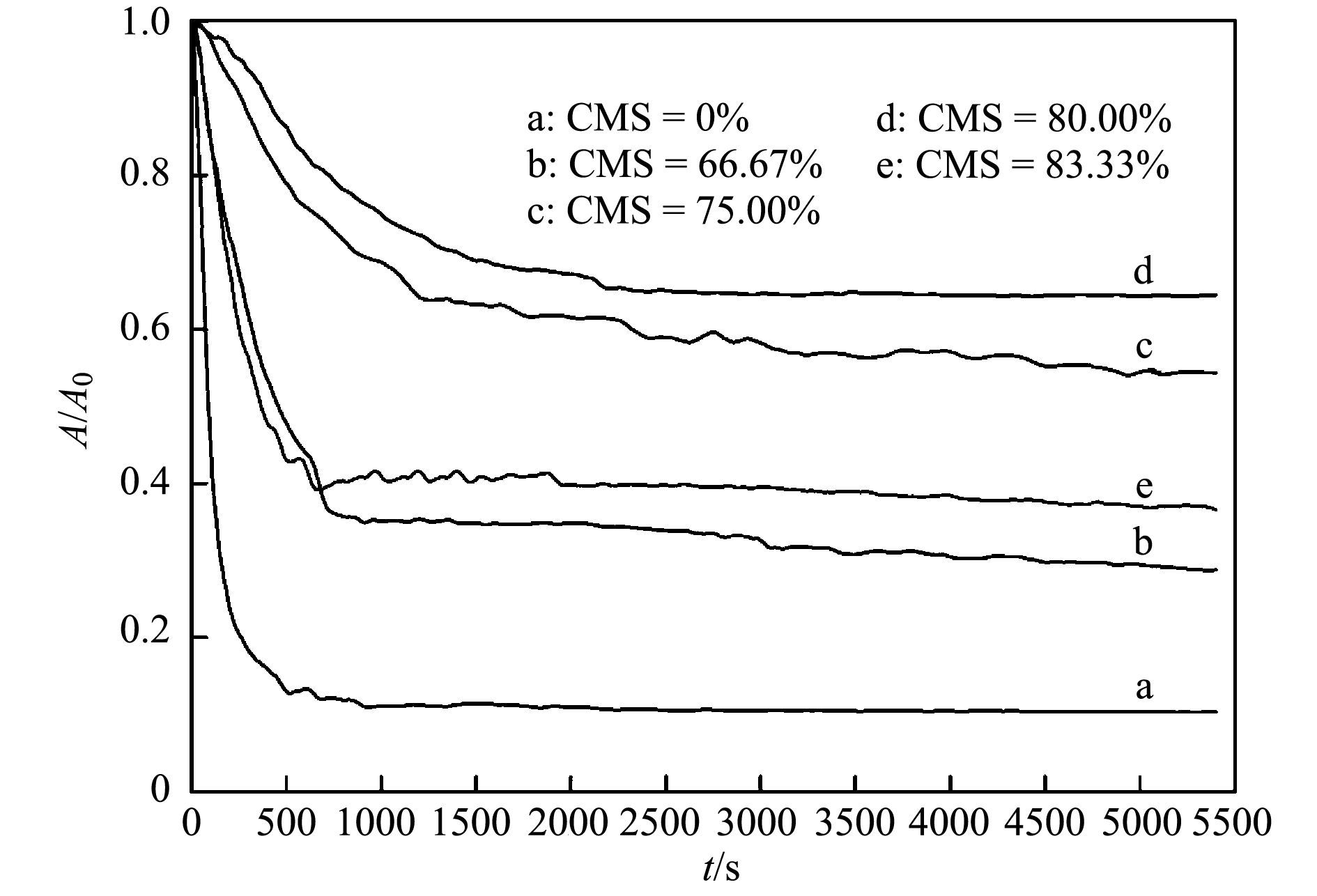
łD 4 ▓╗═¼ŅÉą═Ą─╝{├ūĶFį┌╦«╚▄ę║ųąĄ─│┴ĮĄ╣ŌūVŪ·ŠĆ
ĪĪĪĪ2.3 ▓╗═¼░³Ė▓▒╚└²╝{├ūĶF╚ź│²╦«ųą2, 4-Č■┬╚▒ĮĘė
ĪĪĪĪ«ö¾wŽĄ×ķ╦ßąįĢr, 2, 4-DCPĄ─ĮĄĮŌ╦┘┬╩ūŅ┐ņ, ųąąį┤╬ų«, ēAąįŚl╝■Ž┬Äū║§ø]ėąĮĄĮŌ, ┴Ē═Ōį┌╦ßąįŚl╝■Ž┬, 2, 4-DCP│╩ĘųūėĀŅæBęūō]░l, ųąąįŚl╝■Ž┬ō]░l┬╩║▄╔┘, ēAąįŚl╝■Ž┬│╩ļxūėĀŅæB, ▓╗ęūō]░l.╦∙ęį▒ŠīŹ“×▓╔ė├ųąąįŚl╝■Ž┬▀MąąĘ┤æ¬, ╝╚─▄▒ŻūC▌^┐ņĄ─ĮĄĮŌ╦┘┬╩ėų┐╔─▄£p╔┘ō]░l.
ĪĪĪĪ╝ā╝{├ū┴ŃārĶFŅw┴Żį┌ūį╔Ē┤┼┴”║═ĘČĄ┬╚A┴”Ą─ū„ė├Ž┬░l╔·łFŠ█, ą╬│╔ų▒ė^┐╔ęŖĄ─┤¾ēKłFŠ█¾w, ▒╚▒Ē├µĘe£pąĪ, ┼cĘ┤æ¬╬’Įėė|├µĘeę▓┤¾┤¾£p╔┘.«ö╝{├ū┴ŃārĶF▒Ē├µėąĘų╔óä®CMS┤µį┌Ģr, CMSĘųūėųą║¼ėąĄ─¶╚╗∙─▄ē“┼cĮī┘ļxūėęįļp²X╝▄ś“Ą─ą╬╩Į│╔µI, Å─Č°īóųŲéõ╝{├ūĮī┘Ņw┴ŻĄ─Ū░¾wFe2+Š∙ä“Ęų╔óį┌Ī░╝{├ūĘ┤æ¬Ų„Ī▒ųą, ▓óį┌▀ĆįŁä®(NaBH4)▀ĆįŁŽ┬čĖ╦┘│╔║╦, ūŅĮKĄ├ĄĮĘĆČ©Ęų╔óĄ─╝{├ūŅw┴Ż.┤╦ĢrĄ─╝{├ūĶFŅw┴Ż▒╚▒Ē├µĘeę¬▒╚╝ā╝{├ūĶFŅw┴Ż┤¾Ą├ČÓ, CMSī”ė┌2, 4-DCPę▓ėąę╗Č©╬³ĖĮ─▄┴”, ┐╔ęį┼c╬█╚Š╬’2, 4-DCP│õĘųĮėė|▓ó░l╔·├ō┬╚Ę┤æ¬, łD 5▒Ē╩Š┴╦CMS-Fe/Ni┼c┬╚ĘėĘ┤æ¬Ą─ÖCųŲ═ŠÅĮ, ┼c2, 4-DCPĄ─Ę┤æ¬ĘĮ│╠╩Į╚ńŽ┬Ż║
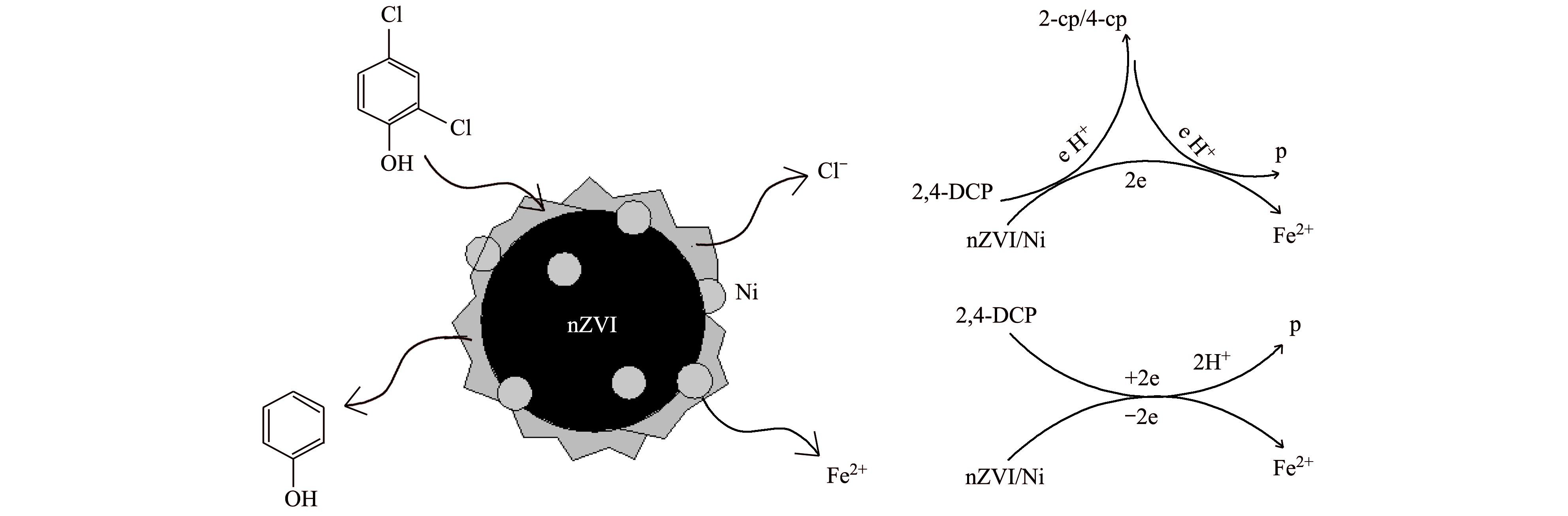
łD 5 CMS-Fe/Ni┼c2, 4-DCPĘ┤æ¬ÖCųŲ
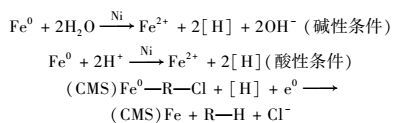
ĪĪĪĪłD 6×ķ▓╗═¼ŅÉą═╝{├ū┴ŃārĶF╚ź│²╦«ųą2, 4-DCPĄ─Ū·ŠĆ.Å─ųą┐╔ęį┐┤│÷╝āFe0(CMS=0.00%)ī”ė┌2, 4-DCPĄ─╚ź│²ą¦╣¹ūŅ▓Ņ, ╚ź│²┬╩┤¾╝sį┌23.62%ū¾ėę, ▀@╩Ūė╔ė┌╝āFe0į┌╦«ųąęūłFŠ█, ╩╣Ųõ▒╚▒Ē├µĘe£p╔┘, ┼c╬█╚Š╬’Įėė|├µĘeūā╔┘, Ūę╚▌ęū▒╗č§╗»╩¦╗Ņ.Č°Ęų╔óą¦╣¹┴╝║├Ą─╝{├ūĶFī”ė┌2, 4-DCPĄ─╚ź│²ą¦┬╩ät┤¾┤¾į÷ÅŖ.«öĘų╔ó䮥─▒╚└²Å─66.67%į÷╝ėĄĮ83.33%Ģr, ╝┤CMS:Fe0×ķ2:1Īó3:1Īó4:1Īó5:1Ģr, ╚ź│²┬╩Ęųäe×ķ61.32%Īó77.28%Īó83.69%║═60.83%.
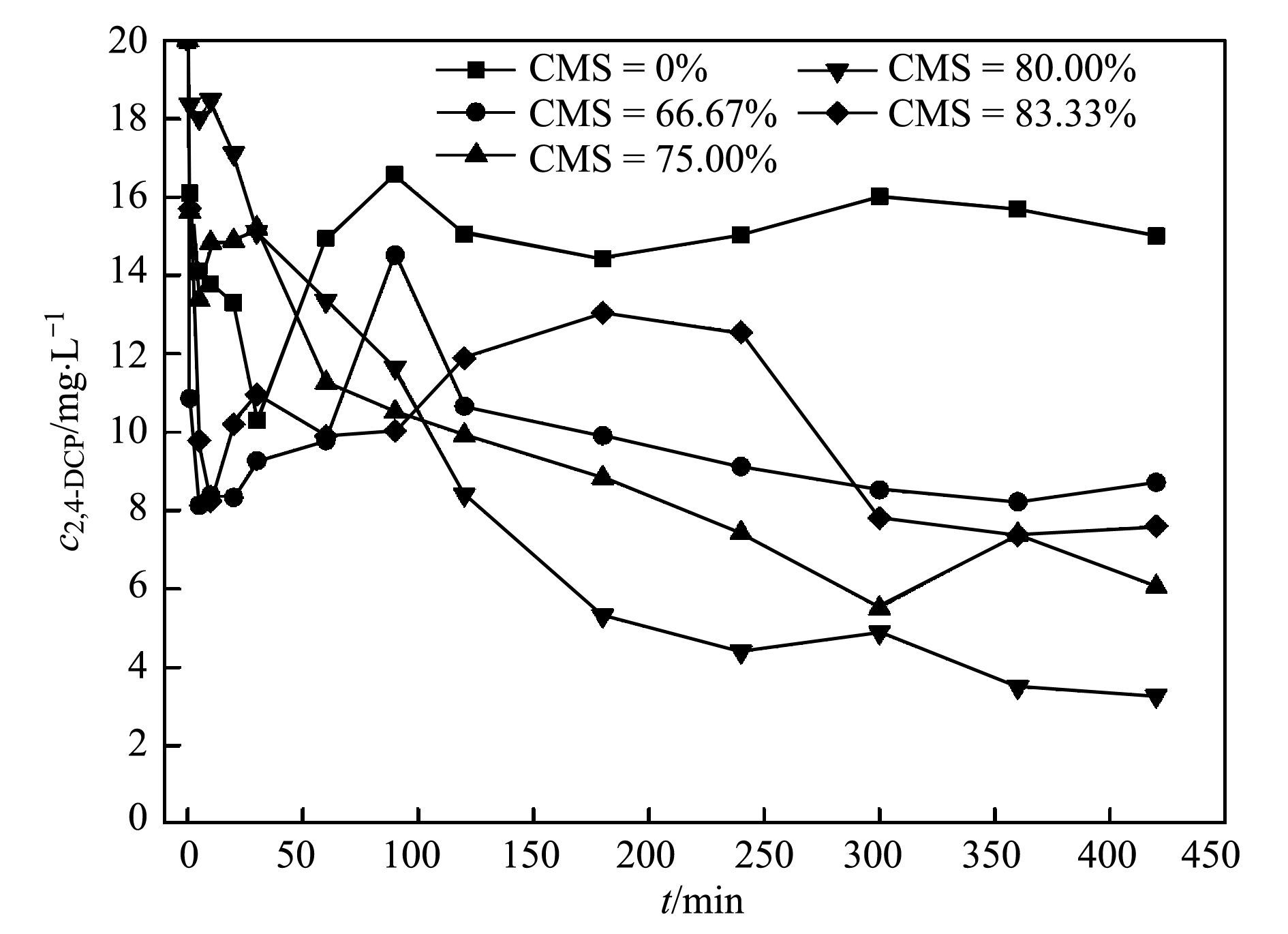
łD 6 ▓╗═¼ŅÉą═Ą─╝{├ū┴ŃārĶF╚ź│²╦«ųą2, 4-DCPØŌČ╚ūā╗»
ĪĪĪĪÅ─łD 6ųą┐╔ęį┐┤│÷, į┌═Č╚ļĘų╔óą═╝{├ūĶFŠ█║Ž╬’║¾, ╬█╚Š╬’2, 4-DCPĄ─ØŌČ╚Ģ■į┌ķ_╩╝Ą─60 minā╚čĖ╦┘ĮĄĄ═ĄĮ▀_ę╗éĆĢ║ĢrĄ─ūŅĄ═ųĄ, ╚╗║¾Ģ■ėąąĪĘ∙Č╚Ą─╔²Ė▀, ūŅ║¾į┘▓╗öÓĮĄĄ═, ØŌČ╚ųĄį┌Įø▀^300 min║¾Č╝╗∙▒Š┌ģė┌ŲĮĘĆ.▀@╩Ūė╔ė┌░³Ė▓į┌╝{├ūĶF▒Ē├µĄ─CMSī”ė┌╬█╚Š╬’ėąę╗éĆ╬³ĖĮū„ė├, į┌═Č╚ļ║¾─▄ē“čĖ╦┘╬³ĖĮ╬█╚Š╬’ĄĮ▓─┴Ž▒Ē├µ, į÷┤¾┴╦NZVIĖĮĮ³2, 4-DCPØŌČ╚, ╬³ĖĮĄ─2, 4-DCP▒╗NZVI├ō┬╚▀ĆįŁ, ╔·│╔2-cpĪó4-cp║═p, ų«║¾Ģ■░l╔·├ōĖĮ, Ųõųąę╗▓┐Ęų╬█╚Š╬’ėų┬²┬²ĮŌ╬÷ĄĮ╚▄ę║ųą, ├ōĖĮ╦┘┬╩┤¾ė┌ĮĄĮŌ╦┘┬╩, ╦∙ęį┤╦Ģr╚▄ę║ųąĄ─╬█╚Š╬’ØŌČ╚Ģ■ėąąĪĘ∙╠ßĖ▀.═¼ĢrĘų╔ó䮥─┤µį┌┐╔ęį╠ßĖ▀╝{├ūĶFĄ─Ę┤æ¬╗Ņąį, ļSų°Ęų╔óä®▒╚└²Ą─į÷╝ė, Š█║Ž╬’Ą─╚ź│²ą¦┬╩ę▓ļSų«į÷╝ė, ╚ź│²ą¦╣¹įĮ├„’@.į┌╬█╚Š╬’ØŌČ╚ę╗Č©Ģr(20mgĪżL-1), CMSš╝Š█║Ž╬’▒╚└²įĮČÓ, ╚ź│²ą¦╣¹įĮ║├, «ö▀_ĄĮ┐é┴┐Ą─80.00%Ģr, ╝┤CMS:Fe0=4:1Ģr, ī”ė┌2, 4-DCPĄ─╚ź│²┬╩ūŅĖ▀, ▀_ĄĮ┴╦83.69%.ų«║¾ļSų°▒╚└²Ą─į÷╝ė, ė╔ė┌╝{├ūĶFŅw┴Ż▒Ē├µCMS┴┐▀^ČÓ, ūĶĄKĶF┼c2, 4-DCPĮėė|, ╚ź│²┬╩Ž┬ĮĄ, ╗žĄĮ┴╦60.83%.ė╔┤╦┐╔ęįĄ├│÷, Ęų╔ó䮚╝Š█║Ž╬’Ą─▒╚└²×ķ80.00%Ģr, ī”ė┌╬█╚Š╬’Ą─╚ź│²ą¦╣¹ūŅ║├.
ĪĪĪĪŪ░╬─│┴ĮĄĘų╔óąį蹊┐ęčūCīŹ┴╦║¼┴┐×ķ80%Ą─CMSėąų·ė┌į÷╝ė╝{├ūĶFĘų╔óąį, ŪęĘų╔óąįūŅ║├, ┐╔ęį═ŲöÓ▀@ĘN┴╝║├Ą─Ęų╔óąįĖ³ęū┤┘╩╣╝{├ūĶF┼c2, 4-DCPĄ─Įėė|ū„ė├, ╦∙ęį╝{├ūĶF░³Ė▓Ą─CMS▒╚└²į┌Ė▀▀_ę╗Č©│╠Č╚Ż║š╝┐é┴┐80%ĢrĢ■ėąų·ė┌╦«ųą2, 4-DCPĄ─╚ź│².
ĪĪĪĪ×ķ┴╦┼┼│²╝{├ūĶFÅ═║Ž▓─┴Žī”ė┌╬█╚Š╬’╬³ĖĮū„ė├Ą─Ė╔ö_, īŹ“×═¼Ģr£yČ©┴╦2, 4-DCPį┌├ō┬╚ĮĄĮŌ▀^│╠ųąĄ─ųąķg«a╬’╝░ūŅĮK«a╬’2-cpĪó4-cp╝░pĄ─ØŌČ╚.═©▀^łD 7(a)║═7(b)┐╔ęį░l¼F, 2-cp║═4-cpĄ─ØŌČ╚Č╝┤µį┌ų°▓©äė, ļSĘ┤æ¬Ą─▀MąąŽ╚╔²Ė▀║¾ĮĄĄ═, Č°łD 6ųą═¼ę╗Ģrķg2, 4-DCPĄ─ØŌČ╚Ž╚ĮĄĄ═į┘ėą▓┐Ęų╗ž╔², šf├„▀@ā╔ĘN╬’┘|×ķ2, 4-DCPĮĄĮŌ▀^│╠ųąĄ─ųąķg«a╬’, ─▄ē“į┘└^└m▒╗ĮĄĮŌ▐D╗»│╔p.▒ŠīŹ“×░l¼F, 2-cpĄ─ØŌČ╚ŽÓī”4-cpĄ─ØŌČ╚▌^Ė▀, į┌║¾Ų┌Š∙ĮĄĮŌ├ō┬╚ūā×ķūŅĮK«a╬’p.ėąčąŠ┐░l¼F, į┌ģÆ解hŠ│Ž┬║¼¹uĘ╝¤NĄ─▀ĆįŁū„ė├║═Ę┤æ¬╬’Ą─╝¬▓╝╦╣ūįė╔─▄ėąĻP, 2-cp║═4-cpĄ─ś╦£╩╝¬▓╝╦╣ūįė╔─▄(”żG”╚)Ęųäe×ķ-56.8 kJĪżmol-1║═-53.1 kJĪżmol-1.╦∙ęį2, 4-DCPĖ³āAŽ“ė┌╔·│╔╝¬▓╝╦╣ūįė╔─▄Ė³Ą═Ą─2-cp.±R┤Š░▓Ą╚═©▀^ļŖ╗»īWč§╗»čąŠ┐ę▓░l¼F, 2, 4-DCPį┌ļŖ╗»īWč§╗»▀^│╠ųąī”╬╗C╩ŪūŅ╚▌ęū░l╔·ėH║╦Ę┤æ¬Ą─╬╗³c, ī”╬╗┬╚ęūÅ─2, 4-DCP▒ĮŁh╔Ž├ō╚ź, ╦∙ęį2-cpĖ³ęū╔·│╔.Å─łD 7(c)┐╔░l¼F, ūįĘ┤æ¬ķ_╩╝Ģr, ▒Ńėąp╔·│╔, šf├„─┐ś╦╬█╚Š╬’─▄ē“▒╗Fe0ų▒Įė▀ĆįŁĮĄĮŌ╔·│╔p, Ę┤æ¬▀Mąą60 min║¾, pĄ─ØŌČ╚į÷ķL╦┘┬╩ūā┐ņ, ┐╔ęįšf├„┤╦Ģr2-cp║═4-cpš²į┌▒╗ĮĄĮŌ×ķp.
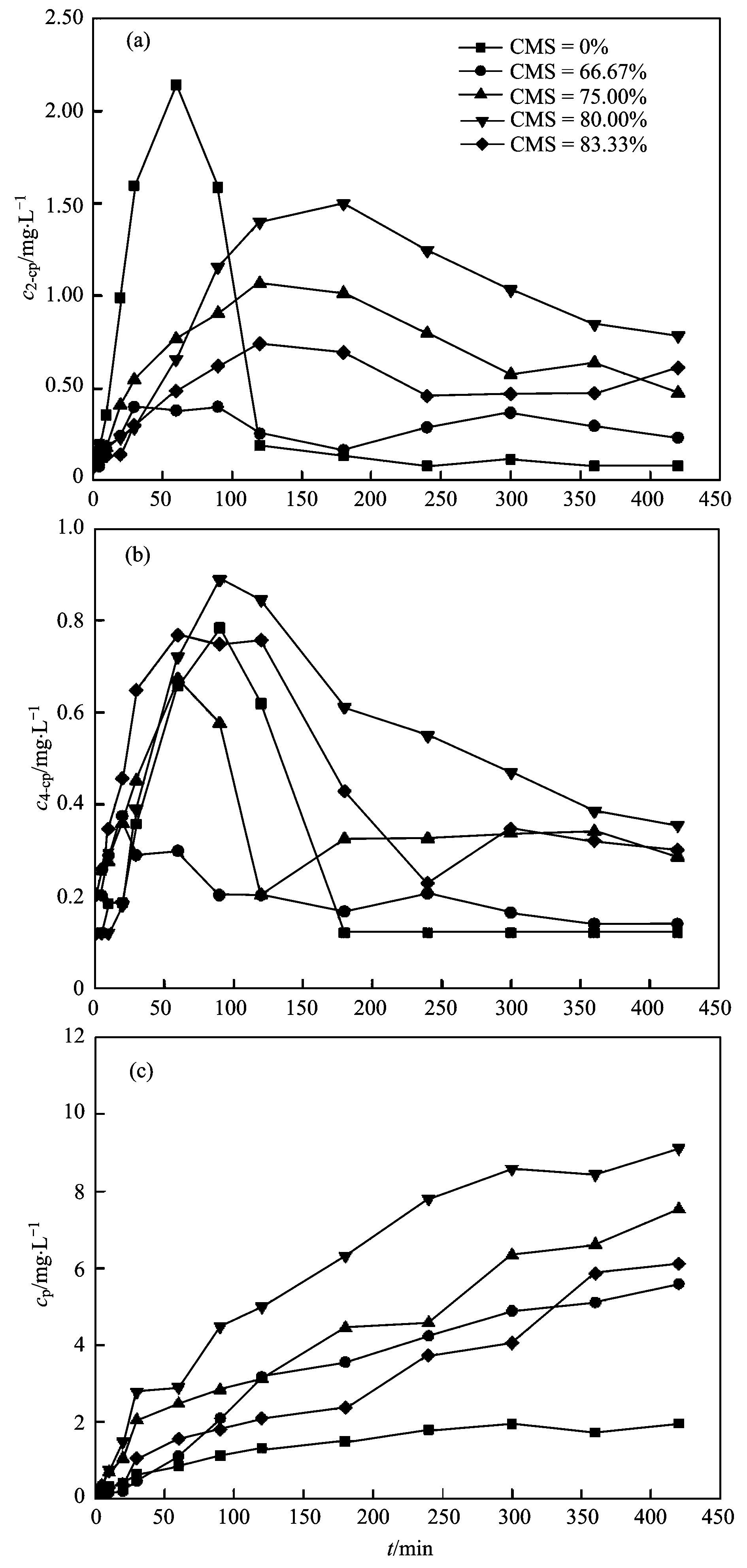
łD 7 2-cpĪó4-cp║═pĄ─ØŌČ╚ūā╗»
ĪĪĪĪ═©▀^łD 6║═łD 7Ą─ī”▒╚┐╔ęį░l¼F, 2, 4-DCP╝╚─▄Ž╚ĮĄĮŌ×ķ2-cp╗“4-cpį┘ĮĄĮŌ×ķp, ę▓─▄ē“ų▒Įė▒╗├ō┬╚ĮĄĮŌ×ķp.ė├┘|┴┐ĘųöĄ×ķ80%Ą─CMSĄ─╝{├ūĶFŠ█║Ž╬’┼e└²ėŗ╦Ń, Ę┤æ¬420 min║¾, 2, 4-DCP║¼┴┐×ķ3.26mgĪżL-1, ┤╦Ģr2-cpĪó4-cp║═p╔·│╔┴┐Ęųäe×ķ0.78Īó0.36║═9.12mgĪżL-1, ┐╔ęį╦Ń│÷2, 4-DCPę╗╣▓▒╗╚ź│²┴╦16.74mgĪżL-1, Ųõųą▒╗ĮĄĮŌ┴╦╣▓14.07mgĪżL-1, ō]░l╝ė╬³ĖĮ╣▓2.67mgĪżL-1, ┤¾▓┐Ęų╬█╚Š╬’▒╗Fe0▀ĆįŁĮĄĮŌ, ĮĄĮŌ┬╩×ķ84%.Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.jianfeilema.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
ĪĪĪĪ3 ĮYšō
ĪĪĪĪ(1) ═©▀^TEM║═XRDĄ─▒Ēš„, ┐╔ęįšf├„CMS░³Ė▓Ą─NZVI▀ĆŠ▀ėą╝{├ūĶFįŁėąĄ─╠žš„ĮYśŗ║═ąį┘|, ė╔ė┌CMSĄ─Ė─ąį░³Ė▓, ┴ŅNZVIĄ─┴ŻÅĮį÷╝ė.═¼Ģr░³Ė▓║¾Ą─NZVIį┌╦«╚▄ę║ųąĄ─Ęų╔óæęĖĪąįą¦╣¹┴╝║├, ░³Ė▓▒╚└²ī”ė┌æęĖĪą¦╣¹ėą▌^┤¾ė░Ēæ, Ą½ęÄ┬╔▓╗╩ŪļSų°░³Ė▓▒╚└²į÷╝ėČ°į÷ÅŖ, «öCMS╦∙š╝▒╚└²×ķ80.00%Ģr, Ęų╔óæęĖĪąįūŅ║├.
ĪĪĪĪ(2) ┼c╬┤░³Ė▓Ą─╝{├ū┴ŃārĶFŽÓ▒╚, ĮøCMS░³Ė▓Ė─ąį║¾Ą─╝{├ūĶFī”ė┌2, 4-DCPĄ─╚ź│²ą¦╣¹ūā║├, Ą½╩Ūą¦╣¹ę▓▓╗╩ŪļS░³Ė▓▒╚└²į÷╝ėČ°į÷ÅŖ, ═¼śėį┌CMS╦∙š╝▒╚└²×ķ80.00%Ģr, ╚ź│²ą¦╣¹ūŅ║├, ▀_ĄĮ┴╦83.69%, ▀@šf├„į┌æęĖĪąį┴╝║├Ą─ŪķørŽ┬, Ęų╔óąįūŅ╝č, ┤╦ĢrĄ─CMS-NZVIŠ▀ėąūŅĖ▀Ą─Ę┤æ¬╗Ņąį, ┼c╬█╚Š╬’Įėė|├µĘeūŅ┤¾, ī”ė┌╬█╚Š╬’Ą─╚ź│²ą¦╣¹ūŅ║├, ─▄ē“┤¾┤¾╠ßĖ▀NZVIĄ─└¹ė├┬╩.
ĪĪĪĪ(3) į┌Ę┤æ¬▀^│╠ųą, 2, 4-DCP╝╚─▄Ž╚├ō╚źę╗éĆ┬╚ļxūėą╬│╔2-cp╗“š▀4-cp, ╚╗║¾į┘└^└m├ō┬╚╔·│╔p, ę▓─▄ē“ų▒Įė├ō╚źā╔éĆ┬╚ļxūėą╬│╔p, ĮĄĮŌ┬╩Ė▀▀_84%, ī”╬█╚Š╬’╚ź│²ą¦╣¹├„’@.ę“┤╦, ▒Š╬─Ą─蹊┐ĮY╣¹ī”ė┌CMS-NZVIį┌╦«ŁhŠ│╬█╚ŠįŁ╬╗ą▐Å═ųąŠ▀ėąę╗Č©ųĖī¦ęŌ┴x, ėąīŹļHæ¬ė├ārųĄ.


