UV/H2O2č§╗»╠Ä└Ē╦«ųą╚ź╬█ä®
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2016-3-15 14:59:14
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪ1 ę²čį
ĪĪĪĪ─┐Ū░Ż¼▒Ē├µ╗Ņąįä®ęčÅVĘ║æ¬ė├ė┌╣żśIĪó▐rśIĪóßt╦ÄĪó╚šė├╗»╣żĄ╚▒ŖČÓŅIė“Ż¼ŽÓæ¬Ą─Ž┤£ņĪó╗»╣żĪó╝Å┐ŚĄ╚ąąśIÅU╦«ųąŠ∙║¼ėą┤¾┴┐▒Ē├µ╗Ņąįä®.┤¾ČÓöĄ▒Ē├µ╗Ņąįä®ļyė┌╔·╬’ĮĄĮŌŻ¼ŪęŲõā╔ėH╠žąį╩╣ų«╚▌ęū╬³ĖĮį┌╬█─Ó╗“│┴Ęe╬’╔Ž.ļSų°╬█╦«ÅS│÷╦«┼┼Ę┼╗“╬█─Ó╠Äų├Ż¼▒Ē├µ╗Ņąįä®▀M╚ļ╦«ŁhŠ│╗“═┴╚└ŁhŠ│Ż¼╬█╚Š═┴╚└║═╦«ŁhŠ│Ż¼Įo╔·æBŁhŠ│║═╚╦¾wĮĪ┐ĄÄ¦üĒØōį┌╬Ż║”.ę“┤╦Ż¼Ė▀ą¦╚ź│²ÅU╦«ųąĄ─▒Ē├µ╗Ņąįä®╩ŪĘŪ│Ż▒žę¬Ą─.
ĪĪĪĪį┌Ė„ŅÉ╬█╦«╠Ä└Ē╝╝ągųąŻ¼Ė▀╝ēč§╗»╝╝ąg(Advanced oxidation processesŻ¼AOPs)─▄Ė▀ą¦╠Ä└Ē║¼▒Ē├µ╗Ņąįä®ÅU╦«Ż¼╩Ū▒╚▌^▀m║ŽĄ─╠Ä└Ē╝╝ąg.│Żė├Ą─AOPs░³└©ūŽ═Ō(UV)Īó│¶č§(O3)Īóļpč§╦«H2O2ĪóUV/H2O2ĪóO3/H2O2ĪóFenton╝╝ągĄ╚.ŲõųąŻ¼╣Ō┤▀╗»č§╗»╝╝ągUV/H2O2└¹ė├UV Ą─╗Ņ╗»ū„ė├Ż¼╝ż░lH2O2«a╔·┴u╗∙ūįė╔╗∙(Īż OH)Ż¼┐╔ęį¤o▀xō±ąįĄž┼cėąÖC╬’Ę┤æ¬Ż¼Ųõī”ėąÖC╬█╚Š╬’Ą─č§╗»─▄┴”▌^å╬¬ÜĄ─UV╗“H2O2╠Ä└Ēėą’@ų°╠ßĖ▀.įō╝╝ągŠ▀ėąĘ┤æ¬Śl╝■£ž║═Īó▓┘ū„║åå╬Īóč§╗»ÅžĄūĪó¤oČ■┤╬╬█╚ŠĄ╚ųTČÓā׳c.īŹ“×╩ę║═ųąįć蹊┐Š∙▒Ē├„Ż¼UV/H2O2╝╝ąg─▄Ė▀ą¦č§╗»│Żė├Ą─ĻÄļxūė▒Ē├µ╗Ņąį䮯¼╚ń╩«Č■═ķ╗∙▒Į╗Ū╦ßŌcĪóEDTAŻ¼Ą½ī”DOCĄ─╚ź│²ą¦┬╩ėąŽ▐Ż¼╚ź│²┬╩į┌0~18%ų«ķg.─┐Ū░│Żė├Ą─╚ź╬█ä®ĘNŅÉĘ▒ČÓĪó│╔ĘųÅ═ļsŻ¼ī”ė┌īŹļH▒Ē├µ╗Ņąįä®ÅU╦«Ą─╠Ä└Ēą¦╣¹ąĶę¬▀Mąąįć“ד×ūC.ę“┤╦Ż¼▒ŠčąŠ┐ßśī”─│ļŖÅSīŹė├Ą─5ĘN╚ź╬█ä®(ų„ę¬│╔Ęų×ķ▒Ē├µ╗Ņąįä®)Ż¼┐╝▓ņUV/H2O2╝╝ągī”Ųõč§╗»ą¦╣¹Ż¼ī”▒╚│§╩╝pHĪóH2O2═Č╝ė┴┐ĪóUV▌ŚššĢrķgĪó▒Ē├µ╗Ņąįä®│§╩╝ØŌČ╚║═ĘNŅÉĄ╚ę“╦žī”č§╗»ą¦╣¹Ą─ė░Ēæ.ę“╦∙ė├5ĘN╚ź╬█䮥─│╔Ęų╬┤ų¬Ż¼╣╩▓╔ė├DOCųĄ▒Ēš„ŲõØŌČ╚Ż¼ė├DOCĄ─╚ź│²┬╩▒Ē╩ŠUV/H2O2╝╝ąg╠Ä└Ēī”╚ź╬█䮥─ĄV╗»─▄┴”Ż¼ęįŲ┌×ķ║¼▒Ē├µ╗Ņąįä®ÅU╦«Ą─╠Ä└Ē╠ß╣®ģó┐╝.
ĪĪĪĪ2 ▓─┴Ž┼cĘĮĘ©
ĪĪĪĪ2.1 īŹ“×▓─┴Ž
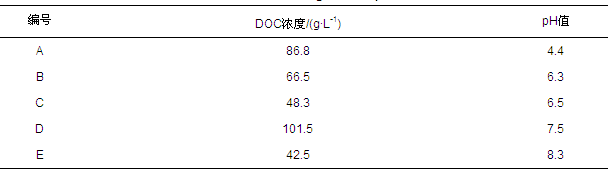
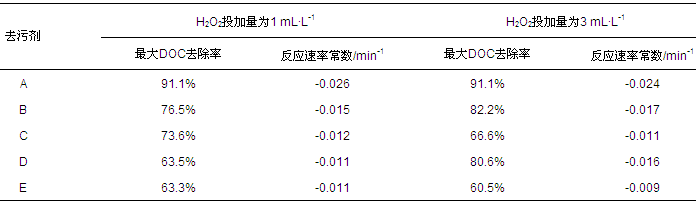
ĪĪĪĪ╚ź╬█ä®╣▓5ĘNŻ¼╚Īūį─│ļŖÅSīŹė├╚ź╬█䮯¼ŠÄ╠¢×ķA~EŻ¼Ė„╚ź╬█ä®įŁę║Ą─DOCØŌČ╚ęŖ▒Ē 1.īŹ“×▓╔ė├ūį┼õ╦«Ż¼ė├ūįüĒ╦«┼õųŲ│╔DOCØŌČ╚×ķ15~100 mg Īż L-1Ą──ŻöMÅU╦«ė├ė┌įć“ׯ¼ŲõųąŻ¼ūįüĒ╦«Ą─DOCØŌČ╚×ķ0.1 mg Īż L-1Ż¼┐╔║÷┬į.ę“╦∙ė├─ŻöMÅU╦«Ą─DOCØŌČ╚┤¾ČÓį┌50 mg Īż L-1ĖĮĮ³Ż¼╣╩īóįōØŌČ╚Ž┬Ė„╚ź╬█ä®╦«╚▄ę║pHųĄ┴ą╚ļ▒Ē 1.ī”5ĘN╚ź╬█ä®▀Mąą┴╦ūŽ═Ō┐╔ęŖ(UV-Vis)╣ŌūVÆ▀├Ķ║═╝t═Ō╣ŌūVĘų╬÷Ż¼į┌▀MąąUV-VisÆ▀├ĶĢrŻ¼ę“╚ź╬█䮥─╬³╣ŌČ╚│¼▀^āxŲ„┴┐│╠Ż¼╣╩ė├╝ā╦«ŽĪßī1000▒Č║¾£yČ©.H2O2(30%)×ķĘų╬÷╝ā.╚▄ę║pHųĄ▓╔ė├1 mol Īż L-1Üõč§╗»Ōc╚▄ę║╗“ŽĪ┴“╦ß▀Mąąš{╣Ø.
ĪĪĪĪ▒Ē1 ╬ÕĘN╚ź╬█ä®įŁę║Ą─DOCØŌČ╚╝░Ųõ╦«╚▄ę║Ą─pHųĄ
ĪĪĪĪ2.2 īŹ“×čbų├
ĪĪĪĪUV/H2O2Ę┤æ¬čbų├×ķUV MAXTM(Trojan╠ß╣®)Ż¼Ę┤æ¬Ų„ų„¾w×ķ2.5 L▓╗õPõō╣▐(ā╚ÅĮ9 cmŻ¼Ė▀40 cm)Ż¼ųąčļĘ┼╚ļę╗ų¦40 WĄ═ē║ūŽ═Ō¤¶(å╬▓©ķL254 nm)Ż¼ūŽ═Ō¤¶═Ōšųėą╩»ėó▓Ż┴¦╠ū╣▄Ż¼╣▐¾wĄ─╔ŽĪóŽ┬Č╦ė╔╣▄Ą└ŽÓ▀BŻ¼▓óė├ęū═■ŲµļŖ┤┼ėŗ┴┐▒├(┴„┴┐×ķ400 mL Īż min-1)═Ųäė╣▐ā╚╦«śė┴„äėŻ¼ęį▒ŻšŽĘ┤æ¬▀^│╠ųą╣▐¾wā╚╦«│õĘų╗ņ║Ž.īóH2O2(═Č╝ė┴┐į┌0.3~3.0 mL Īż L-1)╝ė╚ļūį┼õ╦«ųąŻ¼╗ņ║ŽŠ∙ä“║¾ė├▒├╬³╚ļĘ┤æ¬╣▐ųąŻ¼┤“ķ_ūŽ═Ō¤¶Ż¼ķ_╩╝Ę┤æ¬.Ę┤æ¬ķ_╩╝║¾Ż¼├┐Ė¶10~15 min╚Ī╦«śėę╗┤╬Ż¼ė├ė┌Öz£yŽÓæ¬Ą─╦«┘|ųĖś╦.
ĪĪĪĪ2.3 Ęų╬÷ĘĮĘ©
ĪĪĪĪ╦∙ėą╦«śėŠ∙Įø▀^0.45 ”╠m╬ó┐ū×V─ż▀^×V║¾▀Mąą£yįćĘų╬÷Ż¼DOC▓╔ė├╚š▒ŠŹuĮ“TOC-VWP ┐éėąÖC╠╝Ęų╬÷āx£yČ©.UV-vis╣ŌūVÆ▀├Ķ▓╔ė├ŹuĮ“UV 3100 ą═Ęų╣Ō╣ŌČ╚ėŗŻ¼▓©ķLįOČ©×ķ200~800 nm.╝t═ŌÆ▀├Ķ▓╔ė├ĖĄ└’╚~ūāōQ╝t═Ō╣ŌūVāxspectrum one(PerkinElmerŻ¼ėóć°)Ż¼DTGSÖz£yŲ„Ż¼╣ŌūVĘČć·4000~400 cm-1Ż¼Ęų▒µ┬╩4 cm-1.pHųĄ▓╔ė├pHėŗ(METTLER TOLEDO®)£yČ©.
ĪĪĪĪ2.4 öĄō■Ęų╬÷
ĪĪĪĪĄV╗»┬╩╝┤DOC╚ź│²┬╩(”Ū)ėŗ╦Ń╣½╩Į×ķŻ║”Ū=(C0-Ct)/C0Ī┴100%Ż¼ŲõųąŻ¼C0ĪóCtĘųäe×ķ│§╩╝╝░Ę┤æ¬tĢr┐╠Ą─╦«śėDOCØŌČ╚(mg Īż L-1).
ĪĪĪĪ3 ĮY╣¹┼cėæšō(Results and discussion) 3.1 H2O2│§╩╝═Č╝ė┴┐║═UV▌ŚššĢrķgī”č§╗»ą¦╣¹Ą─ė░Ēæ
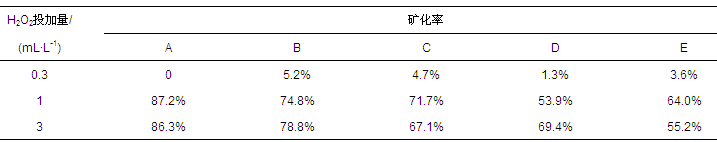
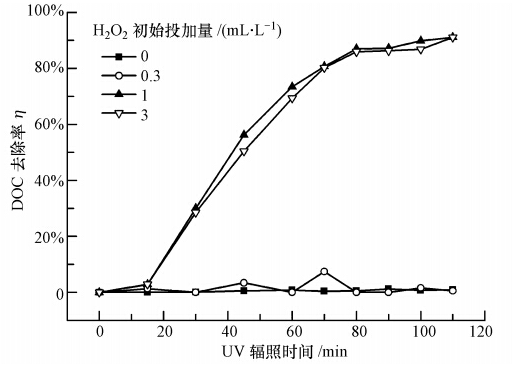
ĪĪĪĪī”▒╚┴╦▓╗═¼H2O2═Č╝ė┴┐(0Īó0.3Īó1Īó3 mL Īż L-1)ī”č§╗»ą¦╣¹Ą─ė░Ēæ.ī”ė┌│§╩╝DOCØŌČ╚×ķ45 mg Īż L-1Ą─╚ź╬█ä®AŻ¼į┌4ĘNH2O2═Č╝ė┴┐Ž┬Ż¼ŲõĄV╗»┬╩ļSUV▌ŚššĢrķgĄ─ūā╗»ŪķøręŖłD 1.ė╔łD┐╔ų¬Ż¼«öH2O2═Č╝ė┴┐×ķ0║═0.3 mL Īż L-1ĢrŻ¼╚ź╬█ä®AĄ─DOCØŌČ╚╗∙▒Š¤oūā╗»Ż¼šf├„āHėąUV▌Śšš▓╗ūŃęįč§╗»╚ź│²╚ź╬█ä®A;«öH2O2═Č╝ė┴┐×ķ1 mL Īż L-1║═3 mL Īż L-1ĢrŻ¼╚ź╬█ä®AĄ─DOCØŌČ╚ļSUV▌ŚššĢrķgĄ─čėķLČ°ųØuĮĄĄ═Ż¼Ūęā╔ĘNŚl╝■Ž┬ī”DOCĄ─╚ź│²Ūķør¤o’@ų°▓Ņ«É.UV▌Śšš30 min║¾Ż¼╦«śėĄ─DOCØŌČ╚ĮĄĄ═30%Ż¼šš╔õ70 min║¾Ż¼DOC╚ź│²┬╩čĖ╦┘╔Ž╔²ĄĮ80%Ż¼ļS║¾ųØu╔Ž╔²ĄĮ90%.Ę┤æ¬90 minū¾ėęŻ¼DOC╚ź│²┬╩Ū·ŠĆ▀M╚ļŲĮ┼_ģ^Ż¼ų«║¾ļSų°UV▌ŚššĢrķgčėķLŻ¼DOC╚ź│²┬╩ūā╗»▓╗├„’@.ī”ė┌Ųõ╦¹4ĘN╚ź╬█䮯¼į┌╚ź╬█ä®│§╩╝DOCØŌČ╚į┌50 mg Īż L-1ĢrŻ¼H2O2═Č╝ė┴┐ī”DOC╚ź│²Ą─ė░ĒæĮY╣¹ęŖ▒Ē 2.ī”ė┌╚ź╬█ä®B║═DŻ¼ļSų°H2O2═Č╝ė┴┐ė╔1 mL Īż L-1╠ßĖ▀ĄĮ3 mL Īż L-1Ż¼UV▌Śšš90 minĢrĄ─DOC╚ź│²┬╩ėą╦∙╔Ž╔²;Č°ī”ė┌╚ź╬█ä®C║═EŻ¼Ūķøräé║├ŽÓĘ┤Ż¼DOC╚ź│²┬╩ļSų°H2O2═Č╝ė┴┐(Å─1 mL Īż L-1╠ßĖ▀ĄĮ3 mL Īż L-1)Ą─į÷╝ėČ°┬įėąĮĄĄ═.▀@╩Ūę“×ķH2O2▓╗āH┐╔╝ė╦┘ Īż OHĄ─╔·│╔Ż¼═¼Ģrėų╩Ū Īż OHĄ─Ō¦£ń䮯¼▀^┴┐Ą─H2O2ī”Ę┤æ¬Ųžōū„ė├(┌wŚŅĄ╚Ż¼2004).ė╔┤╦Ą├│÷Ż¼«ö╚ź╬█䮥─│§╩╝DOCØŌČ╚į┌50 mg Īż L-1ĢrŻ¼H2O2═Č╝ė┴┐┐╔įOČ©×ķ1 mL Īż L-1.
ĪĪĪĪ▒Ē2 H2O2═Č╝ė┴┐ī”5ĘN╚ź╬█䮥V╗»┬╩Ą─ė░Ēæ(Ę┤æ¬Ģrķg90 min)
ĪĪĪĪ┤╦═ŌŻ¼ė╔łD 1┐╔ęįŪÕ│■Ąž┐┤ĄĮŻ¼Ę┤æ¬Ģrķgī”ĄV╗»ą¦╣¹Ą─ė░ĒæĘŪ│Ż├„’@Ż¼«öĘ┤æ¬Ģrķgį┌30 minęįā╚ĢrŻ¼ī”DOCĄ─╚ź│²┬╩į┌5%~40%Ą─ĘČć·.PaganoĄ╚(2008)Ą─蹊┐ę▓░l¼FŻ¼Ę┤æ¬Ģrķg×ķ30 minĢrŻ¼╝┤╩╣▒Ē├µ╗Ņąį䮥─╚ź│²┬╩ęčĮøĮėĮ³100%Ż¼Ą½ī”COD║═DOCĄ─╚ź│²┬╩Š∙▌^Ą═(Ęųäe×ķ0~25%║═0~18%).įōĮY╣¹┼c▒ŠčąŠ┐Ą─ĮY╣¹▒Ż│ųę╗ų┬Ż¼▀Mę╗▓Įšf├„UV▌ŚššĢrķg╩Ūė░ĒæĄV╗»┬╩Ą─ĻPµIę“╦ž.║·┐Ī╔·Ą╚(2007)└¹ė├UV/H2O2č§╗»╠Ä└Ē100 mg Īż L-1Ą─╩«Č■═ķ╗∙▒Į╗Ū╦ßŌc(SDBS)Ż¼░l¼FūŅ╝čĘ┤æ¬Ģrķg×ķ1 hŻ¼Č°▒ŠčąŠ┐ųąūŅ╝čĘ┤æ¬Ģrķg×ķ1.5 h.▀@ą®▓Ņ«É┐╔─▄┼c▒Ē├µ╗Ņąį䮥─ĘNŅÉ╝░│§╩╝ØŌČ╚ėąĻPŻ¼═¼ĢrųĄĄ├ūóęŌĄ─╩Ū▒Š╬─£yįć╩ŪĄV╗»┬╩(╝┤DOC╚ź│²┬╩)Ż¼Č°Ū░š▀£yČ©╩Ū▒Ē├µ╗Ņąį䮥─╚ź│²┬╩.
ĪĪĪĪłD 1 H2O2═Č╝ė┴┐ī”╚ź╬█ä®Ač§╗»ą¦╣¹Ą─ė░Ēæ
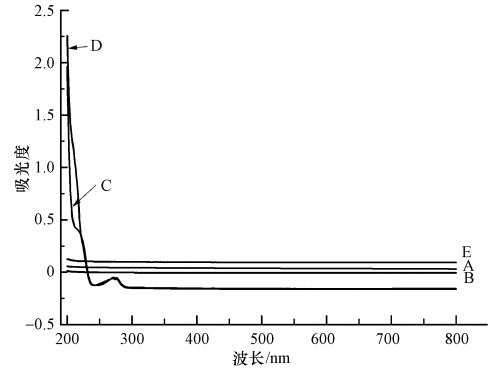
ĪĪĪĪė╔łD 2┐╔ų¬Ż¼╚ź╬█ä®AĪóB║═Eį┌š¹éĆ▓©ķLČ╬Š∙¤o├„’@╬³╩šĘÕŻ¼Č°╚ź╬█ä®C║═Dį┌▓©ķL×ķ270 nm╠Ä│÷¼F╬ó╚§Ą─╠žš„╬³╩šĘÕ.ė╔┤╦┐╔ų¬Ż¼5ĘN╚ź╬█ä®į┌▓©ķL×ķ254 nm╠ÄŠ∙¤o├„’@╬³╩šŻ¼▓╗Ģ■░l╔·ų▒Įė╣ŌĮŌŻ¼įō═Ųšōę▓═©▀^╔Ž╩÷ĮY╣¹Ą├ĄĮ“×ūCŻ¼╝┤į┌▓╗═Č╝ėH2O2╗“H2O2Ą─═Č╝ėØŌČ╚▀^Ą═ĢrŻ¼UV▌Śšš║¾╚ź╬█䮥─ĄV╗»┬╩▓╗Ė▀.ę“┤╦Ż¼▒ŠčąŠ┐Śl╝■Ž┬Ż¼╚ź╬█䮥─č§╗»ĮĄĮŌų„ę¬╩Ū Īż OHĄ─ū„ė├.
ĪĪĪĪłD 2 ╬ÕĘN╚ź╬█䮥─UV-vis╣ŌūVłD
ĪĪĪĪ3.2 ╚ź╬█ä®│§╩╝ØŌČ╚ī”č§╗»ą¦╣¹Ą─ė░Ēæ
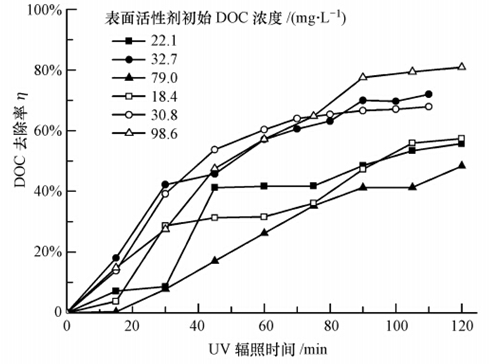
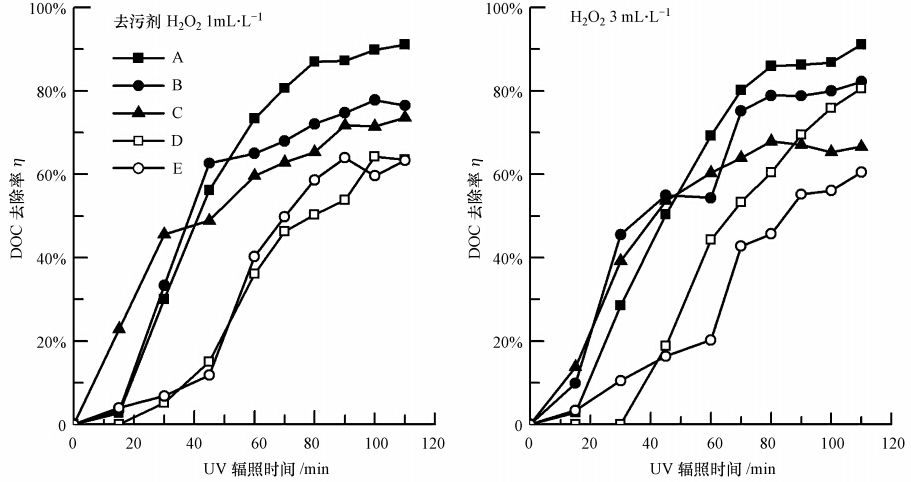
ĪĪĪĪė╔łD 2┐╔ų¬Ż¼╚ź╬█ä®C║═Dį┌270 nm╠Äėą╬ó╚§╬³╩šŻ¼«öŲõØŌČ╚▌^Ė▀ĢrŻ¼┐╔─▄į┌254 nm╠Äę▓ėąę╗Č©╬³╩šŻ¼ė░ĒæūŽ═Ō╣ŌĄ─═Ė╣Ō┬╩╝░Ę┤æ¬╦┘┬╩.╣╩▀x╚Ī╚ź╬█ä®C×ķ└²Ż¼┐╝▓ņŲõ│§╩╝ØŌČ╚ī”č§╗»ą¦╣¹Ą─ė░ĒæŻ¼ĮY╣¹ęŖłD 3.═Č╝ė1 mL Īż L-1Ą─H2O2Ģr(łDųąīŹą─Ę¹╠¢)Ż¼ī”│§╩╝DOCØŌČ╚×ķ32.7 mg Īż L-1╦«śėĄ─ĄV╗»ą¦╣¹ūŅ║├Ż¼DOC╚ź│²┬╩ūŅ┤¾┐╔▀_70%Ż¼Č°│§╩╝DOCØŌČ╚ūŅ┤¾Ą─79 mg Īż L-1╦«śėī”æ¬Ą─DOC╚ź│²┬╩ūŅĄ═Ż¼ūŅ┤¾āH▀_ĄĮ50%.į┌H2O2═Č╝ė┴┐×ķ3 mL Īż L-1Ģr(łDųą┐šą─Ę¹╠¢)Ż¼ī”▌^Ė▀│§╩╝ØŌČ╚(30.8║═98.6 mg Īż L-1)╦«śėĄ─DOC╚ź│²┬╩į┌▌ŚššŪ░80 min¤o’@ų°▓Ņ«ÉŻ¼ų«║¾ī”Ė▀ØŌČ╚╦«śėĄ─DOC╚ź│²┬╩Ė³Ė▀Ż¼ūŅ┤¾╚ź│²┬╩Ęųäe×ķ70%║═80%Ż¼Č°ī”Ą═ØŌČ╚(18.4 mg Īż L-1)╦«śėĄ─DOC╚ź│²┬╩ŽÓī”▌^Ą═Ż¼ūŅ┤¾╚ź│²┬╩×ķ60%.ė╔┤╦┐╔ęŖŻ¼╚ź╬█ä®│§╩╝ØŌČ╚ī”ė┌č§╗»ą¦╣¹ėąę╗Č©ė░ĒæŻ¼į┌H2O2═Č╝ė┴┐ę╗Č©ĢrŻ¼╚ź╬█ä®│§╩╝ØŌČ╚│¼▀^ę╗Č©ĘČć·ĢrŻ¼╠Ä└Ēą¦╣¹ūā▓ŅŻ¼╝┤ę╗Č©Śl╝■Ž┬Ż¼╚ź╬█ä®│§╩╝ØŌČ╚ī”č§╗»ą¦╣¹ėąžōė░Ēæ(Olmez-Hanci et al., 2011).
ĪĪĪĪłD 3 ╚ź╬█ä®C│§╩╝ØŌČ╚ī”č§╗»ą¦╣¹Ą─ė░Ēæ(łDųąīŹą─³cī”æ¬H2O2═Č╝ė┴┐×ķ1 mL Īż L-1Ż¼┐šą─³cī”æ¬H2O2═Č╝ė┴┐×ķ3 mL Īż L-1)
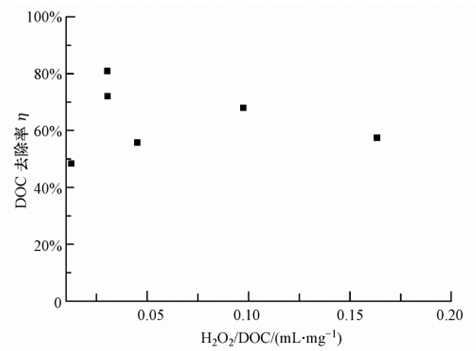
ĪĪĪĪī”▒╚╚ź╬█ä®│§╩╝DOCØŌČ╚ŽÓ╦ŲĢrŻ¼H2O2═Č╝ė┴┐ī”╚ź╬█ä®DOC╚ź│²Ą─ė░Ēæ.«ö╚ź╬█ä®│§╩╝DOCØŌČ╚į┌10~30 mg Īż L-1ĢrŻ¼H2O2═Č╝ė┴┐×ķ1 mL Īż L-1║═3 mL Īż L-1Ą─ā╔ĮMįć“×ĮY╣¹¤o’@ų°▓Ņ«É;«ö╚ź╬█ä®│§╩╝ØŌČ╚į┌80~90 mg Īż L-1ĢrŻ¼Ė▀═Č┴┐H2O2─▄’@ų°┤┘▀Mī”DOCĄ─╚ź│².DOC╚ź│²┬╩ļSH2O2/DOC▒╚ųĄĄ─ūā╗»ęÄ┬╔ęŖłD 4Ż¼┐╔ų¬«öH2O2/DOC▒╚ųĄ×ķ0.03 mL Īż mg-1Ż¼╝┤├┐30 mg DOC═Č╝ė1 mL H2O2ĢrŻ¼ī”æ¬Ą─DOC╚ź│²┬╩ūŅĖ▀Ż¼┐╔▀_70%~80%.ę▓Š═╩ŪšfŻ¼H2O2═Č╝ė┴┐┤µį┌ūŅ▀mĘČć·Ż¼«ö═Č╝ė┴┐▀^┤¾╗“▀^ąĪĢrŻ¼ī”č§╗»▀^│╠╩Ūžōė░Ēæ(┌wŚŅĄ╚Ż¼2004).ė╔łD 4ę▓šf├„Ż¼▓╔ė├H2O2/DOC▒╚ųĄ▒Ē╩Š═Č╝ė┴┐╩Ū▒╚▌^║Ž▀mĄ─ģóöĄ.
ĪĪĪĪłD 4 DOC╚ź│²┬╩ļSH2O2/DOC▒╚ųĄĄ─ūā╗»ęÄ┬╔
ĪĪĪĪ3.3 │§╩╝pHī”č§╗»ą¦╣¹Ą─ė░Ēæ
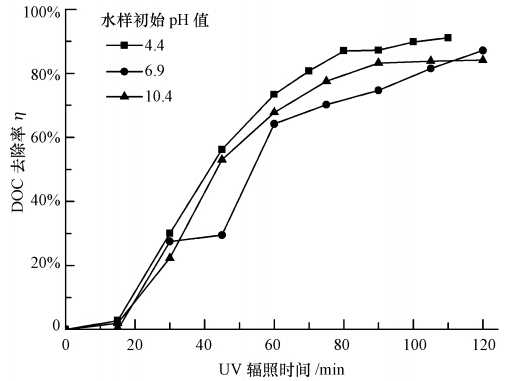
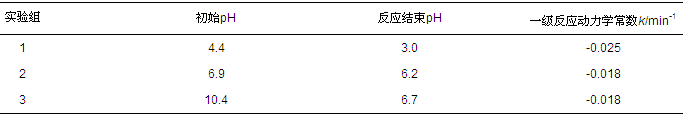
ĪĪĪĪ╚▄ę║│§╩╝pHųĄī”╣Ō┤▀╗»č§╗»▀^│╠ėą▌^┤¾ė░ĒæŻ¼└¹ė├TiO2/UVč§╗»╠Ä└Ē║¼SDBSÅU╦«ĢrŻ¼│§╩╝pHųĄį┌8~10ĢrĄ─č§╗»ą¦╣¹ūŅ║├(═¶čįØMĄ╚Ż¼2002;┌w┴ߥ╚Ż¼2004);Č°į┌UV/H2O2ŽĄĮy╠Ä└Ē100 mg Īż L-1 SDBSÅU╦«ĢrŻ¼ūŅ╝čpHųĄ×ķ6.5(║·┐Ī╔·Ą╚Ż¼2007).▒ŠčąŠ┐ęį╚ź╬█ä®A×ķ└²Ż¼┐╝▓ņ╦«śė│§╩╝pHųĄī”č§╗»ą¦╣¹Ą─ė░Ēæ.╚ź╬█ä®AĄ─╦«╚▄ę║│╔╦ßąįŻ¼į┌DOCØŌČ╚×ķ50 mg Īż L-1ĢrŻ¼ŲõpHųĄ×ķ4.4.ė├NaOHīóŲõ│§╩╝pHųĄĘųäeš{╣Øų┴7║═10ĖĮĮ³Ż¼ī”▒╚3ĘN│§╩╝pHųĄŚl╝■ī”č§╗»ą¦╣¹Ą─ė░Ēæ.ė╔łD 5┐╔ų¬Ż¼3Śl╚ź│²┬╩Ū·ŠĆĄ─┌ģä▌ę╗ų┬Ż¼ī”╬┤š{╣ØpHųĄ(pH=4)╦«śėĄ─č§╗»ą¦╣¹╔įā×ė┌pHš{╣Ø║¾Ą─╦«śė(pHųĄš{╣Øų┴7║═10ū¾ėę)Ż¼Ū░š▀Ą─ūŅ┤¾╚ź│²┬╩▀_ĄĮ90%Ż¼Č°║¾ā╔š▀Ą─ūŅ┤¾╚ź│²┬╩į┌85%ĖĮĮ³.▀@┼cLinĄ╚(1999)Ą─蹊┐ĮY╣¹ę╗ų┬Ż¼įōĘ┤æ¬Ę¹║Žę╗╝ēĘ┤æ¬äė┴”īWĘĮ│╠Ż¼ŽÓæ¬Ą─äė┴”īWģóöĄkęŖ▒Ē 3.ė╔▒Ē 3┐╔ų¬Ż¼│§╩╝pH×ķ4ĢrĄ─ĮĄĮŌ╦┘┬╩ūŅ┐ņŻ¼╦┘┬╩│ŻöĄ×ķ-0.025 min-1Ż¼Č°š{╣ØpHųĄ║¾Ą─ĮĄĮŌ╦┘┬╩¤o’@ų°▓Ņ«É.įōĮY╣¹┼c║·┐Ī╔·Ą╚(2007)Ą─ĮY╣¹ėąą®▓Ņ«ÉŻ¼Ą½SanzĄ╚(2003)└¹ė├UV/H2O2ŽĄĮy╠Ä└Ē2500 mg Īż L-1 SDBSĢrę▓░l¼FpHųĄī”Ę┤æ¬╦┘┬╩Ą─ė░Ēæ▓╗’@ų°Ż¼┼c▒ŠčąŠ┐Ą─ĮY╣¹ę╗ų┬.Ę┤æ¬ĮY╩°║¾Ż¼╚▄ę║Ą─pHųĄŠ∙ėą╦∙ĮĄĄ═(▒Ē 3)Ż¼═Ų£y┐╔─▄╩Ūč§╗»▀^│╠ųą╔·│╔ąĪĘųūė╦ßŅÉ╬’┘|(Karci et al., 2013).╚ń▒Ē 1╦∙╩ŠŻ¼Ųõ╦¹4ĘN╚ź╬█ä®╦«╚▄ę║Ą─pHųĄį┌ųąąįĘČć·(6~8)Ż¼ŪęUV/H2O2ī”Ųõč§╗»ą¦╣¹Š∙▌^║├(▒Ē 2)Ż¼╣╩═Ų╦]UV/H2O2č§╗»╠Ä└Ē▀@ÄūĘN▒Ē├µ╗Ņąįä®ÅU╦«Ģr¤oąĶš{╣ØpHųĄ.
ĪĪĪĪłD 5 ╦«śė│§╩╝pHųĄī”č§╗»ą¦╣¹Ą─ė░Ēæ
ĪĪĪĪ▒Ē3 Ę┤æ¬Ū░║¾╚▄ę║pHųĄūā╗»╝░ŲõĘ┤æ¬äė┴”īWģóöĄ
ĪĪĪĪ3.4 ╚ź╬█ä®ĘNŅÉĄ─ė░Ēæ
ĪĪĪĪī”▒╚UV/H2O2ī”5ĘN╚ź╬█䮥─č§╗»ą¦╣¹Ż¼Ęųäeī”▒╚H2O2═Č╝ė┴┐×ķ1 mL Īż L-1║═3 mL Īż L-1Ą─ā╔ĘN▓┘ū„Śl╝■Ż¼╚ź╬█ä®╦«╚▄ę║Ą─│§╩╝DOCØŌČ╚Š∙×ķ50 mg Īż L-1Ż¼ĮY╣¹ęŖłD 6.ė╔łD┐╔ų¬Ż¼5ĘN╚ź╬█ä®DOCĄ─╚ź│²┬╩Ū·ŠĆ┌ģä▌ę╗ų┬Ż¼╚ź│²┬╩Ū·ŠĆŠ∙│╩Są═.UV/H2O2č§╗»ī”5ĘN╚ź╬█ä®DOCĄ─╚ź│²┬╩║═╚ź│²╦┘┬╩ėą▌^┤¾▓Ņ«É.į┌H2O2═Č╝ė┴┐×ķ1 mL Īż L-1ĢrŻ¼č§╗»ī”╚ź╬█ä®AĄ─DOC╚ź│²┬╩ūŅĖ▀Ż¼▀_ĄĮ91%Ż¼ī”B║═CĄ─DOC╚ź│²┬╩į┌75%ū¾ėęŻ¼Č°ī”D║═EĄ─ūŅ┤¾DOC╚ź│²┬╩āH×ķ63%.įōĘ┤æ¬Ę¹║Žę╗╝ēĘ┤æ¬äė┴”īW─Żą═Ż¼Ųõī”æ¬Ą─Ę┤æ¬äė┴”īW│ŻöĄęŖ▒Ē 4.ė╔▒Ē┐╔ų¬Ż¼╚ź╬█ä®AĄ─č§╗»╦┘┬╩’@ų°Ė▀ė┌Ųõ╦¹4ĘN.ī”▒╚H2O2═Č╝ė┴┐×ķ3 mL Īż L-1┼c1 mL Īż L-1Ą─č§╗»ą¦╣¹┐╔ų¬Ż¼ā╔ĘNŪķørŽ┬ī”╚ź╬█ä®A║═EĄ─DOC╚ź│²┬╩▒Ż│ų▓╗ūāŻ¼3 mL Īż L-1 H2O2ī”╚ź╬█ä®B║═DĄ─DOC╚ź│²┬╩┬įėą╔Ž╔²Ż¼Ą½ī”╚ź╬█ä®CĄ─DOC╚ź│²┬╩ėą╦∙ĮĄĄ═.ė╔┤╦┐╔ų¬Ż¼ļm╚╗UV/H2O2─▄ē“¤o▀xō±ąįĄžč§╗»ėąÖC╬’Ż¼Ą½ī”Š▀ėą▓╗═¼ĘųūėĮYśŗ║═└Ē╗»╠žąįĄ─ėąÖC╬’Ą─č§╗»─▄┴”║═ą¦╣¹ėą╦∙▓╗═¼.ßśī”│╔Ęų▓╗═¼Ą─╚ź╬█䮯¼ąĶę¬▀MąąŅAīŹ“×ęį┤_Č©ūŅ╝čĄ─╣żū„Śl╝■.
ĪĪĪĪłD 6 UV/H2O2ī”▓╗═¼╚ź╬█䮥─č§╗»╚ź│²ą¦╣¹
ĪĪĪĪ▒Ē4 ūŅ┤¾DOC╚ź│²┬╩║═ę╗╝ēĘ┤æ¬äė┴”īWģóöĄī”▒╚
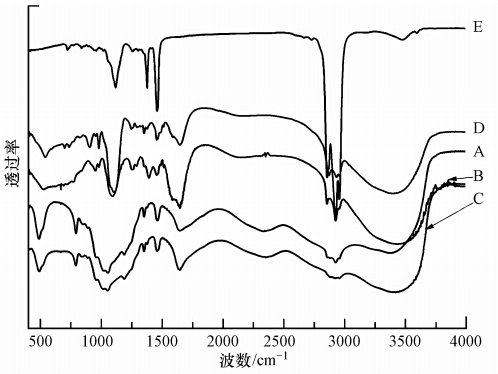
ĪĪĪĪī”5ĘN╚ź╬█ä®▀Mąą┴╦╝t═Ō╣ŌūVĄ─Č©ąįĘų╬÷Ż¼ĮY╣¹ęŖłD 7.ė╔łD┐╔ų¬Ż¼5ĘN╚ź╬█䮥─╝t═Ō╣ŌūVłDĖ„▓╗ŽÓ═¼Ż¼Ą½ėąą®╚ź╬█䮥─ų„ę¬╬³╩šĘÕėąŅÉ╦ŲĄ─╠žš„.└²╚ńŻ¼╚ź╬█ä®A~DŠ∙į┌1645 cm-1║═1458 cm-1╠Äėą▌^ÅŖ╬³╩šŻ¼┤╦╬╗ų├┐╔─▄╩ŪCOO-Ą─╠žš„╬³╩šŻ¼Č°╚ź╬█ä®EĄ─╝t═Ō╣ŌūVųą¤o┤╦╬³╩šĘÕ;╚ź╬█ä®B║═CĘųäeį┌3420 cm-1║═1060 cm-1╠Äėą▌^ÅŖ╬³╩š;╚ź╬█ä®D║═Eį┌1100 cm-1╠Äėą▌^ÅŖ╬³╩š.Ą½ę“╚ź╬█ä®│╔ĘųÅ═ļsŻ¼āHÅ─╝t═ŌūVłD║▄ļy═Ų£y╚źŲõ│╔Ęų.Ą½ĮY║ŽłD 5Ż¼┐╔ęį═ŲöÓ╚ź╬█䮥─│╔Ęų║═ų„ę¬╣┘─▄łFĄ─▓Ņ«Éīóī¦ų┬UV/H2O2č§╗»ą¦╣¹Ą─▓╗═¼.Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.jianfeilema.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
ĪĪĪĪłD 7 ╬ÕĘN╚ź╬█䮥─╝t═Ō╣ŌūVłD
ĪĪĪĪ4 ĮYšō
ĪĪĪĪ▒ŠčąŠ┐ęį─│ļŖÅSīŹė├Ą─5ĘN╚ź╬█ä®×ķ蹊┐ī”Ž¾Ż¼┐╝▓ņ┴╦UV/H2O2ī”5ĘN╚ź╬█䮥─ĄV╗»─▄┴”.蹊┐ĮY╣¹▒Ē├„Ż¼╦∙蹊┐5ĘN╚ź╬█ä®į┌254 nm╠ÄŠ∙¤o╠žš„╬³╩šŻ¼ų▒Įė▓╔ė├UV▌ŚššĮĄĮŌŻ¼ą¦╣¹▌^▓Ņ.«ö─ŻöMÅU╦«ųą╚ź╬█ä®│§╩╝DOCØŌČ╚×ķ50 mg Īż L-1ĢrŻ¼ūŅ╝čH2O2═Č╝ė┴┐×ķ1 mL Īż L-1Ż¼Ę┤æ¬Ģrķg×ķ90 minĢrŻ¼ī”5ĘN╚ź╬█䮥─ĄV╗»┬╩(DOC╚ź│²┬╩)į┌53%~90%ų«ķgŻ¼ĄV╗»ą¦╣¹ę“╚ź╬█ä®ĘNŅÉ▓╗═¼Č°ėą▌^┤¾▓Ņ«É.UV▌ŚššĢrķg╩Ūė░Ēæ╚ź╬█䮥V╗»ą¦╣¹Ą─ųžę¬ę“╦žŻ¼į┌UV▌Śšš90 minā╚Ż¼ĄV╗»┬╩ļSų°UV▌ŚššĢrķgĄ─čėķLČ°į÷┤¾Ż¼╚ź│²┬╩Ū·ŠĆĘ¹║Žę╗╝ēĘ┤æ¬äė┴”īWĘĮ│╠.ÅU╦«│§╩╝pHųĄī”č§╗»ą¦╣¹Ą─ė░Ēæ▓╗’@ų°Ż¼ī”ÅU╦«č§╗»╠Ä└ĒŪ░┐╔▓╗ąĶ꬚{╣ØpHųĄ;H2O2/DOC▒╚ųĄī”č§╗»ą¦╣¹ėąė░ĒæŻ¼ī”╚ź╬█ä®CĄ─ūŅ╝č▒╚└²×ķ0.03 mL Īż mg-1.ė╔┤╦┐╔ų¬Ż¼UV/H2O2╝╝ąg─▄Ė▀ą¦ĄV╗»ÅU╦«ųąĄ─▒Ē├µ╗Ņąįä®│╔ĘųŻ¼H2O2 /DOC▒╚ųĄ║═UV▌ŚššĢrķg╩Ūė░Ēæ╚ź│²ą¦┬╩Ą─ĻPµIę“╦ž.