┤┼ąį║ŻįÕ╦ßĶFĮķ┐ū╠╝╬óŪ“╠Ä└Ē║¼╔ķÅU╦«
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2018-7-1 8:53:16
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪ1 ę²čį(Introduction)
ĪĪĪĪ╔ķ(Arsenic)╩Ūę╗ĘNČŠąįśOÅŖĄ─ŅÉĮī┘į¬╦ž, ╔ķ╝░╔ķĄ─╗»║Ž╬’į┌ūį╚╗ĮńųąÅVĘ║┤µį┌.蹊┐░l¼F, ¤oÖC╔ķĄ─ČŠąį▀h┤¾ė┌ėąÖC╔ķ, Č°╚²ār╔ķČŠąį▒╚╬Õār╔ķÅŖ(Clancy et al., 2013).─┐Ū░, ßśī”╦«¾wųą╔ķ╬█╚ŠĄ─╠Ä└ĒĘĮĘ©░³└©╚ź│²Ęųļx║═č§╗»ĮĄČŠā╔éĆĘĮŽ“, ╬³ĖĮĘ©ę“Š▀ėąŠG╔½┐╔ąąĪó▒ŃĮ▌Ė▀ą¦Ą─╠ž³cČ°▒╗ć°ā╚═ŌīWš▀ĻPūó, ųØu│╔×ķę╗ĘN╚ź│²╔ķĄ─ųžę¬ĘĮĘ©(Mohan et al., 2011), Ą½ķ_░l║═Ė─▀M╬³ĖĮ▓─┴Ž╩Ū─┐Ū░蹊┐Ą─ļy³c.║ŻįÕ╦ßŌc╩Ūę╗ĘN╠ņ╚╗ČÓ╠Ū, ę“Š▀ėą¤oČŠĪó¤o║”Ą─╠ž³cČ°▒╗▌^įńĄžū„×ķ╦Ä╬’ęųųŲä®æ¬ė├ė┌ßt╦ÄŅIė“(Mahdavinia et al., 2014).Į³─ĻüĒ, ║ŻįÕ╦ßŌcę▓▒╗ÅVĘ║æ¬ė├į┌ųžĮī┘╠Ä└ĒŅIė“.└²╚ń, Åł│§▀MĄ╚(2010)ęį║ŻįÕ╦ßŌcū„×ķ░³┬±ä®╣╠Č©╗»░³┬±╗Ņąį╠┐║═ČÓš│ąįč┐µ▀ŚUŠ·▓óæ¬ė├ė┌ųžĮī┘Pb2+Ą─╚ź│², ĮY╣¹░l¼F, ░³┬±ä®Ą─ę²╚ļśO┤¾┐sČ╠┴╦╬³ĖĮŲĮ║ŌĄ─é„┘|▀^│╠, ╠ß╔²┴╦Å═║Ž▓─┴ŽĄ─╬³ĖĮąį─▄║═ĘĆČ©ąį.ParkĄ╚(2010)ł¾Ą└┴╦æ¬ė├Ė„ĘN║ŻįÕ╦ß¹}─²─z╗∙╬³ĖĮä®╚ź│²ųžĮī┘ŃU, ░l¼F║ŻįÕ╦ß¹}─²─z╗∙ī”ųžĮī┘Ą─ĮY║Ž─▄┴”Üwę“ė┌─z╗∙║╦ą─╚▄ę║ųąĄ─³SįŁ─z, ▒Ē├µ╬³ĖĮĄ─ųžĮī┘ļxūė─▄ē“öU╔ó▓ó▀węŲĄĮ─z╗∙ā╚▓┐.蹊┐▀Ć░l¼F, ║ŻįÕ╦ßŌc╚▄ę║┐╔ęį┼c║▄ČÓČ■ār║═╚²ārĻ¢ļxūėĘ┤æ¬ą╬│╔─²─z, ļxūėĮ╗┬ōĘ┤æ¬ų„ę¬═©▀^║ŻįÕ╦ßŌcųą╣┼┴_╠Ū╦ߥ─Ōcļxūė┼cŲõ╦¹Č■ārĪó╚²ārĻ¢ļxūė▀Mąą▓╗┐╔─µĮ╗ōQ(Qi et al., 2012).
ĪĪĪĪ─┐Ū░, └¹ė├ĶFč§╗»╬’╠Ä└Ē║¼╔ķÅU╦«ęčĮøėąę╗Č©Ą─蹊┐╗∙ĄA, ╚ńAndĄ╚(1997)▌^įńĄž╠ß│÷ĶFč§╗»╬’ī”╔ķŠ▀ėąĖ▀ėH║═┴”, ▌^Ė▀Ą─▒Ē├µļŖ║╔║═┤¾▒╚▒Ē├µĘe┘xėĶ┴╦ĶFč§╗»╬’┴╝║├Ą─╬³ĖĮ─▄┴”.║ŻįÕ╦ߊ█║Ž╬’žō▌dĄ─ĶFč§╗»╬’╗∙Å═║Ž╬³ĖĮä®Į³üĒĄ├ĄĮ┴╦▌^ČÓĄ─ĻPūó, æ{ĮĶŲõ▌^Ė▀Ą─╔·╬’ŽÓ╚▌ąįśO┤¾Ąž┐sČ╠┴╦╬³ĖĮ▀^│╠Ą─é„┘|Ģrķg, ░lō]┴╦ĶFč§╗»╬’Ą─ūŅā׹į─▄(Sigdel et al., 2016).└²╚ń, SwainĄ╚(2013)īóFeĪóZrĄ╚ōĮ╚ļįÕ╦ß¹}¾wŽĄųąųŲéõ┴╦FZCAļs╗»▓─┴Žė├ė┌╠Ä└Ē╦«¾wųžĘ·ļxūė;SohfongĄ╚(2009)īó┤┼ąį╬³ĖĮä®┤┼ĶFĄV(Fe3O4)Ņw┴Ż└¹ė├░³┬±Ą─ĘĮ╩ĮōĮ╚ļĄĮ║ŻįÕ╦ßŌ}╚▄─z¾wŽĄųą, ╠ĮŠ┐┴╦▓─┴Žī”ā╔ĘNāræB║¼╔ķÅU╦«Ą─╬³ĖĮą¦╣¹.ŠC╔Ž▓╗ļy░l¼F, ─┐Ū░Ą─蹊┐ČÓ╝»ųąė┌└¹ė├║ŻįÕŌ}▀@ę╗ĘĆČ©─²─z¾wŽĄ, ▓ó═©▀^╚▄─²ĪóĮ■ØnĪó╣▓│┴ĄĒĄ╚ĘĮ╩ĮųŲéõĶFč§╗»╬’Å═║Ž▓─┴Ž.╗∙ė┌┤╦, ▒ŠčąŠ┐ęį║ŻįÕ╦ßŌcū„×ķŪ░“ī▓─┴Ž, └¹ė├║ŻįÕ╦ßŌcęū┼cĻ¢ļxūė░l╔·╣▓ārĮ╗┬ōĄ─╠žąįį┌║ŻįÕ╦ßŌcŪ░“ī¾w▒Ē├µįŁ╬╗žō▌dč§╗»ĶF╝{├ūŅw┴Ż, │╔╣”ųŲéõ║ŻįÕ╦ßĶF─²─ząĪŪ“, ▓óį┌ųŲéõ▀^│╠ųą└¹ė├─“╦žū„×ķųŲ┐ūä®ģó┼cĄĮ╬óŪ“║Ž│╔«öųą, ęįīŹ¼F╝{├ūĶFį┌Ū░“ī▓─┴Ž▒Ē├µĄ─įŁ╬╗║Ž│╔.═¼Ģr, ═©▀^ī”▓─┴ŽĄ─ėąŚl╝■Ė▀£ž┴čĮŌųŲéõ│¼Ēś┤┼ąį║ŻįÕ╦ßĶFĮķ┐ū╠╝╬óŪ“(MAMC), į┌Ū░Ų┌╗∙ĄA╔Ž▌^×ķ╚½├µĄžĘų╬÷Å═║Ž▓─┴Žī”As(ó¾)║═As(ó§)Ą─╬³ĖĮąį─▄.į┌ī”▓─┴Žąį┘|▀Mąą▌^×ķ╝Üų┬Ą─▒Ēš„║¾, ░l¼F║ŻįÕ╦ßŌcŪ░“ī╚▄ę║×ķ╝{├ūĶFč§╗»╬’╠ß╣®┴╦ĘĆČ©Ą─╣Ū╝▄ų¦ĘQ║═ĘĆ╣╠▌d³c, ╝ė┤¾┴╦╝{├ūĶFč§╗»╬’Ņw┴ŻĄ─Ęų╔óąį┼cĘĆČ©ąį.ūŅ║¾, ╠ĮŠ┐═Č╝ė┴┐ĪópHųĄĪóĢrķg║═│§╩╝╬█╚Š╬’ØŌČ╚Ą╚ī”▓─┴Ž╬³ĖĮąį─▄Ą─ė░Ēæ.
ĪĪĪĪ2 īŹ“×┼cĘĮĘ©(Materials and methods)2.1 įćä®┼cāxŲ„
ĪĪĪĪįć䮯║║ŻįÕ╦ßŌcĪó─“╦žĪóŠ┼╦«Ž§╦ßĶFĪóüå╔ķ╦ßŌcĪó╔ķ╦ßŌcĪóÜõč§╗»ŌcĪóØŌ¹}╦ߊ∙×ķĘų╬÷╝ā, ┘Åė┌ć°╦Ä╗»īWįćä®ėąŽ▐╣½╦Š, ╚źļxūė╦«×ķīŹ“×╩ęūįųŲ.
ĪĪĪĪāxŲ„Ż║90-1ą═┤┼┴”öć░ĶŲ„(╔Ž║Ż└ū┤┼)ĪóKQ-100B│¼┬Ģ▓©ŪÕŽ┤Ų„(╔Ž║Ż└ź╔Į╩µ├└āxŲ„ÅS)Īó▒Ńöy╩ĮpHėŗ(╔Ž║Ż└ū┤┼)ĪóļŖĖą±Ņ║ŽĄ╚ļxūė┘|ūVāx(ICP-MS, ├└ć°ńĻĮ░ŻĀ¢─¼)ĪóH1650┼_╩ĮĖ▀╦┘ļxą─ÖC(║■─ŽŽµāxāxŲ„įOéõėąŽ▐╣½╦Š)ĪóCHA-SÜŌįĪ║Ń£žš±╩ÄŽõ(│Żų▌ć°╚AāxŲ„įOéõÅS)ĪóBR-14NTšµ┐šĖ▀£ž╣▄╩ĮĀt(▓®╝{¤ßĀtėąŽ▐╣½╦Š).
ĪĪĪĪ2.2 ▓─┴ŽĄ─ųŲéõ2.2.1 ┤┼ąį║ŻįÕ╦ßĶFĮķ┐ū╠┐Ą─ųŲéõ
ĪĪĪĪ┤┼ąį║ŻįÕ╦ßĶFĮķ┐ū╠╝╬óŪ“(MAMC)Ą─ųŲéõ┴„│╠╚ńłD 1╦∙╩Š.£╩┤_ĘQ╚Ī1.0 g║ŻįÕ╦ßŌcĘ█─®╚▄ĮŌė┌100 mL╚źļxūė╦«ųą, ▓óė┌╦«įĪųą╝ė¤ß╩╣╣╠¾wĘ█─®│õĘų╚▄ĮŌ, ųŲéõ│╔║ŻįÕ╦ßŌc’¢║═╚▄ę║;īó─“╦ž╝ė╚ļĄĮ’¢║═╚▄ę║ųąū„×ķųŲ┐ūä®(ĻÉ├¶Ą╚, 2016), Ųõųą, ─“╦ž║═MAMCĄ─┘|┴┐▒╚×ķ1:1, ┤┼┴”öć░Ķ30 min║¾└õģs┤²ė├(ėøū÷SACŪ░“ī╚▄ę║);£╩┤_ĘQ╚Ī2.02 gŠ┼╦«Ž§╦ßĶF╣╠¾wĘ█─®, ╚▄ĮŌė┌100 mL╚źļxūė╦«ųą, ┼õų├│╔5%Ą─Ž§╦ßĶF╚▄ę║;╩╣ė├ßtė├ūó╔õŲ„(┐ūÅĮ0.34 mm)īó└õģsų┴╩ę£žĄ─SAC╚▄ę║ęŲ╚ļūó╔õŲ„ųą, ▓óęį20Ą╬Īż min-1Ą─╦┘┬╩ųĄ╬╝ė╚ļĄĮŽ§╦ßĶF╚▄ę║ųą(Ę┤æ¬▀^│╠▒Ż│ų▓╗öÓöć░Ķ).«öSAC╚▄ę║ė÷ĄĮŽ§╦ßĶF╚▄ę║ĢrĢ■ą╬│╔╦«Ą╬ĀŅĄ─ąĪŅw┴Ż, ┤┼┴”öć░ĶŲ„ą╬│╔Ą─╦«▓©õ÷£uĢ■░čą╬│╔Ą─ąĪŅw┴Żą²╚ļ╚▄ę║Ąū▓┐, ┤_▒Ż║¾└mą╬│╔Ą─Ņw┴Ż▓╗«a╔·š│▀B¼FŽ¾.Ę┤æ¬═Ļ«ģ║¾īó¤²▒Ł├▄ĘŌ, Ę┼ų├ė┌╩ę£žŽ┬ĻÉ╗»48 h;ĻÉ╗»═Ļ«ģ║¾īóą╬│╔Ą─Ņw┴Ż╬’╚Ī│÷, ▓óė├╚źļxūė╦«┤Ņ┼õ│¼┬Ģ▓©ŪÕŽ┤Ų„ŪÕŽ┤12~15┤╬, ų▒ĄĮŪÕŽ┤ę║ųąÖz£y¤oFe3+ØB│÷;ŪÕŽ┤═Ļ╚½║¾īó▓─┴ŽĘ┼╚ļšµ┐š└õā÷Ė╔į’Ų„ųą└õā÷Ė╔į’48 h, ą╬│╔▓╗║¼╦«ĘųĄ─³S║ų╔½╣╠¾wŅw┴Ż(SA@Fe Particles);īóSA@FeŅw┴ŻĘ┼ų├ė┌╣▄╩ĮĀtųą, į┌═©╚ļĄ¬ÜŌĄ─Śl╝■Ž┬░┤šš1 ĪµĪżmin-1Ą─╔²£ž╦┘Č╚į┌300 Īµ╝ė¤ß3 h, ūį╚╗└õģs║¾ą╬│╔┤┼ąį║ŻįÕ╦ßĶFĮķ┐ū╠╝╬óŪ“(MAMC).
ĪĪĪĪłD 1
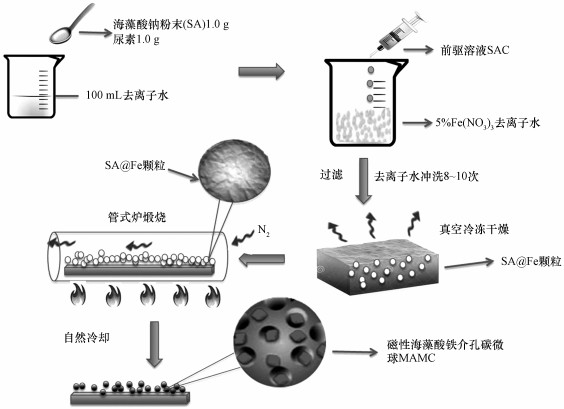
ĪĪĪĪłD 1 MAMCųŲéõ┴„│╠łD
ĪĪĪĪ2.3 ▓─┴ŽĄ─▒Ēš„
ĪĪĪĪMAMCĄ─ą╬æB║══Ō├▓▓╔ė├¤ßł÷░l╔õÆ▀├ĶļŖńR’@╬óńR(QUANTA430, ├└ć°FEI╣½╦Š)ė^£y, X╔õŠĆ╣ŌļŖūė─▄ūV═©▀^Thermo ESCALAB 250XIX╔õŠĆ╣ŌļŖūė─▄ūVāx(├└ć°┘É─¼’w╩└Ā¢┐Ų╝╝)£yČ©, ▓─┴ŽĄ─¤ßĘĆČ©ąįė╔¤ßųžĘų╬÷āx(Q500, ├└ć°TA╣½╦Š)£yČ©, ▓─┴ŽĄ─┤┼ąį£yįćė╔┤┼īW£y┴┐ŽĄĮyMPMS (SQUID) XL(├└ć°Quantum Design╣½╦Š)½@Ą├.
ĪĪĪĪ2.4 ▓─┴Ž╬³ĖĮĪó├ōĖĮīŹ“×
ĪĪĪĪ▓─┴ŽĄ─╬³ĖĮīŹ“×Ęų×ķ═Č╝ė┴┐īŹ“×ĪópHųĄ┐žųŲīŹ“×Īó╬³ĖĮäė┴”īWīŹ“×ĪóĄ╚£ž╬³ĖĮīŹ“×Īó├ōĖĮ║═į┘╔·īŹ“×5éĆ▓┐Ęų, ╬³ĖĮŲĮ║Ō║¾Ą─×Vę║▓╔ė├ļŖĖą±Ņ║ŽĄ╚ļxūė░l╔õ╣ŌūV£yČ©╚▄ę║ųą╩ŻėÓ╔ķĄ─ØŌČ╚.ŽÓ═¼Śl╝■Ž┬įOų├┐š░ūī”ššĮM▀Mąąģó┐╝ī”šš, ┐╝▓ņČÓĘNę“╦žī”╬³ĖĮ┴┐Ą─ė░Ēæ, Ųõųą, ╬³ĖĮųą╚╦╣żÅU╦«Ą─Ė„ĘNØŌČ╚╠▌Č╚Š∙ė╔╔ķ╦ßŌc(Na3AsO3)Īóüå╔ķ╦ß╝{(NaAsO2)┼õųŲĄ──Ėę║ŽĪßīČ°│╔.×ķ┴╦┴┐╗»▓─┴ŽĄ─╬³ĖĮą¦╣¹, MAMCĄ─╬³ĖĮ┴┐║═╚ź│²┬╩░┤ššęįŽ┬╣½╩Į▀Mąąėŗ╦Ń:
ĪĪĪĪ╩Įųą, QR×ķ▓─┴ŽĄ─╚ź│²┬╩;C0×ķ╔ķĄ─│§╩╝ØŌČ╚(mgĪż L-1);C×ķ╠Ä└Ē║¾╚▄ę║ųą╔ķĄ─ØŌČ╚(mgĪż L-1);V×ķ╚▄ę║Ą─¾wĘe(L);M×ķ╬³ĖĮ䮥─ė├┴┐(g);qe×ķŲĮ║ŌĢrĄ─╬³ĖĮ┴┐(mgĪż g-1).
ĪĪĪĪ2.4.1 ═Č╝ė┴┐īŹ“×
ĪĪĪĪ£╩┤_ĘQ╚Īę╗Č©┴┐Ą─MAMC, ░┤šš0.5Īó1Īó2Īó3 gĪż L-1...(ę└┤╦ęÄ┬╔į÷╝ėų┴10 gĪż L-1)Ą─═Č╝ė┴┐╝ė╚ļĄĮ50 mLĄ─ļxą─╣▄ųą, ═∙ļxą─╣▄ųą╝ė╚ļ25 mLØŌČ╚×ķ20 mgĪż L-1Ą─║¼AsÅUę║, Ę┼ų├ė┌ÜŌįĪ║Ń£žš±╩ÄŽõųąš±╩Äų▒ĄĮ╬³ĖĮŲĮ║Ō, 3200 rĪż min-1ļxą─║¾▀^×VĘųļx, ×V│÷ę║ŽĪßī┤²£y.
ĪĪĪĪ2.4.2 pHųĄ┐žųŲīŹ“×
ĪĪĪĪ£╩┤_ĘQ╚Ī0.100 g MAMCśėŲĘė┌ČÓéĆ50 mL╦▄┴Žļxą─╣▄ųą, ░┤ššīŹ“×ę¬Ū¾╩╣ė├0.1 molĪż L-1Ą─NaOH║═HClš{╣ØÅUę║pHųĄ, Ųõųą, ║¼AsÅUę║ØŌČ╚Š∙×ķ150 mgĪż L-1, š{╣ØpHųĄų┴2Īó3Īó4Īó5Īó6Īó7Īó8Īó9Īó10Īó11, │õĘųš±╩Ä24 h║¾3200 rĪż min-1ļxą─, ╩╣ė├ßtė├ūó╔õŲ„░▓čb0.45 ”╠m×V─ż▀^×V, ×V│÷ę║ŽĪßī┤²£y.
ĪĪĪĪ2.4.3 ╬³ĖĮäė┴”īWīŹ“×
ĪĪĪĪ╬³ĖĮäė┴”īWīŹ“×ųą╬³ĖĮ䮥─ė├┴┐čžė├Ū░Ų┌īŹ“×½@Ą├Ą─ūŅ╝čĮY╣¹(═Č╝ė┴┐×ķ1 gĪż L-1, pH=6.5), ╚▄ę║¾wĘe×ķ25 mL, įOų├ČÓéĆŲĮąąśėŲĘ, ═¼ĢrĘ┼ų├ė┌ÜŌįĪ║Ń£žš╩ÄŽõųą, ░┤ššĢrķgą“┴ąŽ╚║¾ķgĖ¶╚Ī│÷As(ó¾)ĪóAs(ó§)śėŲĘ, ▀^×Vļxą─║¾Öz£y╚▄ę║ųą╔ķĄ─ØŌČ╚▓ó▀Mąąäė┴”īWöM║Ž.
ĪĪĪĪ2.4.4 Ą╚£ž╬³ĖĮīŹ“×
ĪĪĪĪĄ╚£ž╬³ĖĮīŹ“×ųą£╩┤_įOų├│§╩╝ÅUę║ØŌČ╚×ķ20Īó50Īó100Īó200Īó300Īó500 mgĪż L-1, Ę┤æ¬Ģrķg║═pH═¼śėčžė├Ū░Ų┌ūŅā×ųĄ(Ę┤æ¬Ģrķg500 min, pH=6.5), ═©▀^Ė─ūā│§╩╝ÅUę║Ą─ØŌČ╚┐╝▓ņ▓─┴ŽĄ─╬³ĖĮąį─▄, ▓óī”╬³ĖĮ▀^│╠▀Mąąā╔ĘNĄ╚£ž─Żą═Ą─öM║Ž.
ĪĪĪĪ2.4.5 ├ōĖĮį┘╔·īŹ“×
ĪĪĪĪīó╬³ĖĮ’¢║═Ą─▓─┴Ž═©▀^═Ō╝ė┤┼ł÷▀Mąą╣╠ę║Ęųļx, īóĘųļx│÷üĒĄ─▓─┴Žė├╚źļxūė╦«│õĘųĮ■Ž┤, └õā÷Ė╔į’║¾, ĘųäeĘ┼╚ļĄĮ0.01Īó0.1Īó1 molĪż L-1Ą─NaOHĮŌ╬³ę║ųą▀Mąą├ōĖĮ║═į┘╔·īŹ“×, ├ōĖĮ║═į┘╔·═Ļ«ģ║¾▀MąąŽÓ═¼Ęųļx▓Į¾E, Ė╔į’║¾╦∙Ą├śėŲĘĘųäe═Č╝ėĄĮ150 mgĪż L-1Ą─║¼As(ó¾)ĪóAs(ó§)ÅUę║ųą┐╝▓ņ├ōĖĮ║¾▓─┴ŽĄ─╬³ĖĮ┴┐.
ĪĪĪĪ3 īŹ“×ĮY╣¹┼cĘų╬÷(Results and analysis)3.1 ▓─┴ŽĄ─▒Ēš„3.1.1 SEMĘų╬÷
ĪĪĪĪ└õł÷░l╔õÆ▀├ĶļŖūė’@╬óńRĄ─ė^▓ņĮY╣¹╚ńłD 2╦∙╩Š, Ųõųą, łD 2AĪóB×ķMAMC╬³ĖĮAsŪ░Ą─ļŖńRłDŲ¼, łD 2CĪóD×ķMAMC╬³ĖĮAs║¾Ą─ļŖńRłDŲ¼.Å─łDųą┐╔ęį┐┤│÷, ▓─┴Ž▒Ē├µėą║▄ČÓ▓╗ęÄätĄ─┐ūŽČ(łD 2BųąĻÄė░ĀŅ), ▓─┴Ž╬³ĖĮŪ░Ęų╔ó│╠Č╚▌^Ė▀;┤╦═Ō, ┐╔ęį▌^×ķ├„’@Ąžė^▓ņĄĮłD 2Bųą▓─┴Ž▒Ē├µžō▌d┴╦┤¾┴┐Ą─Ņw┴ŻĀŅĄ─╬’¾w, ┼õ╠ūEDS─▄ūVį¬╦ž│╔ĘųĘų╬÷▒Ē├„(łD 2E), Ņw┴ŻĀŅ╬’¾w×ķĶFč§╗»╬’Ą─┐╔─▄ąį▌^┤¾, łD 2Bųą▓ÕłDa’@╩Š│÷ĶFč§╗»╬’Ņw┴Ż├▄╝»Ąžžō▌dĄĮ┴╦▓─┴ŽīėķgŖAīė┐ūŽČųą.ŠC╔Ž╦∙╩÷, SEMłDŽ±─▄ē“▌^×ķŪÕ╬·Ąž▒Ē├„č§╗»ĶFŅw┴ŻęčĮø│╔╣”žō▌dĄĮ┴╦║ŻįÕ╦ß¹}Ū░“ī¾wĄ─▒Ē├µ;EDSöĄō■▒Ē├„, ▓─┴ŽĶFį¬╦žĄ─š╝▒╚Ė▀▀_52.32%ęį╔Ž, Ūę▓─┴Ž╬³ĖĮŪ░Ą─As║¼┴┐ĮėĮ³ė┌0, žSĖ╗Ą─ĶFč§╗»╬’×ķęį╔ķ╦ßĖ∙Īóüå╔ķ╦ßĖ∙ą╬╩Į┤µį┌Ą─╔ķļxūė╠ß╣®┴╦▌^×ķžSĖ╗Ą─╬³ĖĮ╬╗³c.┤╦═Ō, ═©▀^łD 2AĪó2B┼cłD 2CĪó2DĄ─ī”▒╚░l¼F, ╬³ĖĮ║¾▓─┴Ž▒Ē├µ▌^×ķ├„’@Ą─┐ūŽČęčĮø▒╗┤¾┴┐ą§ĀŅ╬’(łAŚUĀŅ)Ė▓╔w, ▓─┴ŽĄ─Ęų╔óąįĮĄĄ═, ▓ó░l╔·┴╦▌^×ķ├„’@Ą─łFŠ█¼FŽ¾, ę▓▀Mę╗▓ĮūCīŹ┴╦╬³ĖĮąą×ķĄ─░l╔·.
ĪĪĪĪłD 2
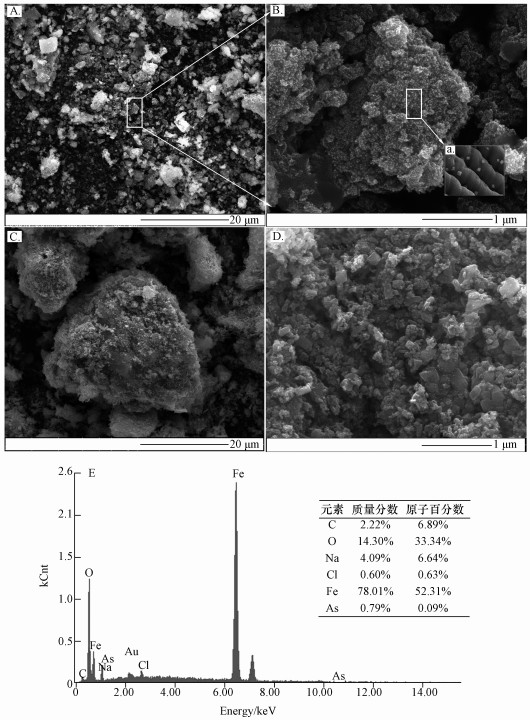
ĪĪĪĪłD 2 MAMC╬³ĖĮŪ░(AĪóBĪóa)Īó║¾(CĪóD)▓╗═¼Ę┼┤¾▒ČöĄļŖńRššŲ¼║═MAMC╬³ĖĮ║¾Ą─EDS─▄ūV╝░į¬╦ž║¼┴┐Ęų▓╝(E)
ĪĪĪĪ3.1.2 BET║═TGAĘų╬÷
ĪĪĪĪ▓─┴ŽĄ─BET║═┐ūÅĮĘų╬÷ĮY╣¹╚ńłD 3a╦∙╩Š, MAMCĄ─▒╚▒Ē├µĘe╝s×ķ62.583 m2Īż g-1, ┐ūÅĮ×ķ12.96 nm, ūC├„▓─┴Žī┘ė┌Įķ┐ū▓─┴ŽĘČ«Ā(┐ūÅĮĮķė┌2 ~50 nmų«ķg).į┌Ą¬ÜŌŁhŠ│Ž┬, ═©▀^Ė─ūāē║┴”▓ó└¹ė├BJHĘ©└LųŲ┴╦▓─┴ŽĄ─╬³ĖĮĪó├ōĖĮŪ·ŠĆ, ┐╔ęį├„’@ė^▓ņĄĮ▀t£■Łhį┌P/P0=0.63╠Ä│÷¼F(Liu et al., 2005).▌^Ė▀ŽÓī”ē║┴”ģ^ė“MAMCø]ėą▒Ē¼F│÷╚╬║╬╬³ĖĮŽ▐ųŲ, šf├„MAMC╩Ūę╗ĘN╬³ĖĮąį─▄ā×įĮĪó┐šŽČ║═▒╚▒Ē├µ▌^×ķ░l▀_Ą─Įķ┐ū▓─┴Ž.¤ßųžĘų╬÷ĘQ╚ĪśėŲĘ3.2 mg, į┌Ą¬ÜŌŁhŠ│Ž┬ęį10 ĪµĪż min-1Ą─╔²£ž╦┘Č╚£yįć┴╦▓─┴ŽĄ─¤ßĘĆČ©ąį.Å─łD 3bųą┐╔ęį┐┤│÷, ▓─┴ŽĄ─┐é┘|┴┐ļSų°£žČ╚Ą─╔²Ė▀ųØuĮĄĄ═, ¤ßĮŌų„ę¬Ęų×ķā╔éĆļAČ╬Ż║į┌0~300 ĪµĄ─£žČ╚Ž┬¤ßĮŌ¼FŽ¾▌^×ķŲĮŠÅ, ¤ßĘĆČ©ąį▌^ÅŖ;Ą½£žČ╚▀_ĄĮ400 Īµęį╔ŽĢr║ŻįÕ╦ßŌc░³┬±Ū░“ī╩▄¤ßĘųĮŌō]░l, įņ│╔▓─┴ŽĄ─¤ßĮŌ╦┘┬╩į÷╝ė, ┘|┴┐ūā╗»▌^×ķ├„’@(Tao et al., 2017).
ĪĪĪĪłD 3
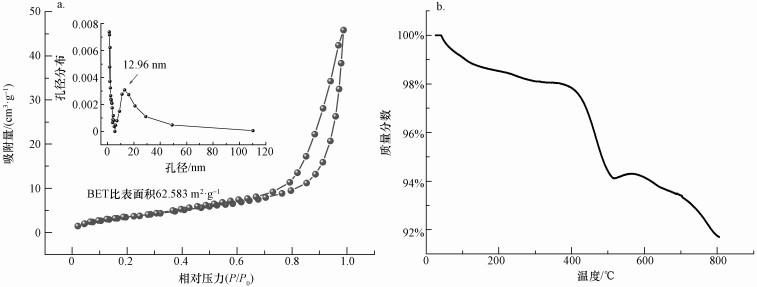
ĪĪĪĪłD 3 MAMC┐ūÅĮĘų▓╝║═BHJŪ·ŠĆ(a)╝░MAMC¤ß╩¦ųž(TGA)Ū·ŠĆ(b)
ĪĪĪĪ3.1.3 XPSĘų╬÷ĮY╣¹
ĪĪĪĪ═©▀^ī”MAMC╬³ĖĮŪ░║¾XPS─▄ūVĪ¬Cį¬╦žĄ─║╦ą─▄ēĄ└ĮY║Ž─▄▀MąąĘųĘÕ╠Ä└Ē, ▓ČūĮĄĮ3éĆ┐╔ęŖĘÕ, īóŲõÜwŅÉ×ķCĪ¬C/CĪ¬H(Ę╝ŽŃūÕ)ĪóCĪ¬O/CĪ¬OĪ¬C(┤╝╩Į┴u╗∙║═├č)ĪóC=O(¶╩╗∙)(Badruddoza et al., 2011).└¹ė├XPSspeak▄ø╝■ī”ššRWAųĄ╝░ĘÕ├µĘe▀MąąĘų╬÷, ░l¼FCĪ¬C/CĪ¬HĪóCĪ¬O/CĪ¬OĪ¬C░l╔·┴╦▌^×ķ├„’@Ą─ĘÕ├µĘeĖ─ūā, įŁę“┼c╔·│╔Ą─Įj║Ž╬’ĖĮĦėąÖC╗∙łFĖĮų°ė┌▓─┴Ž▒Ē├µėąĻP(Š█▒¹Č■┤╝PPG/╝ū§źŅÉŠ█║Ž╬’╝░Ųõ═¼╦ž«Éą╬¾w)(Zheng et al., 2009).═©▀^ī”FeĪóNaĄ─║╦ą─▄ēĄ└ĮY║Ž─▄Ęų╬÷┐╔ęį┐┤│÷, ╬³ĖĮŪ░║¾ā╔ĘNļxūėĄ─ĘÕ├µĘe░l╔·┴╦▒╚▌^├„’@Ą─Ė─ūā, Naį¬╦žüĒį┤ė┌║ŻįÕ╦ßŌc¹}¾wŽĄųą, ▓─┴Žį┌▀MąąĄĮųŲéõĪóĻÉ╗»▀^│╠Ģr, ║ŻįÕ╦ßŌcųąĄ─╣┼┴_╠Ū╦ߥ─Na+┼cFe3+░l╔·▓╗┐╔─µļxūėĮ╗┬ō, Ą½Ę┤æ¬▀^│╠ųąą╬│╔Ą──²─z─żūĶĄK┴╦ę╗▓┐ĘųNa+Ą─╚▄│÷, └õā÷Ė╔į’║═Ė▀£ž¤²ĮY║¾, Na+ę└┼f┤µį┌ė┌MAMCųą▓óš╝ō■▓┐Ęų╬³ĖĮ³c╬╗;Ė▀£ž¤²ĮY▀^│╠╩╣Ą├MAMCą╬│╔┴╦Įķ┐ū┐šŽČ, ę╗Č©│╠Č╚╔ŽöU┤¾┴╦ļxūėĮ╗ōQ═©Ą└, Na+į┌╝ė╚ļĄĮ║¼AsÅUę║ųąĢr, ┤¾▓┐ĘųNa+▀M╚ļĄĮ╚▄ę║¾wŽĄųą▓óŪęßīĘ┼╬³ĖĮ╬╗³c, ī¦ų┬XPS£yįćĮY╣¹ųą╬³ĖĮ║¾▓─┴Ž¾wŽĄ«öųąNa+ĘÕĄ─ūā╗».FeĄ─║╦ą─▄ēĄ└ĘÕ├µĘeį┌╬³ĖĮ║¾£p╔┘Ė─ūāę╗▓┐ĘųÜwę“ė┌╬³ĖĮ▀^│╠ųą╔ķ╦ßĶF(FeAsO4)Ą─╔·│╔║═▓┐ĘųFe3+░l╔·╦«ĮŌ╔·│╔Fe(OH)3Č°▒╗äāļx│÷▓─┴Ž.łD 4eĘ┤ė│┴╦▓─┴Ž╬³ĖĮ║¼╔ķÅUę║Ū░║¾Ą─XPS─▄ūV, łDūV▒Ē├„, MAMCį┌╬³ĖĮŪ░║¾ĘÕ├µĘe░l╔·▌^×ķ├„’@Ą─▓©äė, ▀@ę▓į┘┤╬ėĪūC┴╦MAMC╬³ĖĮAs(ó¾)║═As(ó§)ąą×ķĄ─░l╔·.
ĪĪĪĪłD 4
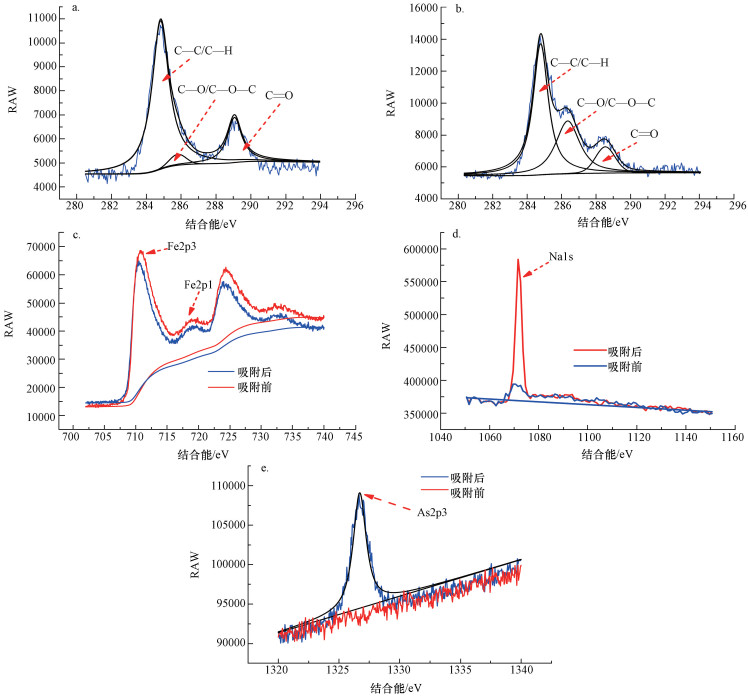
ĪĪĪĪłD 4╠╝(a.╬³ĖĮŪ░, b.╬³ĖĮ║¾)ĪóĶF(c)ĪóŌc(d)Īó╔ķ(e)į¬╦ž║╦ą─▄ēĄ└╬³ĖĮŪ░║¾Ą─XPSłDŽ± Fig. 4 C1s(a.before, b.after), Fe2p(c), Na1s(d) and As2p(e) orbit before and after As adsorption
ĪĪĪĪ3.1.4 ┤┼ąįĘų╬÷
ĪĪĪĪ═©▀^▓─┴ŽĄ─┤┼ąį£yįć└LųŲ┴╦MAMCĄ─┤┼£■╗žŠĆ, į┌▓─┴ŽĄ─╬³ĖĮ▀^│╠ųą╩®╝ė┤┼ł÷ī”╚▄ę║╚▄┘|▀Mąą┤┼Ęųļx(łD 5).▓─┴ŽĄ─’¢║═┤┼╗»ÅŖČ╚×ķ20.86 emuĪż g-1, │CŅB┴”Hc=51.64 Oe, ╬³ĖĮ䮊▀ėą│¼ÅŖĄ─Ēś┤┼ąį(Mahdavinia et al., 2016), ─▄ē“īŹ¼F’¢║═╬³ĖĮ║¾Įķ┘|ų«ķgĄ─Ęųļx(┤┼ł÷Ęųļx£yįć╚ńłD 5ū¾╔ŽĮŪ▓ÕłD╦∙╩Š), ┤┼£■╗žŠĆĄ─Šų▓┐Ę┼┤¾łD(ėęŽ┬ĮŪ▓ÕłD)▒Ē├„▓─┴ŽĄ─┤┼£■║¾¼FŽ¾▒╚▌^╬ó╚§, └Ēšō╔Ž┐╔ęįū„×ķę╗ĘNąį─▄ā×įĮĄ─ė└┤┼▓─┴Ž(│CŅB┴”Hc>30 AĪż m-1)(Li et al., 2012).
ĪĪĪĪłD 5
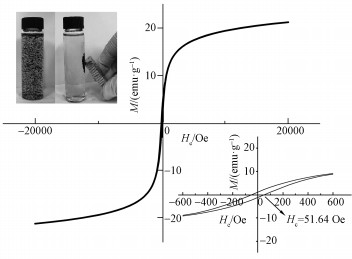
ĪĪĪĪłD 5┤┼£■╗žŠĆĪó┤┼£■Šų▓┐╗žŠĆĘ┼┤¾łD(ėęŽ┬)║═┤┼ł÷╩®╝ėĘųļxĮY╣¹(ū¾╔Ž)
ĪĪĪĪ3.2 As╬³ĖĮīŹ“×Ęų╬÷3.2.1 ═Č╝ė┴┐īŹ“×
ĪĪĪĪÅ─═Č╝ė┴┐īŹ“ץ─ĮY╣¹(łD 6)┐╔ęį┐┤│÷, «ö║¼AsÅUę║ØŌČ╚×ķ50 mgĪż L-1Ģr, ╚▄ę║ųąAsĄ─╚ź│²┬╩ļSų°▓─┴Ž═Č╝ė┴┐Ą─į÷╝ėČ°į÷┤¾, Ū░Ų┌Ą─ą▒┬╩▌^┤¾, ūā╗»┬╩▌^├„’@, Ą½«ö═Č╝ė┴┐┌ģĮ³ė┌1.0 gĪż L-1(╣╠ę║▒╚×ķ1:25)Ģr, ▓─┴Ž░lō]│÷ūį╔ĒĄ─ūŅ┤¾ą¦┬╩, ┤╦ĢrłDųąĘ┤ė││÷üĒĄ─╚ź│²┬╩ę▓ĮėĮ³ūŅā×.
ĪĪĪĪłD 6
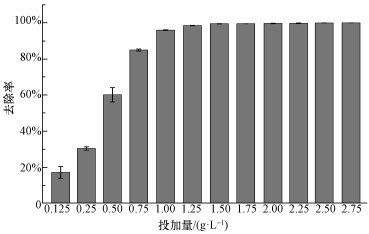
ĪĪĪĪłD 6 MAMC═Č╝ė┴┐īŹ“×
ĪĪĪĪ3.2.2 pHųĄī”╬³ĖĮ▀^│╠Ą─ė░ĒæīŹ“×
ĪĪĪĪĘųäeš{╣Ø║¼╔ķ─ŻöMÅU╦«(ØŌČ╚×ķ250 mgĪż L-1) pHųĄų┴2Īó3Īó4Īó5Īó6Īó7Īó8Īó9Īó10Īó11, ░┤šš1:25Ą─╣╠ę║▒╚£╩┤_ĘQ╚ĪMAMC╝ė╚ļĄĮ100 mLÕFą╬Ų┐ųą, │õĘųš±╩Ä║¾ļxą─▀^×V, Öz£y×V│÷ę║ĮY╣¹, ╠ĮŠ┐pHųĄ┼c▓─┴ŽĄ─╬³ĖĮ┴┐qeĄ─ĻPŽĄ, ĮY╣¹╚ńłD 7╦∙╩Š.▓─┴Žī”As(ó¾)║═As(ó§)Ą─╬³ĖĮ┴┐┼c╚▄ę║Ą─pHųĄĻPŽĄ▌^×ķ├▄Ūą, ī”ė┌║¼As(ó§)Ą─ÅU╦«, ╦ßąįŚl╝■Ė³ėą└¹ė┌▓─┴ŽĄ─╬³ĖĮ, Ą½pHųØu╔²Ė▀Ģr, å╬╬╗▓─┴ŽĄ─╬³ĖĮ┴┐ųØuĮĄĄ═, ▓óį┌pH=9Ģr╝▒äĪŽ┬ĮĄ.▀@╩Ūę“×ķ╬³ĖĮ䮥─▒Ē├µļŖ║╔╠žąį║═╚▄┘|ą╬æB┼c╚▄ę║Ą─pHųĄėąųžę¬Ą─ĻPŽĄ(Stumm et al., 1993), «öpHųĄ▒Ż│ųį┌3.0~6.0Ģr, As(ó§)ų„ę¬ęįH2AsO4-Ą─ą╬╩Į┤µį┌, «öpH×ķ8.0~10.5Ģr, As(ó§)ęįHAsO42-Ą─ą╬╩Į┤µį┌, Č°AsO43-│÷¼Fį┌Ė³Ė▀Ą─pHųĄģ^ķg(Kim et al., 2014), «ö╚▄ę║Įķ┘|ųąĄ─pHųĄ┤¾ė┌MAMCĄ─Ą╚ļŖ³cpHųĄĢr(pHPZC=6.3Ī└0.5), Ģ■╝ė┤¾▓─┴Ž▒Ē├µĄ─žōļŖ║╔┴┐, ▀MČ°╝ė┤¾▓─┴Ž┼cĻÄļxūėĄ─ņoļŖ│Ō┴”, As(ó§)Ą─╬³ĖĮ┴┐┐╔─▄Ģ■├„’@£p╔┘(Kanel et al., 2006).ī”ė┌║¼As(ó¾)Ą─ÅU╦«, ▓─┴Žį┌Ė▀pHųĄ║═Ą═pHĢrĄ─╬³ĖĮą¦╣¹Č╝▓╗├„’@, «ö╚▄ę║Ą─pHųĄ▌^Ą═Ģr, MAMC▒Ē├µĄ─▓┐ĘųĶFč§╗»╬’Ģ■░l╔·╚▄ĮŌ(ė^▓ņĄĮėąĶF¹}╔·│╔, ╚▄ę║¾wŽĄŅü╔½░l╔·Ė─ūā), Å─Č°£p╔┘┴╦╔ķ╦ßĖ∙Ą─╬³ĖĮ╬╗³c.ļSų°╚▄ę║Ą─pHųĄųØu╔²Ė▀, Įī┘č§╗»╬’╔ŽĄ─┼õ¾w╬³ĖĮųØuį÷╝ė, ĘŪļŖļxüå╔ķ╦ß(H3AsO30)Ė³ėą└¹ė┌╬³ĖĮĄĮMAMCĄ─ĘŪļxūė╗»╬╗³c╔Ž(Cumbal et al., 2005).«öpH▀h┤¾ė┌PZC³cĢr, ╝{├ūĶFč§╗»╬’░l╔·╦«ĮŌ, «a╬’Fe(OH)3░l╔·ļŖūė▐DęŲČ°╔·│╔Fe(OH)4-, ╝ė┤¾┴╦ęįĻÄļxūėą╬╩Į┤µį┌Ą─ļxūėķgĄ─ĖéĀÄ╬³ĖĮ┼cÄņü÷│Ō┴”, Å─Č°ęųųŲH2AsO3-ĪóHAsO32-ĪóAsO33-Ą╚╔ķ╦ßĖ∙Ą╚ĻÄļxūėą╬╩ĮĄ─╬³ĖĮ(Zhang et al., 2013).┐╝æ]ĄĮīŹ“ץ─┐╔ąąąį, īóŽ┬ę╗▓ĮīŹ“ץ─╚▄ę║Įķ┘|Ą─pHųĄČ©╬╗ĄĮ6.5.Š▀¾w┬ōŽĄ╬█╦«īÜ╗“ģóęŖhttp://www.jianfeilema.cnĖ³ČÓŽÓĻP╝╝ąg╬─Ön
ĪĪĪĪłD 7
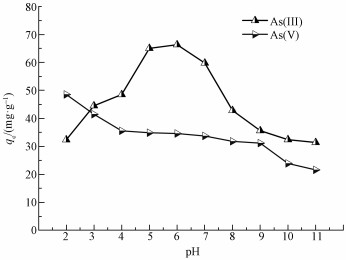
ĪĪĪĪłD 7 pHųĄī”MAMC╬³ĖĮā╔ĘNāræBAsĄ─ė░Ēæ
ĪĪĪĪ3.2.3 ╬³ĖĮäė┴”īWīŹ“×
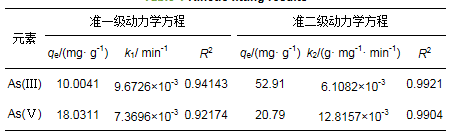
ĪĪĪĪį┌═¼£ž═¼ē║Ž┬, As(ó¾)║═As(ó§)┐š░ū╚▄ę║ØŌČ╚×ķ150 mgĪż L-1, └¹ė├╬³ĖĮäė┴”īWīŹ“×╠ĮŠ┐▓╗═¼Ę┤æ¬ĢrķgŽ┬▓─┴Žī”As(ó¾)ĪóAs(ó§)Ą─╬³ĖĮ┴┐.īŹ“×▓╔ė├Č©Ģr╚ĪśėĘ©, ═©▀^£yČ©╠žČ©ĢrķgČ╬ŲĮ║ŌĢrĄ─ÅUę║ØŌČ╚ėŗ╦Ń│÷╠žČ©Ģr┐╠Ą─╬³ĖĮ┴┐, ė├Origin9▄ø╝■ī”╬³ĖĮ▀^│╠▀MąąŠĆąį£╩ę╗╝ēäė┴”īW(╩Į(1))Īó£╩Č■╝ēäė┴”īW(╩Į(2))öM║Ž(┴_ŌĢĄ╚, 2017), ╦∙Ą├ĮY╣¹╚ńłD 8╦∙╩Š.
ĪĪĪĪłD 8

ĪĪĪĪłD 8 MAMCĄ─╬³ĖĮäė┴”īWīŹ“×ĮY╣¹(a)╝░Ųõäė┴”īWöM║ŽĮY╣¹(b.£╩ę╗╝ēäė┴”īW, c.£╩Č■╝ēäė┴”īW)
ĪĪĪĪ╩Įųą, qe║═qtĘųäe╩Ū╬³ĖĮŲĮ║ŌĢr║═tĢr┐╠Ą─╬³ĖĮ╚▌┴┐(mgĪż g-1), t×ķ╬³ĖĮĢrķg(min), k1×ķ£╩ę╗╝ēäė┴”īW╬³ĖĮ╦┘┬╩│ŻöĄ(min-1), k2×ķ£╩Č■╝ēäė┴”īW╬³ĖĮ│ŻöĄ(gĪż mg-1Īż min-1).
ĪĪĪĪĖ∙ō■╩Į(1)║═╩Į(2)öM║Žln(qe-qt)-t║═t/qt-tĄ─ŠĆąįĻPŽĄ╚ńłD 8b║═8c╦∙╩Š, ĘĮ│╠Ą─┐╔øQŽĄöĄR2╚ń▒Ē 1╦∙╩Š.═©▀^ī”ā╔ĘNāræB║¼╔ķÅU╦«Ą─╬³ĖĮäė┴”īWīŹ“×ĮY╣¹Ą─Ęų╬÷░l¼F, ▓─┴Žī”ė┌As(ó¾)ĪóAs(ó§)Ą─╬³ĖĮ▀^│╠▌^ØMūŃė┌£╩Č■╝ēäė┴”īWĘĮ│╠.į┌│§╩╝ÅUę║ØŌČ╚×ķ150 mgĪż L-1Ģr, £╩Č■╝ēäė┴”īWĘĮ│╠ėŗ╦Ń│÷Ą─└ĒšōūŅ┤¾╬³ĖĮ┴┐(As(ó¾) 52.91 mgĪż g-1ĪóAs(ó§) 20.79 mgĪż g-1)┼c«öŪ░ØŌČ╚īŹ“×ųĄ▌^×ķĮėĮ³, Ūę▓─┴Žį┌500 minĢr╗∙▒Š▀_ĄĮ╬³ĖĮŲĮ║Ō.Å─łD 8aųą▓╗ļy░l¼F, MAMC▀_ĄĮ╬³ĖĮŲĮ║ŌĢrī”ė┌As(ó¾)Ą─╬³ĖĮ┴┐┤¾ė┌ī”As(ó§)Ą─╬³ĖĮ┴┐, ▀@╩Ūę“×ķAs(ó¾)ĪóAs(ó§)į┌ĶFč§╗»╬’╝{├ūŅw┴Żā╚Īó═ŌöU╔óÖCųŲ▓╗═¼įņ│╔(Babaee et al., 2017).
ĪĪ
ĪĪĪĪ3.2.4 Ą╚£ž╬³ĖĮīŹ“×
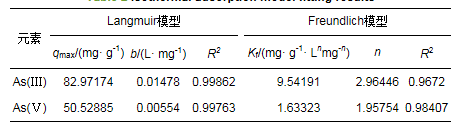
ĪĪĪĪį┌£žČ╚║═ē║┴”ŽÓ═¼Ą─ŪķørŽ┬, ═©▀^Ė─ūā╚▄ę║ųąAs(ó¾)║═As(ó§)Ą─│§╩╝╬’ØŌČ╚, £yČ©Ė„ØŌČ╚Ž┬▓─┴ŽĄ─’¢║═╬³ĖĮ┴┐║═╚▄ę║╬³ĖĮ║¾Ą─ŲĮ║ŌØŌČ╚.īŹ“ץ├ĄĮ▓─┴Žī”As(ó¾)║═As(ó§)Ą─╬³ĖĮĄ╚£žŪ·ŠĆĮY╣¹╚ńłD 9╦∙╩Š, Ą╚£ž─Żą═öM║ŽĮY╣¹╚ń▒Ē 2╦∙╩Š.└¹ė├LangmuirĘĮ│╠(╩Į(3))║═FreundlichĘĮ│╠(╩Į(4))ī”▓─┴ŽĄ─╬³ĖĮĄ╚£žŪ·ŠĆ▀MąąĘŪŠĆąįöM║Ž, įćłD═©▀^╬³ĖĮ─Żą═üĒ╠ĮŠ┐MAMCĄ─╬³ĖĮÖC└Ē.
ĪĪĪĪłD 9
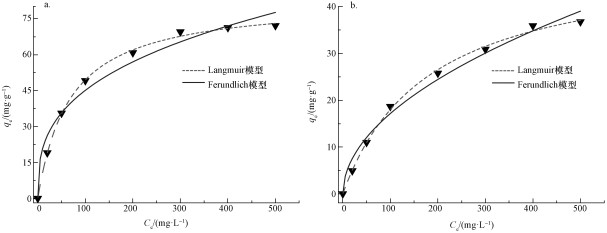
ĪĪĪĪłD 9Ą╚£ž╬³ĖĮ─Żą═öM║ŽĮY╣¹(a.As(ó¾), b.As(ó§))
ĪĪĪĪ
ĪĪĪĪ╩Įųą, qmax×ķ╬³ĖĮ䮥─å╬īė’¢║═ūŅ┤¾╬³ĖĮ┴┐(mgĪż g-1), b×ķLangmuir│ŻöĄ(LĪż mg-1), ▒Ē╩Š╬³ĖĮėH║═┴”, Kf×ķ╬³ĖĮ─▄┴”ŲĮ║Ō│ŻöĄ, n×ķ▓╗Š∙ä“ŽĄöĄ.Freundlich╬³ĖĮĄ╚£žĘĮ│╠╩Ūę╗éĆĮø“×╣½╩Į, ŲõnųĄįĮ┤¾, šf├„╬³ĖĮąį─▄įĮ║├.ę╗░ŃšJ×ķ1/nį┌0.1~0.5ų«ķg, ╚▌ęū╬³ĖĮ;1/n┤¾ė┌2Ģr╬³ĖĮ▌^ļy▀Mąą.
ĪĪĪĪ═©▀^ī”ā╔ĘNĄ╚£ž╬³ĖĮ─Żą═Ą─R2┐╔ęį┼ąöÓ, MAMCī”As(ó¾)ĪóAs(ó§)Ą─╬³ĖĮ▀^│╠Ė³Ę¹║ŽLangmuir─Żą═, ═Ų£yMAMC╩ŪŠ▀ėąėąŽ▐╬³ĖĮ╬╗³cĄ─╬³ĖĮä®, ī”ųžĮī┘As▀Mąąå╬Ęųūėīė╬³ĖĮ(Dada et al., 2012), ▓─┴Žī”As(ó¾)Ą─└ĒšōūŅ┤¾╬³ĖĮ┴┐(82.97174 mgĪż g-1)┤¾ė┌ī”As(ó§)Ą─└ĒšōūŅ┤¾╬³ĖĮ┴┐(50.52885 mgĪż g-1), šf├„▓─┴Žī”As(ó¾)Ą─╬³ĖĮ─▄┴”ā×ė┌As(ó§)(Dixit et al., 2003; Yu et al., 2006).Å─Freundlich─Żą═ųą░l¼F, MAMCī”As(ó¾)Ą─▓╗Š∙ä“ŽĄöĄŠ∙┤¾ė┌1Ūę1/nĮķė┌0.1~0.5ų«ķg, šf├„╬³ĖĮ▀^│╠×ķā×╗▌╬³ĖĮ, ▓─┴ŽĄ─╬³ĖĮąį─▄▌^║├, Č°MAMCī”As(ó§)Ą─1/n┤¾ė┌0.5, ▀Mę╗▓ĮÅŖš{┴╦▓─┴Žī”As(ó¾)Ą─╬³ĖĮ─▄┴”ā×ė┌As(ó§)▀@ę╗ĮYšō.
ĪĪĪĪ3.4.5 ├ōĖĮį┘╔·īŹ“×ĮY╣¹
ĪĪĪĪ├ōĖĮį┘╔·īŹ“×ĮY╣¹╚ńłD 10╦∙╩Š, īŹ“×ųąĘųäe▓╔ė├0.01Īó0.1Īó1 molĪż L-1Ą─NaOHī”╬³ĖĮAs(ó¾)║═As(ó§)Ą─▓─┴Ž▀Mąą├ōĖĮ║═į┘╔·īŹ“×.ĮY╣¹▒Ē├„, ╩╣ė├0.1 molĪż L-1Ą─NaOHū„×ķ▓─┴ŽĄ─├ōĖĮ║═į┘╔·╚▄ę║▌^×ķ└ĒŽļ(Babaee et al., 2017; Pitt et al., 2016), ▓─┴Žį┌▀Mąą4┤╬├ōĖĮ║¾ī”As(ó¾)║═As(ó§)Ą─╚ź│²ą¦╣¹╚į╚╗─▄ē“▒Ż│ųį┌85%║═59%ū¾ėę, ▓─┴Žī”As(ó¾)ĪóAs(ó§)Ą─╚ź│²ą¦╣¹ļSų°├ōĖĮ║═į┘╔·┤╬öĄĄ─į÷╝ėČ°£p╔┘.▀@┐╔─▄╩Ūę“×ķēAąįŁhŠ│Ģ■įņ│╔║ŻįÕ╦ßŌcŪ░“ī║═▓┐Ęų╝{├ūĶFč§╗»╬’Ą─╚▄ĮŌ, Å─Č°įņ│╔▓┐Ęų╬³ĖĮ╬╗³c£p╔┘, įņ│╔▓─┴Ž╬³ĖĮ╚▌┴┐Ą─ĮĄĄ═.
ĪĪĪĪłD 10
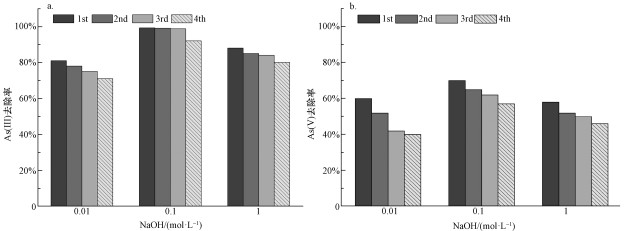
ĪĪĪĪłD 10├ōĖĮ║═į┘╔·īŹ“×ĮY╣¹(a.As(ó¾), b.As(ó§))
ĪĪĪĪ4 ĮYšō(Conclusions)
ĪĪĪĪ1) ▒ŠīŹ“×ęį║ŻįÕ╦ßŌc×ķŪ░“ī─Ż░Õ, ═©▀^ļxūėĮ╗┬ōĘ©│╔╣”║Ž│╔┴╦ČÓ┐ū║ŻįÕ╦ßĶF╬óŪ“, Įø▀^šµ┐š└õā÷║═Ė▀£ž╠╝╗»ųŲéõ┴╦┤┼ąį║ŻįÕ╦ßĶFĮķ┐ū╠╝╬óŪ“(MAMC), ═©▀^ī”MAMCĄ─▒Ēš„Ęų╬÷ūCīŹ┴╦▓─┴Ž╠Ä└Ē╦«¾wAs(ó¾)ĪóAs(ó§)Ą─┐╔ąąąį.
ĪĪĪĪ2) ╬³ĖĮīŹ“×ųąęį╚╦╣ż─ŻöMÅU╦«×ķī”Ž¾╠ĮŠ┐┴╦MAMCī”ā╔ĘNāræB║¼AsÅU╦«Ą─╠Ä└Ē─▄┴”, ▓ó╠Įėæ┴╦pHųĄĪó▓─┴ŽĄ─═Č╝ė┴┐Īó│§╩╝╬█╚Š╬’ØŌČ╚ĪóĮėė|ĢrķgĄ╚ę“╦ž▓─┴Ž╬³ĖĮąį─▄Ą─ė░Ēæ.īŹ“×░l¼F, į┌╠Ä└ĒĄ═ØŌČ╚(10~50 mgĪż L-1)║¼╔ķÅU╦«Ģr, ▓─┴ŽĄ─ūŅā×═Č╝ė┴┐×ķ1 gĪż L-1, ▓─┴Ž╬³ĖĮ▀^│╠╩▄pHĄ─ė░Ēæ▌^┤¾, į┌╠Ä└ĒAs(ó¾)ÅU╦«Ģr, ╚▄ę║▌^Ė▀pHųĄ(pH>9)║═▌^Ą═pHųĄ(pH < 6)Š∙▓╗└¹ė┌╬³ĖĮ▀^│╠Ą─▀Mąą, į┌╠Ä└ĒAs(ó§)ÅU╦«Ģr, ╦ßąįŚl╝■Ė³ėą└¹ė┌╬³ĖĮĘ┤æ¬Ą─▀Mąą.╬³ĖĮäė┴”īWīŹ“×░l¼F, ▓─┴ŽĄ─╬³ĖĮ▀^│╠Ė³ØMūŃė┌£╩Č■╝ē╬³ĖĮäė┴”īWĘĮ│╠, ▓─┴Žī”ųžĮī┘AsĄ─╬³ĖĮ▀^│╠▌^ĘĆČ©Ūęį┌500 minĢr╗∙▒Š▀_ĄĮ╬³ĖĮŲĮ║Ō.Ą╚£ž╬³ĖĮīŹ“×ĮY╣¹ųąR2ųĄ▒Ē├„, LangmuirĘĮ│╠─▄ē“Ė³║├ĄžØMūŃ▓─┴Žī”As(ó¾)║═As(ó§)Ą─╬³ĖĮ▀^│╠, ▓─┴Žī”AsĄ─╬³ĖĮ▀^│╠ØMūŃā×╗▌╬³ĖĮŚl╝■, ▓─┴Žī”As(ó¾)Ą─╬³ĖĮ─▄┴”ā×ė┌As(ó§), ▓─┴Žī”ā╔ĘNāræBĄ─AsļxūėĄ─╬³ĖĮ×ķ╬’└Ē╬³ĖĮ║═╗»īW╬³ĖĮ═¼Ģr▀Mąą.
ĪĪĪĪ3) MAMCĄ─į┘╔·īŹ“×ūCīŹ┴╦▓─┴Žį┘╔·Ą─┐╔ąąąį, īŹ“×░l¼F, 0.1 molĪż L-1NaOHĄ─į┘╔·ąį─▄║═├ōĖĮąį─▄▌^║├, Ė▀ØŌČ╚Ą─į┘╔·║═├ōĖĮĮķ┘|▓ó▓╗─▄╠ß╔²į┘╔·▓─┴Ž╬³ĖĮ┴┐, ▓─┴Žī”ė┌As(ó¾)Ą─├ōĖĮąį─▄ā×ė┌As(ó§), ▓─┴ŽĮø▀^4┤╬├ōĖĮ║═į┘╔·MAMCī”ė┌As(ó¾)║═As(ó§)╚į╚╗─▄ē“▒Ż│ų90%║═60%ęį╔ŽĄ─╬³ĖĮ─▄┴”, ▀@ę▓šf├„┴╦MAMC─▄ē“īŹ¼FČ■┤╬└¹ė├║═裣hį┘╔·, ─▄ē“▀_ĄĮŠG╔½ŁhŠ│╣”─▄▓─┴ŽĄ─ę¬Ū¾.(üĒį┤Ż║ŁhŠ│┐ŲīWīWł¾ ū„š▀Ż║ĮŁš┐╚ń)