Ęą╩»╬³ĖĮÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─ąį─▄
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2017-2-27 14:00:47
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪļSų°¼F┤·╗»╣żąąśIĄ─░lš╣Ż¼║¼ėąī”Ž§╗∙▒ĮĘėĄ─ėąÖCÅU╦«┤¾┴┐┼┼Ę┼; ė╔ė┌ī”Ž§╗∙▒ĮĘėŠ▀ėą┴╝║├Ą─╔·╗»ĘĆČ©ąįŻ¼▓╗ęūĮĄĮŌŻ¼Å─Č°įņ│╔┴╦ć└ųžĄ─╦«¾wŁhŠ│╬█╚Š. ─┐Ū░Ż¼Å─ÅU╦«ųą╚ź│²ī”Ž§╗∙▒ĮĘėĄ─ĘĮĘ©ų„ę¬ėą╬ó╔·╬’ĮĄĮŌĘ©Īó ▌═╚ĪĘ©Īó ╬³ĖĮĘ©ęį╝░╣Ō┤▀╗»č§╗»Ę©[1, 2, 3, 4, 5]. ŲõųąŻ¼╬³ĖĮĘ©ė╔ė┌▓╗ę²╚ļą┬Ą─╬█╚Š╬’Ż¼─▄║─▌^Ą═Ż¼Ūę─▄ē“Å─ÅU╦«ųąĘųļx╬█╚Š╬’╝ėęįųžą┬└¹ė├Ż¼éõ╩▄ÅVĘ║ĻPūó. ╠ņ╚╗Ęą╩»¬Ü╠žĄ─╦─├µ¾wĮYśŗĪó Š▐┤¾Ą─▒╚▒Ē├µĘeĪó ĘĆČ©Ą─╗»īWąį┘|Ż¼╩╣Ą├ŲõŠ▀ėą▌^║├Ą─╬³ĖĮąį─▄Ż¼┤╦═ŌŻ¼Ęą╩»ųąĄ─Ļ¢ļxūė╩╣ŲõŠ▀ėąņoļŖ╬³ę²┴”Ż¼ī”śOąį║═ęūśO╗»ĘųūėĄ─╬³ĖĮū„ė├▌^ÅŖ[6]. ßśī”ÅU╦«ųąĄ─ī”Ž§╗∙▒ĮĘėŻ¼ė╔ė┌Ī¬C6H5╗∙łF╩Ū┐╔śO╗»╗∙łFŻ¼╩╣Ą├Ęą╩»─▄ē“▒╗æ¬ė├ė┌ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╚ź│²[7, 8, 9, 10]. ╚╗Č°Ż¼╠ņ╚╗Ęą╩»▒Ē├µ╣Ķč§ĮYśŗ╦∙Š▀ėąĄ─ėH╦«ąįŻ¼╩╣Ą├Ųõ╬³ĖĮėąÖC╬’Ą─śOŽ▐ąį─▄▓╗└ĒŽļŻ¼ę“┤╦Ż¼×ķ┴╦╠ßĖ▀Ęą╩»╚ź│²ÅU╦«ųąėąÖC╬█╚Š╬’Ą──▄┴”Ż¼│Żį┌╩╣ė├Ū░ī”Ųõ▀MąąĖ─ąį╠Ä└Ē[11, 12]Ż¼└²╚ńŻ║╠ņ╚╗Ęą╩»Įø┘|┴┐ØŌČ╚×ķ5 g ĪżL-1╩«┴∙═ķ╗∙╚²╝ū╗∙õÕ╗»õ@╚▄ę║Į■┼▌║¾Ż¼─▄ē“╠ßĖ▀ī”ĘėŅÉÅU╦«Ą─╚ź│²ą¦╣¹[13, 14].
ĪĪĪĪ▒ŠčąŠ┐▓╔ė├HDTMAī”╠ņ╚╗Ęą╩»▀MąąĖ─ąįŻ¼╠ĮėæĖ─ąįŚl╝■ī”Ęą╩»╬³ĖĮ─▄┴”Ą─ė░ĒæŻ¼┐╝▓ņĖ─ąįĘą╩»╬³ĖĮÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─ąį─▄Ż¼į┌┤╦╗∙ĄA╔ŽŻ¼čąŠ┐╬³ĖĮ▀^│╠ųąĄ─äė┴”īW║═╬³ĖĮĄ╚£žŠĆ╠žš„.
ĪĪĪĪ1 ▓─┴Ž┼cĘĮĘ©
ĪĪĪĪ1.1 īŹ“×▓─┴Ž
ĪĪĪĪīŹ“×╦∙ė├╠ņ╚╗Ęą╩»┘Åūį╔Ž║Żć°╦Ä╝»łF╗»īWįćä®ėąŽ▐╣½╦ŠŻ¼20-40─┐Ż¼ĮøīŹ“×£yĄ├ŲõĻ¢ļxūėĮ╗ōQ┴┐×ķ0.36 mol Īżkg-1Ż¼╠ņ╚╗Ęą╩»śėŲĘĮøš¶s╦«Ų»Ž┤║¾Ż¼į┌105ĪµŽ┬║µĖ╔éõė├; ╩«┴∙═ķ╗∙╚²╝ū╗∙õÕ╗»õ@┘Åūį│╔Č╝╩ą┐Ų²ł╗»╣żįćä®ÅS(ŽÓī”Ęųūė┘|┴┐Ż║364.45 g Īżmol-1)Ż¼Ęų╬÷╝ā.
ĪĪĪĪ1.2 īŹ“×ĘĮĘ©
ĪĪĪĪ1.2.1 HDTMAĖ─ąįĘą╩»Ą─ųŲéõ
ĪĪĪĪ╗∙ė┌¼FėąčąŠ┐[13, 14]Ż¼┼õųŲ┘|┴┐ØŌČ╚×ķ0.8%Īó 1.0%Īó 1.2%Īó 1.4%Īó 1.6%Ą─▓╗═¼pHųĄĄ─HDTMA╚▄ę║Ż¼īó╠ņ╚╗Ęą╩»Ęųäe┼c┼õųŲ║├Ą─HDTMA╚▄ę║ęį1 Ī├10(┘|┴┐¾wĘe▒╚Ż¼┘|┴┐å╬╬╗gŻ¼¾wĘeå╬╬╗mL)╗ņ║ŽŻ¼ė┌25ĪµŻ¼120 r Īżmin-1š±╩Ä6 h║¾Ż¼3 000 r Īżmin-1ļxą─20 min╩š╝»│┴ĄĒ╬’Ż¼▓╔ė├š¶s╦«ø_Ž┤Ż¼ŽÓ═¼Śl╝■Ž┬ļxą─║═ø_Ž┤4-5┤╬Ż¼ų▒ĄĮø_Ž┤║¾Ą─╔ŽŪÕę║ųąÖz£y▓╗ĄĮHDTMAŻ¼ūŅ║¾╩š╝»│┴ĄĒ╬’ė┌100ĪµŽ┬Ė╔į’12 hŻ¼½@Ą├Ė─ąįĘą╩».
ĪĪĪĪ1.2.2 ╬³ĖĮīŹ“×
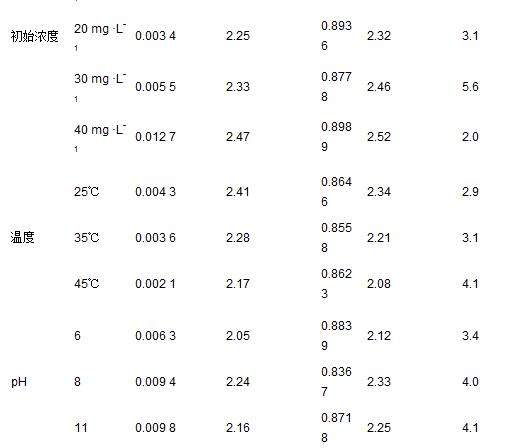
ĪĪĪĪ£╩┤_ĘQ╚Īę╗Č©┴┐Ą─Ė─ąįĘą╩»╠Ē╝ėų┴1.0 LØŌČ╚×ķ20 mg ĪżL-1Ą─ī”Ž§╗∙▒ĮĘė╚▄ę║ųąŻ¼│Ż£žŚl╝■Ž┬120 r Īżmin-1öć░Ķ2 h║¾Ż¼ņo│┴30 minŻ¼╚Ī╔ŽŪÕę║Įø0.45 ”╠m×V─ż▀^×V║¾Ż¼£yČ©ŲõųąĄ─ī”Ž§╗∙▒ĮĘėØŌČ╚. ÅU╦«pH▓╔ė├0.1 mol ĪżL-1Ą─HCl╗“NaOH╚▄ę║š{╣Ø. ░┤Ž┬┴ą╣½╩Įėŗ╦Ńī”Ž§╗∙▒ĮĘė╬³ĖĮ┴┐qe║═╚ź│²┬╩”ŪŻ║
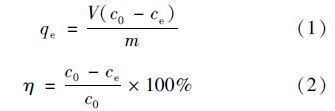
ĪĪĪĪ╩ĮųąŻ¼c0║═ceĘųäe×ķÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─│§╩╝ØŌČ╚║═╬³ĖĮŲĮ║ŌĢrĄ─ØŌČ╚Ż¼mg ĪżL-1; m×ķĖ─ąįĘą╩»═Č╝ė┴┐Ż¼g; V×ķÅU╦«śė╚▌ĘeŻ¼L.
ĪĪĪĪ1.2.3 Öz£yĘĮĘ©
ĪĪĪĪīŹ“×▀^│╠ųąŻ¼ī”Ž§╗∙▒ĮĘė╚▄ę║Ą─ØŌČ╚▓╔ė├ūŽ═ŌĘų╣Ō╣ŌČ╚Ę©£yČ©Ż¼ūŅ┤¾╬³╩š▓©ķL×ķ317 nm; ÅU╦«pHųĄ▓╔ė├pHėŗ(pHS-3C)Öz£y; ÅU╦«ųąHDTMAØŌČ╚▓╔ė├Ęų╣Ō╣ŌČ╚Ę©£yČ©Ż¼ūŅ┤¾╬³╩š▓©ķL×ķ470 nm; Ė─ąįĘą╩»Ą─Ļ¢ļxūėĮ╗ōQ┴┐▓╔ė├ęę╦ßõ@Ę©£yČ©.
ĪĪĪĪ1.3 ╬³ĖĮäė┴”īW
ĪĪĪĪ╗∙ė┌╬³ĖĮīŹ“ץ├ĄĮĄ─ī”Ž§╗∙▒ĮĘėĄ─ūŅ╝č╬³ĖĮŚl╝■Ż¼▒Ż│ųĖ─ąįĘą╩»═Č╝ė┴┐Īó ÅU╦«pHųĄĄ╚▓╗ūāŻ¼═©▀^Öz£y╬³ĖĮ▀^│╠ųąĖ─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘė╬³ĖĮ┴┐Ą─ūā╗»Ż¼┐╝▓ņī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮäė┴”īW╠žš„. ę╗╝ē╦┘┬╩ĘĮ│╠║═Č■╝ē╦┘┬╩ĘĮ│╠Ą─Ēææ¬─┐ś╦Š∙╩Ū├Ķ╩÷╬³ĖĮäė┴”īW▀^│╠Ż¼Ęųäe╚ńĘĮ│╠(3)║═(4)╦∙╩ŠŻ║
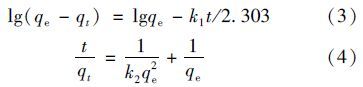
ĪĪĪĪ╩ĮųąŻ¼qt×ķtĢr┐╠Ęą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮ┴┐Ż¼mg Īżg-1; k1×ķę╗╝ē╦┘┬╩ĘĮ│╠╦┘┬╩│ŻöĄŻ¼min-1; k2╩ŪČ■╝ē╦┘┬╩ĘĮ│╠╦┘┬╩│ŻöĄŻ¼g Īż(mg Īżmin)-1; t×ķĘ┤æ¬Ģrķg(min).
ĪĪĪĪ1.4 ╬³ĖĮĄ╚£žŠĆ
ĪĪĪĪę╗░ŃŪķørŽ┬Ż¼╚▄┘|Å─╚▄ę║ųą▐DęŲĄĮ╬³ĖĮä®╔Ž▀@ę╗äėæB▀^│╠╚ĪøQė┌╣╠-ę║ŽÓų«ķgĄ─╬³ĖĮŲĮ║ŌŻ¼╬³ĖĮĄ╚£žŠĆš²╩Ūė├üĒ├Ķ╩÷╚▄┘|Ą─▀@ę╗╬³ĖĮ▀^│╠Ą─Ż¼ūŅ×ķĄõą═Ą─╩ŪFreundlichĪó LangmuirĄ╚£žŠĆĘĮ│╠[15, 16]. ╗∙ė┌╬³ĖĮīŹ“ץ├ĄĮĄ─ī”Ž§╗∙▒ĮĘėĄ─ūŅ╝č╬³ĖĮŚl╝■Ż¼▒Ż│ųĖ─ąįĘą╩»═Č╝ė┴┐Īó ÅU╦«pHųĄĄ╚▓╗ūāŻ¼į┌▓╗═¼īŹ“×£žČ╚Śl╝■Ž┬Ż¼═©▀^Öz£y╬³ĖĮŲĮ║ŌĀŅæBĢrĖ─ąįĘą╩»Ą─ŲĮ║Ō╬³ĖĮ┴┐┼cÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╩ŻėÓ┴┐ų«ķgĄ─ĻPŽĄŻ¼┐╝▓ņĖ─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮĄ╚£žŠĆ╠žš„. FreundlichĪó LangmuirĄ╚£žŠĆĘųäe╚ńĘĮ│╠(5)║═(6)╦∙╩ŠŻ║
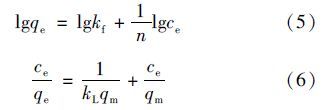
ĪĪĪĪ╩ĮųąŻ¼kf║═n×ķFreundlich│ŻöĄ; kL×ķLangmuir│ŻöĄ; qm×ķūŅ┤¾╬³ĖĮ┴┐Ż¼mg Īżg-1.
ĪĪĪĪ2 ĮY╣¹┼cėæšō
ĪĪĪĪ2.1 ▓╗═¼Ė─ąįŚl╝■ī”Ęą╩»╚ź│²ÅU╦«ųąī”Ž§╗∙▒ĮĘėąį─▄Ą─ė░Ēæ
ĪĪĪĪė╔łD 1┐╔ų¬Ż¼«ö▓╗š{╣ØHDTMA╚▄ę║Ą─pHųĄŻ¼▓╗═¼┘|┴┐ØŌČ╚Ą─HDTMA╚▄ę║Ė─ąįųŲéõĄ─Ęą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─ŲĮ║Ō╬³ĖĮ┴┐Š∙Ė▀ė┌╠ņ╚╗Ęą╩»Ą─0.54 mg Īżg-1Ż¼░┤ššå╬│╠ķ¬[14]Ą─蹊┐Ż¼╠ņ╚╗Ęą╩»Įø▀^HDTMAĖ─ąį║¾Ż¼ė╔ė┌HDTMAĮYśŗųą╩Ķ╦«ķL╠╝µ£ķgĄ─ŽÓ╗źū„ė├Ż¼į┌Ęą╩»▒Ē├µą╬│╔┴╦ŅÉ╦Ų─z╩°Ą─ę╗īėĖ▓╔w╬’Ż¼╩╣ī”Ž§╗∙▒ĮĘė═©▀^Ęų┼õū„ė├▀M╚ļĄĮĘą╩»▒Ē├µĄ─HDTMAėąÖCŽÓųąČ°Ą├ęį╚ź│². īŹ“×ĮY╣¹’@╩ŠŻ¼«öHDTMA╚▄ę║┘|┴┐ĘųöĄ×ķ1.2%ĢrŻ¼┼c╠ņ╚╗Ęą╩»ęį10 Ī├1▒╚└²╗ņ║ŽųŲéõĄ─Ė─ąįĘą╩»ī”ÅU╦«ųąĄ─ī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮ┴┐▀_ĄĮūŅ┤¾Ż¼╝s×ķ2.52 mg Īżg-1Ż¼Ė▀ė┌╗“Ą═ė┌1.2%ĢrŻ¼ī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮ┴┐Š∙├„’@ĮĄĄ═Ż¼▀@┼cå╬│╠ķ¬Ą╚Ą─蹊┐ĮYšōŽÓ╦Ų[13, 14]. HDTMAØŌČ╚Ą═ĢrŻ¼žō▌dĄĮĘą╩»▒Ē├µĄ─┴┐ąĪŻ¼▓╗─▄ėąą¦Ąžį┌Ęą╩»▒Ē├µą╬│╔╩Ķ╦«ąįĄ─Ė▓╔wīėŻ¼╚ń┤╦ųŲéõĄ├ĄĮĄ─Ė─ąįĘą╩»▓╗─▄ėąą¦ĄžĮY║Žī”Ž§╗∙▒ĮĘė; HDTMAØŌČ╚▀^Ė▀ĢrŻ¼ŲõĪ░ā╔ėHąįĪ▒ĮYśŗĢ■╩╣Ą├HDTMAęįļxūėĮ╗ōQĘĮ╩ĮĘų▓╝į┌Ęą╩»-ę║ŽÓĮń├µŻ¼Ęą╩»▒Ē├µ▀^ČÓĄ─HDTMAę▓Ģ■░l╔·ĮŌ╬÷¼FŽ¾Ż¼Å─Č°ĮĄĄ═Ė─ąįĘą╩»Ą─▒Ē├µĘĆČ©ąįŻ¼▀MČ°╩╣Ą├ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─ĮY║Ž─▄┴”▌^╚§[17, 18, 19].
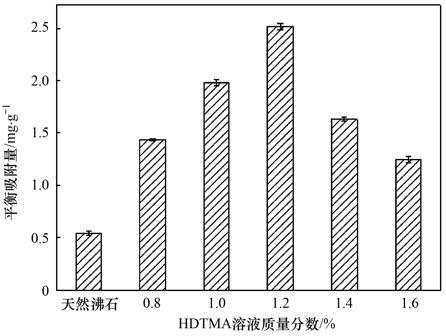
ĪĪĪĪłD 1 HDTMA╚▄ę║┘|┴┐ĘųöĄī”Ė─ąįĘą╩»╬³ĖĮÅU╦«ųąī”Ž§╗∙▒ĮĘėą¦╣¹Ą─ė░Ēæ
ĪĪĪĪė╔łD 2┐╔ų¬Ż¼į┌Ė─ąįĘą╩»ųŲéõ▀^│╠ųąŻ¼▒Ż│ųHDTMA╚▄ę║┘|┴┐ØŌČ╚▓╗ūāĄ─ŪķørŽ┬Ż¼ļSų°HDTMA╚▄ę║pHųĄį÷╝ėų┴10Ż¼╦∙ųŲéõĄ├ĄĮĄ─Ė─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮ┴┐ųØuį÷╝ėŻ¼▓ó▀_ĄĮ2.53 mg Īżg-1. ╦ßēAŚl╝■ė░ĒæĖ─ąįą¦╣¹Ą─įŁę“į┌ė┌Ż║╦ßąįŚl╝■Ž┬Ż¼Ęą╩»▒Ē├µĄ─▓┐ĘųSiĪ¬OH║═AlĪ¬OH╗∙łFę“┘|ūė╗»Č°Ä¦š²ļŖŻ¼▓╗└¹ė┌HDTMAĄ─žō▌dŻ¼╚ń┤╦ųŲéõĄ├ĄĮĄ─Ė─ąįĘą╩»▓╗─▄ėąą¦ĮY║Žī”Ž§╗∙▒ĮĘė; ŽÓĘ┤Ż¼ēAąįŁhŠ│Ė³ėą└¹ė┌HDTMAį┌Ęą╩»▒Ē├µĄ─žō▌dŻ¼▀@╩Ūė╔ė┌ēAąįŁhŠ│╩╣Ą├Ęą╩»╝▄śŗųąĄ─č§Ä¦žōļŖ║╔[20]. ėąčąŠ┐▒Ē├„Ż¼ÅŖēAąįŁhŠ│ę²╚ļĄ─NaOHę▓Ģ■Ė─╔ŲĘą╩»╬³ĖĮ╬█╚Š╬’Ą─ąį─▄[21]. ŠC╔Ž┐╝æ]Ż¼į┌Ž┬╩÷╬³ĖĮīŹ“×ųąŻ¼Ė─ąįĘą╩»Ą─ųŲéõŚl╝■įOų├×ķHDTMA╚▄ę║┘|┴┐ØŌČ╚1.2%Ż¼pHųĄ10.

ĪĪĪĪłD 2 HDTMA╚▄ę║pHųĄī”Ė─ąįĘą╩»╬³ĖĮÅU╦«ųąī”Ž§╗∙▒ĮĘėą¦╣¹Ą─ė░Ēæ
ĪĪĪĪ2.2 ╬³ĖĮŚl╝■ī”Ęą╩»╚ź│²ÅU╦«ųąī”Ž§╗∙▒ĮĘėąį─▄Ą─ė░Ēæ
ĪĪĪĪī”Ž§╗∙▒ĮĘėĄ─╚ź│²┬╩┼cĘą╩»═Č╝ė┴┐į┌ę╗Č©ĘČć·ā╚│╩š²ŽÓĻPĻPŽĄ. å╬│╠ķ¬Ą╚[13]蹊┐▒Ē├„Ż¼ļSų°Ė─ąįĘą╩»═Č╝ė┴┐Ą─į÷╝ėŻ¼╚ź│²┬╩ųØuį÷┤¾Ż¼Ą½═Č╝ė┴┐│¼▀^20 g ĪżL-1Ģr╚ź│²┬╩į÷Ę∙ųØuūāŠÅ. ė╔łD 3┐╔ų¬Ż¼HDTMAĖ─ąįĘą╩»═Č╝ė┴┐į┌4-8 g ĪżL-1ĘČć·ā╚ūā╗»ĢrŻ¼ÅU╦«ųąī”Ž§╗∙▒ĮĘė╚ź│²┬╩ļSų°Ė─ąįĘą╩»═Č╝ė┴┐Ą─į÷╝ėČ°į÷┤¾Ż¼Č°Ūęį÷ķL╦┘┬╩▌^┐ņŻ¼═Č╝ė┴┐×ķ8 g ĪżL-1ĢrŻ¼╚ź│²┬╩Ė▀▀_89.7%. └^└m═Č╝ėĖ─ąįĘą╩»Ż¼ī”Ž§╗∙▒ĮĘė╚ź│²┬╩│ų└mį÷╝ėŻ¼Ą½į÷╝ė┌ģä▌ūāĄ├ŠÅ┬²Ż¼▀@╩Ūę“×ķ═Č╝ė┴┐▌^ąĪĢrŻ¼▀_ĄĮ╬³ĖĮŲĮ║ŌĀŅæBĢr╦∙╬³ĖĮĄ─ī”Ž§╗∙▒ĮĘėĄ─┐é┴┐║▄ąĪŻ¼¾w¼F×ķ╚ź│²┬╩▌^Ą═; ļSų°Ęą╩»═Č╝ė┴┐Ą─į÷╝ėŻ¼Ųõ╬³ĖĮĄ─ī”Ž§╗∙▒ĮĘė┴┐ę▓į┌▓╗öÓį÷╝ėŻ¼¾w¼F×ķ╚ź│²┬╩ļS═Č╝ė┴┐Ą─į÷╝ėČ°į÷┤¾. ļSų°Ęą╩»═Č╝ė┴┐į÷╝ėĄĮ╬³ĖĮäėæBŲĮ║ŌŻ¼Ęą╩»╬³ĖĮĄ─ī”Ž§╗∙▒ĮĘė┐é┴┐┼cÅU╦«ųąī”Ž§╗∙▒ĮĘėØŌČ╚ų«ķgĄ─ØŌČ╚ē║▓ŅįĮüĒįĮąĪŻ¼ūŅĮKī¦ų┬ī”Ž§╗∙▒ĮĘė╚ź│²┬╩ųØu▀_ĄĮŲĮ║Ō.
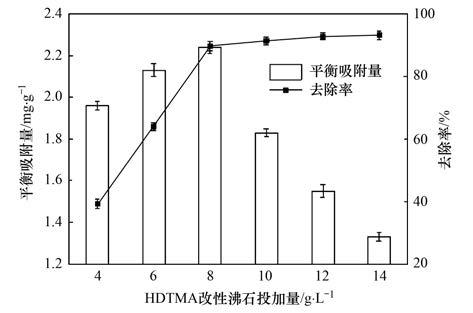
ĪĪĪĪłD 3 Ė─ąįĘą╩»═Č╝ė┴┐ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘė╬³ĖĮą¦╣¹Ą─ė░Ēæ
ĪĪĪĪė╔łD 4┐╔ų¬Ż¼į┌▓╗═¼pHŚl╝■Ž┬Ż¼Ė─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╚ź│²┬╩Š∙Ė▀ė┌╠ņ╚╗Ęą╩»Ą─ūŅ┤¾╚ź│²┬╩(21.6%). ļSų°ÅU╦«pHĄ─į÷╝ėŻ¼Ė─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╚ź│²┬╩ųØuį÷╝ėŻ¼į┌pH×ķ6ĢrŻ¼ī”Ž§╗∙▒ĮĘėĄ─╚ź│²┬╩ūŅĖ▀Ż¼╝s×ķ93.9%. «öÅU╦«×ķēAąįĢr(╚ńpH=8)Ż¼ī”Ž§╗∙▒ĮĘėĄ─╚ź│²┬╩├„’@ĮĄĄ═Ż¼ļSų°pHųĄĄ─└^└mį÷╝ė(pH>8)Ż¼ī”Ž§╗∙▒ĮĘėĄ─╚ź│²┬╩Ę┤Č°ėą╦∙į÷╝ė(į÷╝ėų┴83.5%). ėąčąŠ┐š▀šJ×ķ[14]Ż¼│÷¼F╔Ž╩÷¼FŽ¾╩Ūė╔ė┌ÅU╦«pHĄ─ūā╗»ī¦ų┬ī”Ž§╗∙▒ĮĘėļŖžōąįĄ─Ė─ūāŻ¼ī”Ž§╗∙▒ĮĘėį┌╦ßąįŚl╝■Ž┬ęįĘųūėą╬æB┤µį┌Ż¼ēAąįŚl╝■Ž┬ęįļxūėą╬æB┤µį┌; ī”Ž§╗∙▒ĮĘėĮŌļx│ŻöĄ×ķ7.16Ż¼pH=6ĢrÅU╦«ųąĄ─ī”Ž§╗∙▒ĮĘėų„ę¬╩ŪĘųūėæBŻ¼į┌Ęą╩»▒Ē├µĄ─HDTMAėąÖCŽÓųąĄ─Ęų┼õŽĄöĄ▀h┤¾ė┌╦«ŽÓ(ŽÓ╦ŲŽÓ╚▄įŁ└Ē)Ż¼Ė³╚▌ęū▒╗╬³ĖĮŻ¼ę“Č°╚ź│²┬╩▌^┤¾. ÅU╦«pHĖ▀ė┌7.16ĢrŻ¼ī”Ž§╗∙▒ĮĘė▓┐Ęųęįļxūėą╬╩Į┤µį┌Ż¼╩╣Ą├Ęųūė╬³ĖĮĮĄĄ═Ż¼į┌ėąÖCŽÓųąĄ─Ęų┼õ┬╩ĮĄĄ═Ż¼ę“┤╦Ż¼pH=8ĢrŻ¼ī”Ž§╗∙▒ĮĘė╚ź│²┬╩▌^Ą═. ļSēAąįŁhŠ│Ą─└^└mį÷ÅŖ(pH>8)Ż¼ÅU╦«ųąĄ─ī”Ž§╗∙▒ĮĘė┤¾▓┐ĘųĮŌļx│╔ĻÄļxūėŻ¼═©▀^ĻÄĪó Ļ¢ļxūėų«ķgĄ─ņoļŖę²┴”▒╗╬³ĖĮĄĮĦš²ļŖĄ─╗Ņąįä®═ŌīėŻ¼ę“Č°┤╦ĢrĄ─╬³ĖĮ┴┐į÷╝ėŻ¼Åł╝t├ĘĄ╚[22]Ą─蹊┐ū¶ūC┴╦▀@ę╗ė^³c. ╔Ž╩÷ĮY╣¹▒Ē├„Ż¼HDTMAĖ─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮų„ę¬╗∙ė┌Ęų┼õū„ė├Ż¼╠ņ╚╗Ęą╩»Įøė╔ėąÖC╩Ķ╦«ąį▒Ē├µ╗Ņąįä®(HDTMA)Ė─ąį║¾Ż¼Ųõ▒Ē├µą╬│╔ėąÖCĘų┼õŽÓŻ¼┐╔ęį╩╣ī”Ž§╗∙▒ĮĘė║▄║├ĄžĪ░╚▄ĮŌĪ▒į┌▀@īėėąÖC─żųąŻ¼ūŅĮKį┌╦«ŽÓ║═HDTMAā╔ŽÓķg▀_ĄĮĘų┼õŲĮ║Ō.
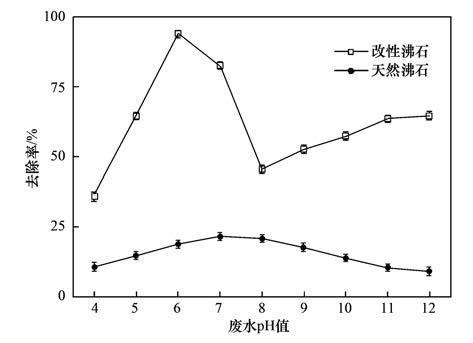
ĪĪĪĪłD 4 ī”Ž§╗∙▒ĮĘėÅU╦«pHųĄī”ÅU╦«ųąī”Ž§╗∙▒ĮĘė╬³ĖĮą¦╣¹Ą─ė░Ēæ
ĪĪĪĪłD 5Ę┤ė│┴╦ī”Ž§╗∙▒ĮĘėĄ─╚ź│²ų„ę¬░l╔·į┌╬³ĖĮ▀^│╠Ū░60 minŻ¼Ė─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╚ź│²┬╩ļSų°Ę┤æ¬ĢrķgĄ─čėķLčĖ╦┘į÷╝ėĄĮ81.7%. į┌30-60 min╚ź│²┬╩Ģ■│÷¼F▓©äėŻ¼įŁę“╩Ū╬³ĖĮĘ┤æ¬ķ_╩╝ĢrŻ¼ī”Ž§╗∙▒ĮĘė▒╗čĖ╦┘╬³ĖĮį┌Ė─ąįĘą╩»Ą─▒Ē├µŻ¼Ą½ė╔ė┌╬³ĖĮĄ├▓╗ē“└╬╣╠Ż¼ī”Ž§╗∙▒ĮĘė┐╔─▄▓┐Ęų░l╔·├ōĖĮŻ¼Å─Č°ī¦ų┬╬³ĖĮą¦╣¹│÷¼F▓©äė. ļSų°ĢrķgĄ─═ŲęŲŻ¼ī”Ž§╗∙▒ĮĘėĘųūėÅ─Ė─ąįĘą╩»▒Ē├µĄ─ėąÖCŽÓŽ“ā╚▓┐öU╔óĄĮĘą╩»┐ūĄ└ųąŻ¼▓óį┌90 minĢrŻ¼╬³ĖĮ┌ģė┌ĘĆČ©Ż¼╚ź│²┬╩▀_ĄĮ93.9%.
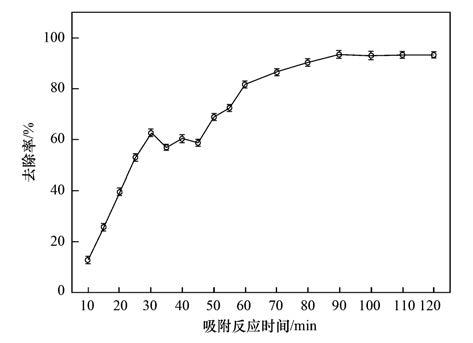
ĪĪĪĪĘą╩»═Č╝ė┴┐Ż║8 g ĪżL-1; pH=6łD 5 ╬³ĖĮĢrķgī”ÅU╦«ųąī”Ž§╗∙▒ĮĘė╬³ĖĮą¦╣¹Ą─ė░Ēæ
ĪĪĪĪ2.3 ╬³ĖĮäė┴”īW║═╬³ĖĮĄ╚£žŠĆ
ĪĪĪĪė╔▒Ē 1┐╔ų¬Ż¼ę╗╝ēäė┴”īW─Żą═Ą─╦┘┬╩│ŻöĄk1║═Č■╝ēäė┴”īW─Żą═Ą─╦┘┬╩│ŻöĄk2Š∙ļSų°ÅU╦«ųą│§╩╝ī”Ž§╗∙▒ĮĘėØŌČ╚Ą─į÷╝ėČ°į÷┤¾Ż¼│§╩╝ī”Ž§╗∙▒ĮĘėØŌČ╚×ķ┐╦Ę■ę║ŽÓ║═╣╠ŽÓų«ķgĄ─é„┘|ūĶ┴”╠ß╣®┴╦ųžę¬Ą─═Ųäė┴”Ż¼ę“┤╦Ż¼│§╩╝ī”Ž§╗∙▒ĮĘėØŌČ╚Ą─╔²Ė▀į┌ę╗Č©ĘČć·ā╚ėą└¹ė┌╠ßĖ▀Ęą╩»Ą─╬³ĖĮ─▄┴”. ┤╦═ŌŻ¼ā╔éĆ─Żą═Ą─╦┘┬╩│ŻöĄk1║═k2ļSų°ÅU╦«£žČ╚Ą─į÷╝ėČ°ĮĄĄ═Ż¼ļSų°pHųĄĄ─╔²Ė▀Č°į÷┤¾. ▓╗═¼īŹ“׌l╝■Ž┬Ż¼ę╗╝ēäė┴”īW─Żą═Ą─ŽÓĻPŽĄöĄ(R2)Š∙Ė▀ė┌0.90Ż¼Č■╝ēäė┴”īW─Żą═Ą─ŽÓĻPŽĄöĄ(R2)ätŠ∙Ą═ė┌0.90Ż¼Č°Ūęę╗╝ēäė┴”īW─Żą═ėŗ╦Ń│÷Ą─ŲĮ║Ō╬³ĖĮ┴┐Ė³╝ėĮėĮ³īŹ“×ųĄ(ŽÓī”š`▓ŅĖ³ąĪ)Ż¼šf├„ę╗╝ēäė┴”īW─Żą═─▄Ė³║├ĄžöM║ŽĖ─ąįĘą╩»╬³ĖĮÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─▀^│╠. ╚ń▒Ē 2╦∙╩ŠŻ¼▓╗═¼£žČ╚Śl╝■Ž┬(25Īó 35Īó 45Īµ)Ż¼ė╔ė┌Langmuir╬³ĖĮĄ╚£žŠĆĄ─R2▌^Ė▀Ż¼šf├„Ųõ─▄ē“Ė³║├ĄžöM║ŽīŹ“×öĄō■.Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.jianfeilema.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
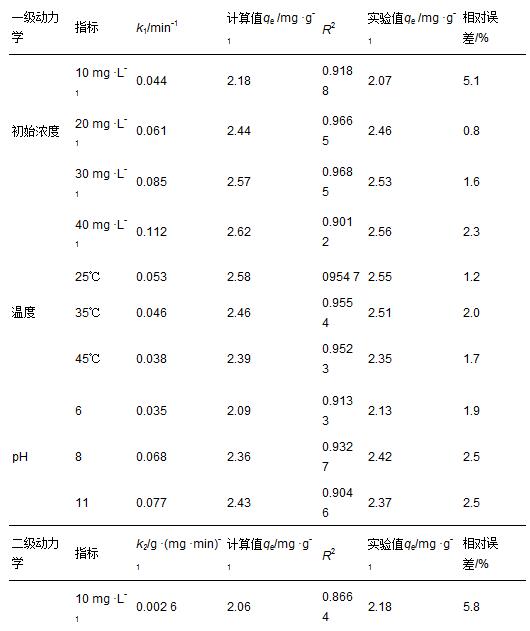
ĪĪ▒Ē 1 ī”Ž§╗∙▒ĮĘė╬³ĖĮäė┴”īWģóöĄ

ĪĪĪĪ▒Ē 2 ī”Ž§╗∙▒ĮĘė╬³ĖĮĄ╚£žŠĆģóöĄ
ĪĪĪĪ3 ĮYšō
ĪĪĪĪ(1) HDTMA┘|┴┐ØŌČ╚┼cpHųĄī”╦∙ųŲéõĄ─Ė─ąįĘą╩»╬³ĖĮī”Ž§╗∙▒ĮĘėĄ──▄┴”ė░Ēæ▌^┤¾. HDTMA┘|┴┐ĘųöĄ×ķ1.2%Ż¼Ūęį┌ēAąįŚl╝■Ž┬(pH=10)Ż¼╦∙ųŲéõĄ─ėąÖCĖ─ąįĘą╩»ī”ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─╬³ĖĮ┴┐ūŅ┤¾(2.53 mg Īżg-1).
ĪĪĪĪ(2) HDTMAĖ─ąįĘą╩»╚ź│²ÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─īŹ“×ųąŻ¼«öī”Ž§╗∙▒ĮĘėÅU╦«pH=6ĢrŻ¼═Č╝ė8 g ĪżL-1Ą─Ė─ąįĘą╩»Ż¼Ę┤æ¬90 min║¾Ż¼ī”Ž§╗∙▒ĮĘėĄ─╚ź│²ą¦╣¹ūŅ║├Ż¼╚ź│²┬╩▀_ĄĮ93.9%.
ĪĪĪĪ(3) ╬³ĖĮäė┴”īW▒Ē├„Ż¼ę╗╝ēäė┴”īW─Żą═─▄Ė³║├ĄžöM║ŽĖ─ąįĘą╩»╬³ĖĮÅU╦«ųąī”Ž§╗∙▒ĮĘėĄ─▀^│╠; Ą╚£žŠĆ蹊┐▒Ē├„Ż¼LangmuirĄ╚£žŠĆ─▄ē“▌^║├ĄžöM║ŽīŹ“×öĄō■.