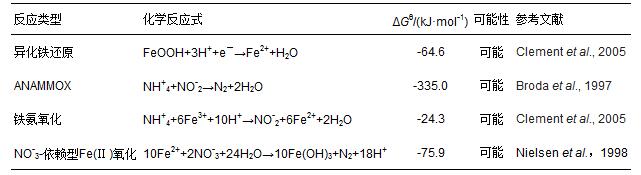
Fe(ó¾)ī”╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁ±Ņ║Ž├ōĄ¬Ą─ė░Ēæ
ųąć°╬█╦«╠Ä└Ē╣ż│╠ŠW ĢrķgŻ║2016-7-19 14:04:34
╬█╦«╠Ä└Ē╝╝ąg | ģRŠ█╚½Ū“Łh▒Ż┴”┴┐Ż¼ĮĄĄ═Ų¾śIų╬╬█│╔▒Š
ĪĪĪĪ1 ę²čį
ĪĪĪĪ«É╗»ĶF▀ĆįŁŻ¼ėųĘQĶF║¶╬³Ż¼╩Ūė╔╠žČ©╬ó╔·╬’“īäėĄ─├Ė┤┘Ę┤æ¬Ż¼ĶF▀ĆįŁŠ·ät╩ŪīŹ¼F▀@ę╗▀^│╠Ą─ų„¾w.įńį┌20╩└╝o│§╚╦éāŠ═ŽÓ└^░l¼F┴╦Fe(ó¾)▀ĆįŁ¼FŽ¾(Harder et al., 1919; Allison et al., 1942; Lovely et al., 1988)Ż¼Į³─ĻüĒŻ¼ļSų°╚╦éāī”«É╗»Fe(ó¾)▀ĆįŁ▀^│╠šJūRĄ─▓╗öÓ╔Ņ╚ļŻ¼Fe(ó¾)Ą─╬ó╔·╬’«É╗»▀ĆįŁ▀^│╠į┌ŁhŠ│╬█╚Šų╬└Ē┼cą▐Å═ŅIė“Ą─æ¬ė├ę▓įĮüĒįĮ╩▄ĄĮųžęĢ.蹊┐▒Ē├„Ż¼╬ó╔·╬’«É╗»Fe(ó¾)▀ĆįŁ▀^│╠┐╔±Ņ┬ōėąÖC╬’ė╚Ųõ╩ŪļyĮĄĮŌėąÖC╬’(╚ń┬╚┤·ėąÖC╬’Īó┼╝Ą¬╚Š┴ŽĪó╩»╗»ŅÉėąÖC╬’)Ą─č§╗»ĮĄĮŌĪóėąČŠųžĮī┘ļxūė(ŌÖĪóŃtĪó╔ķĄ╚)Ą─ĄV╗»╝░ģó┼cūį╚╗ĮńųąĄ─Ą¬┴ū裣h(Li et al., 2010; Sabrina et al., 2007).═¼ĢrŻ¼«É╗»Fe(ó¾)▀ĆįŁ╬ó╔·╬’╝┤ĶF▀ĆįŁŠ·(Iron-reducing bacteriaŻ¼IRB)ę▓╩Ū╗Ņąį╬█─ÓĄ─ųžę¬ĮM│╔▓┐ĘųŻ¼įōŅÉ╬ó╔·╬’┐╔š╝ĄĮ╗Ņąį╬█─Ó╬ó╔·╬’┐é┴┐Ą─3%ū¾ėę(Nielsen et al., 2002).ę“┤╦Ż¼ÅŖ╗»╬█╦«╠Ä└ĒŽĄĮyųą╬ó╔·╬’«É╗»Fe(ó¾)▀ĆįŁ▀^│╠Ż¼ī”ė┌╠ßĖ▀╬█╦«╠Ä└ĒŽĄĮyī”ļyĮĄĮŌėąÖC╬’Ą─ĮĄĮŌą¦┬╩Ż¼ęį╝░Ė─╔Ų╬█╦«ųą├ōĄ¬│²┴ūą¦╣¹Ą╚ėąų°ųžę¬Ą─ęŌ┴x.Ȱ蹊┐▓╗═¼ą╬╩ĮĄ─Fe(ó¾)ī”╗Ņąį╬█─Ó╬ó╔·╬’«É╗»▀ĆįŁ▀^│╠Ą─ė░ĒæŻ¼īżšęę╗ĘN┴«ārĪóęū▒╗╬ó╔·╬’└¹ė├Ą─Fe(ó¾)į┤Ż¼¤oę╔╩ŪīŹ¼F▀@ę╗▀^│╠Ą─ĻPµI.IvanovĄ╚(2010)└¹ė├ĶFĄV╩»┼cFe(OH)3ī”ŁhŠ│ųą┤Ų╝ż╦žĄ─ĮĄĮŌą¦╣¹▀Mąą┴╦ĮøØ·ąį▒╚▌^;StabnikovĄ╚(2004)▓╔ė├رĄžĶFĄV╩»ĪóĖ╗ĶFš│═┴«a╔·Fe(ó“)▀_ĄĮ│²┴ūĄ──┐Ą─;ÖĶĖ╗▓©Ą╚(2009)蹊┐┴╦ßśĶFĄVĪó│ÓĶFĄVĪó┤┼ĶFĄV║═õōį³Ą╚ĶFč§╗»╬’▒Ē├µĮY║ŽĶFŽĄĮyī”Ž§╗∙▒ĮĄ─▀ĆįŁ▐D╗»─▄┴”.Ą½─┐Ū░┤¾ČÓ蹊┐ų„ę¬ĻPūóė┌ĶF▀ĆįŁŠ·╝āŠ·Ą─æ¬ė├Ż¼Ūę╩╣ė├Śl╝■┐┴┐╠Ż¼Č°čąŠ┐ģÆ觌l╝■Ž┬╗Ņąį╬█─Ó╬ó╔·╬’Ą─«É╗»▀ĆįŁ▀^│╠Ż¼▓óīóŲõæ¬ė├ė┌╬█╦«├ōĄ¬ĘĮ├µĄ─╬─½I▀ƧręŖł¾Ą└.
ĪĪĪĪę“┤╦Ż¼▒ŠčąŠ┐▓╔ė├┴«ārĄ─č§╗»ĶFŲżĪóŪÓĄV║═╝tĄV┼cFe(OH)3ū„×ķFe(ó¾)į┤Ż¼═©▀^ŲĮąąī”▒╚įć“×┐╝▓ņ┴╦▓╗═¼ą╬╩ĮFe(ó¾)ī”╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁ─▄┴”╝░¾wŽĄųą▓╗═¼ą╬╩ĮĄ¬ūā╗»Ą─ė░ĒæŻ¼▓óī”╬ó╔·╬’Įķī¦Ą─ČÓĮMĘųĮ╗╗źū„ė├ÖCųŲŻ¼ė╚Ųõ╩Ū╬ó╔·╬’-Fe-N±Ņ║ŽÖCųŲ▀Mąą│§▓Į╠ĮėæŻ¼ų╝į┌×ķ═Č┘Y╔┘Īó▀\ąą┘Mė├Ą═Īó├ōĄ¬ą¦╣¹ĘĆČ©Ą─│Ū╩ą╬█╦«├ōĄ¬╣ż╦ćĄ─ķ_░l╠ß╣®ę╗ĘNą┬Ą─╦╝┬Ę.
ĪĪĪĪ2 ▓─┴Ž┼cĘĮĘ©
ĪĪĪĪ2.1.1 ▓─┴ŽĄ─ųŲéõ
ĪĪĪĪīŹ“×▀xė├č§╗»ĶFŲżĪóŪÓĄVĪó╝tĄVū„×ķFe(ó¾)į┤Ż¼▓óęį│Żė├Ą─Fe(ó¾)į┤Ī¬Ī¬Fe(OH)3ū„×ķī”▒╚.īŹ“×ė├Fe(OH)3æęę║(║¼ĶF┴┐×ķ5.188 g Īż L-1)▓╔ė├╚╦╣ż║Ž│╔Ą─ĘĮĘ©┼õųŲŻ¼╝┤ė├0.4 mmol Īż L-1Ą─FeCl3║═0.5 mol Īż L-1 NaOH╚▄ę║┬²╦┘ųą║═│┴ĄĒŻ¼Ą├ĄĮĄ─╝t║ų╔½│┴ĄĒė├╚źļxūė╦«Ę┤Å═Ž┤£ņŻ¼ųžÅ═6┤╬ų┴═Ļ╚½╚ź│²æęę║ųąĄ─┬╚ļxūė║═Ōcļxūė×ķų╣(Lovley et al., 1986).▓╔ė├JSM-5600LVĄ═šµ┐šÆ▀├ĶļŖūė’@╬óńRX╔õŠĆ─▄┴┐╔½╔óūVāxī”č§╗»ĶFŲżĪóŪÓĄV╝░╝tĄV▀Mąą▒Ē├µą╬├▓ė^▓ņ(łD 1)╝░ĮM│╔Ęų╬÷(▒Ē 1)Ż¼┐╔ęŖŻ¼č§╗»ĶFŲż▒Ē├µų┬├▄Ż¼Č°ŪÓĄV║═╝tĄV┴Ż Č╚Ęų╔óŻ¼│╩▌^×ķ├▄īŹĄ─ĘĆČ©ĮYśŗą╬╩ĮŻ¼║¼ĶF┴┐(┘|┴┐ĘųöĄ)ę└┤╬╝s×ķ71.3%Īó58.6%Īó36.2%.ė╔ė┌īŹ“×▓╔ė├Ą─č§╗»ĶFŲżŠ▀ėąę╗Č©Ą─čėš╣ąįŻ¼▌^ļyŲŲ╦ķŻ¼ę“┤╦Ż¼═Č╝ėŪ░īóč§╗»ĶFŲż╝¶╦ķų┴┴ŻÅĮ×ķ2.0~3.0 mmĄ─ŚlĀŅŻ¼Č°ā╔ĘNĄV╩»Š∙ĮøĘ█╦ķĪóčą─źĪó║YĘųŻ¼▀xō±80─┐┴ŻÅĮ▀Mąąįć“×.

ĪĪĪĪłD 1 │§╩╝▓╗═¼Fe(ó¾)Ą─▒Ē├µą╬├▓ė^▓ņłD(a.č§╗»ĶFŲżŻ¼b.ŪÓĄVŻ¼c.╝tĄV)
ĪĪĪĪ▒Ē1 ▓╗═¼Fe(ó¾)üĒį┤╝░ĮM│╔│╔Ęų▒╚▌^
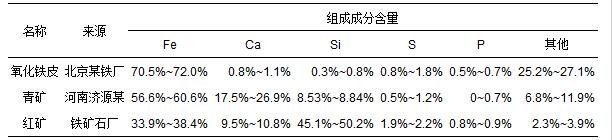
ĪĪĪĪ2.1.2 ĮėĘN╬█─Ó┼cīŹ“×ė├╬█╦«
ĪĪĪĪĮėĘN╬█─Ó╚Īūį▒ŠīŹ“×╩ęųąčb╠Ņėą║ŻŠdĶF-AT-PVFÅ═║Ž╠Ņ┴ŽĄ─SBBRĘ┤æ¬Ų„Ż¼ėąą¦╚▌Ęe×ķ0.36 m3(└ŅĮ▄Ą╚Ż¼2010).įōĘ┤æ¬Ų„ęčĘĆČ©▀\ąą1─ĻČÓŻ¼╬█─ÓŠ▀ėą▌^Ė▀Ą─╬ó╔·╬’╗Ņąį.īóįōĮėĘN╬█─Óė├╚źļxūė╦«Ę┤Å═ŪÕŽ┤Īóļxą─Ż¼ęįĮĄĄ═╬█─ÓųąFe(ó“)ĪóNH+4-NŻ¼═Ļ╚½╚ź│²NO-2-NĪóNO-3-NļxūėŻ¼▒▄├Ōī”īŹ“׫a╔·Ė╔ö_.ūŅĮK£yČ©ō]░ląįæęĖĪ╣╠¾w(MLVSS)┼cæęĖĪ╣╠¾w(MLSS)Ą─▒╚ųĄ×ķ0.6Ż¼pHųĄ×ķ7.2Ż¼╦∙║¼Fe(ó“)║═Fe(tot)║¼┴┐Ęųäe×ķ14.83Īó200.55 mg Īż L-1Ż¼╬┤Öz£y│÷NO-2-NĪóNO-3-N.ŲõųąŻ¼Ę┤款wŽĄā╚╬█─ÓĮėĘN┴┐×ķ1.41 g Īż L-1.
ĪĪĪĪ▓╔ė├╚╦╣ż┼õ╦«Ż¼┼õ╦«│╔Ęų×ķŻ║10 mLŲŽ╠č╠Ū(10 mmol Īż L-1)Īó5 mL┬╚╗»õ@(5 g Īż L-1)╝░25 mmol Īż L-1Ą─┴ū╦ß¹}ŠÅø_ę║(KH2PO4┼cK2HPO4Ą──”Ā¢▒╚×ķ0.5809)1.5 mLŻ¼ŲõųąŻ¼╬ó╔·╬’╦∙ąĶ╬ó┴┐į¬╦žė╔ĮėĘN╬█─Ó▒Š╔Ē╦∙║¼ę║╦∙╠ß╣®.įō║Ž│╔╬█╦«│§╩╝TNĪóNH+4-NĘųäe×ķ137.8║═121.0 mg Īż L-1.
ĪĪĪĪ2.2 īŹ“×ĘĮĘ©
ĪĪĪĪ2.2.1 ▓╗═¼ą╬╩ĮFe(ó¾)├ōĄ¬ą¦╣¹Ą─ī”▒╚īŹ“×
ĪĪĪĪ▓╔ė├ģÆč§║Ń£ž┼ÓBīŹ“ׯ¼╚Ī6éĆŽĄ┴ą100 mLč¬ŪÕŲ┐(├┐éĆŽĄ┴ą░³└©9éĆŲ┐)Ż¼╝ė╚ļ╔Ž╩÷╚╦╣ż┼õ╦«Ż¼Ęųäe═Č╝ė1 g(ęįĶFč§╗»╬’┘|┴┐ėŗ)▓╗═¼ą╬╩ĮFe(ó¾)Ż¼ų├ė┌Ė▀ē║£ńŠ·Õüā╚Ż¼ė┌121 ĪµŽ┬£ńŠ·20 minŻ¼Ę┼ų┴¤oŠ·╩ę▀Mąą└õģsŻ¼ć└Ė±░┤¤oŠ·▓┘ū„Ę©ĮėĘNĮøģÆč§╠Ä└Ē((30Ī└1)ĪµŽ┬├▄ĘŌ7 d)║¾Ą─╔Ž╩÷ĮėĘN╬█─ÓŻ¼═¼ĢrįOų├£ńŠ·Ą─╗Ņąį╬█─Ó(CK1)(ė├15%(V/V)Ą─ęę┤╝Į■┼▌Ė¶ę╣)(Ivanov et al., 2010).ūŅ║¾Č©╚▌ų┴80 mLŻ¼│õĄ¬┼┼觯¼┐žųŲ╗ņ║Žę║│§╩╝pHį┌7.2Ī└0.2ū¾ėę.Ė„ĮMŠ∙╝ė╔w├▄ĘŌŻ¼ė┌(30Ī└1)Īµ║Ń£ž┼ÓBŽõųą▒▄╣Ō┼ÓB.╦∙ėą£yįćŠ∙3┤╬ųžÅ═.
ĪĪĪĪ2.2.2 ĶF▀ĆįŁ▀^│╠ųą░l╔·NH+4č§╗»Ą─ūCīŹīŹ“×
ĪĪĪĪęįč§╗»ĶFŲżū„×ķĶF▀ĆįŁŠ·╬©ę╗ļŖūė╩▄¾wŻ¼▓╔ė├╚ń╔ŽīŹ“×ĘĮĘ©Ż¼čėķL┼ÓBĢrķgęįūĘ█Ö▀^│╠ųąNO-2║═NO-3ØŌČ╚Ą─ūā╗»Ż¼▓óėŗ╦ŃFe(ó“)«a╔·┴┐┼cNH+4č§╗»┴┐ų«ķgĻPŽĄ.
ĪĪĪĪ2.3 ╚Īśė╝░£yČ©ĘĮĘ©
ĪĪĪĪė╔ė┌╗Ņąį╬█─Ó«É╗»Fe(ó¾)▀ĆįŁ«a╔·Ą─Fe(ó“)╝╚┐╔ęįĮŌļxæBĄ─ą╬╩Į┤µį┌ėų┐╔ęį╬³ĖĮæBĄ─ą╬╩Į┤µį┌Ż¼ę“┤╦Ż¼īŹ“×ųą▓╔ė├0.5 mol Īż L-1¹}╦ß╚▄ę║ī”æęę║Į■╠ߣyČ©¾wŽĄĄ─Č■ārĶF║═╚²ārĶFĄ─ĘĮĘ©Ż¼▓óĘųäeęįFe(ó“)tot╝░Fe(ó¾)tot▒Ē╩Š.Š▀¾wĘĮĘ©╚ńŽ┬Ż║├┐┤╬▓╔śėĢrĖ„╚Ī│÷1Ų┐Ż¼│õĘųōuä“Ż¼Ė„╚Īįćśėā╔Ę▌.Ųõųąę╗Ę▌ė├ė┌Fe(ó“)║═Fe(tot)ØŌČ╚Ą─£yČ©Ż¼╝┤╬³╚Ī2 mLæęę║Ż¼ų├ė┌║¼8 mL(0.5 mol Īż L-1)¹}╦ß╚▄ę║Ą─Ħ╔wŠ█ęꎮļxą─╣▄ųąŻ¼į┌ōu┤▓╔Žš±╩ÄĮ■╠ß1 h(Stabnikov et al.Ż¼2004);┴Ē╚Īę╗Ę▌(10 mL)ė├ė┌NH+4-N╝░TNĄ─£yČ©.Š∙į┌1500 r Īż min-1Ą─▐D╦┘Ž┬ļxą─10 minŻ¼╚Ī╔ŽŪÕę║ė├0.22 ”╠m×V─ż▀^×V.Ė„ųĖś╦Ą─£yČ©Š∙▓╔ė├ś╦£╩Ę©(ć°╝ęŁhŠ│ūo┐éŠųŻ¼2002).Fe(ó“)╝░Fe(tot)£yČ©▓╔ė├ÓÅĘŲå¬▀°Ęų╣Ō╣ŌČ╚Ę©Ż¼TN£yČ©▓╔ė├ēAąį▀^┴“╦ßŌøŽ¹ĮŌūŽ═ŌĘų╣Ō╣ŌČ╚Ę©Ż¼NH+4-N£yČ©▓╔ė├╝{╩Žįćä®▒╚╔½Ę©Ż¼NO-2-N£yČ©▓╔ė├N-(1-▌┴╗∙)-ęęČ■░Ę╣ŌČ╚Ę©Ż¼NO-3-N£yČ©▓╔ė├„ĻŽŃ▓▌ĘėĘ©Ż¼pH£yČ©▓╔ė├▒Ńöy╩ĮČÓģóöĄ(pH/Oxi 340i)£yČ©āx.
ĪĪĪĪ3 ĮY╣¹┼cėæšō
ĪĪĪĪ3.1 ▓╗═¼Fe(ó¾)į┤ī”╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁ─▄┴”Ą─ė░Ēæ
ĪĪĪĪģÆ觌l╝■Ž┬IRBĄ─Ė╗╝»┼ÓBīŹ“×ųąŻ¼═Č╝ė▓╗═¼Fe(ó¾)¾wŽĄųąFe(ó“)tot╝░Fe(ó¾)totØŌČ╚ūā╗»╚ńłD 2╦∙╩ŠŻ¼ŲõųąŻ¼│§╩╝Fe(ó“)totØŌČ╚×ķ(16.71Ī└1.47)mg Īż L-1.ė╔łD 2┐╔ęŖŻ¼ī”ššĮM(CK1)Ą─Fe(ó“)tot╝░Fe(ó¾)totØŌČ╚╗∙▒Š▒Ż│ų▓╗ūāŻ¼▀@šf├„Ųõ╦³¾wŽĄųą╦∙░l╔·Ą─Fe(ó“)tot╝░Fe(ó¾)totØŌČ╚ūā╗»╩Ūė╔ IRBū„ė├Č°«a╔·.0~7 dŻ¼▓╗═¼Fe(ó¾)╩▄IRB«É╗»▀ĆįŁČ°ĮŌļx│÷Ą─Fe(ó“)totØŌČ╚┤¾ų┬│╩ŠĆąįį÷╝ėŻ¼▒Ē¼F│÷▌^║├Ą─ĶF▀ĆįŁ─▄┴”Ż¼ŲõųąŻ¼Fe(OH)3Īóč§╗»ĶFŲżĪóŪÓĄV╝░╝tĄVĄ─Fe(ó“)totūŅ┤¾«a╔·┬╩Ęųäe×ķ19.24Īó17.51Īó11.65Īó9.83 mg Īż L-1 Īż d-1Ż¼┼cFe(ó¾)į┤Ą─║¼ĶF┴┐│╩▌^║├Ą─š²Ž“ĻPŽĄ;Č°į┌ 7~13 d Fe(ó“)totØŌČ╚Š∙│╩¼F┐ņ╦┘Ž┬ĮĄ┌ģä▌Ż¼13 d║¾╗∙▒ŠĘĆČ©.ųĄĄ├ūóęŌĄ─╩ŪŻ¼łD 2bųąč§╗»ĶFŲż¾wŽĄųąFe(ó¾)totĄ─ØŌČ╚į┌Ū░7 d│╩¼F│ų└mŽ┬ĮĄĄ─┌ģä▌Ż¼ų«║¾│ų└mį÷╝ėŻ¼16 d║¾Ųõ¾wŽĄųąFe(ó¾)totØŌČ╚ęč│¼▀^ Fe(OH)3¾wŽĄ.šf├„č§╗»ĶFŲż╩Ūę╗ĘN▌^ęū▒╗╬ó╔·╬’└¹ė├Ą─ Fe(ó¾)į┤ą╬╩Į.

ĪĪĪĪłD 2 ▓╗═¼Fe(ó¾)į┤ī”╗Ņąį╬█─ÓĶF▀ĆįŁ▀^│╠ųąFe(ó“)tot╝░Fe(ó¾)totØŌČ╚Ą─ūā╗»
ĪĪĪĪ└█ėŗ┼ÓB7 d║¾¾wŽĄųąFe(ó“)totØŌČ╚│╩¼F│ų└mŽ┬ĮĄĄ─┌ģä▌Ż¼▀@┐╔─▄╩Ūė╔ė┌ęįŽ┬įŁę“ī¦ų┬Ż║ó┘ō■ŽÓĻPł¾Ą└(ųņŠS╗╬Ą╚Ż¼2011; Benner et al., 2002)Ż¼į┌╬ó╔·╬’▀ĆįŁ▀^│╠ųąėą┤┼ĶFĄV«a╔·Ą─¼FŽ¾░l╔·Ż¼╔·│╔┤┼ĶFĄVĄ─═¼ĢrŽ¹║─¾wŽĄųąĄ─Fe(ó“)Ż¼ī¦ų┬Fe(ó“)ØŌČ╚’@ų°Ž┬ĮĄ.īóģó╝ėĘ┤æ¬Ą─ĄV╬’ŽÓĮøXRDĘų╬÷Ż¼┤┼ĶFĄVĄ─╔·│╔┐╔ė├Ę┤æ¬╩Į2FeOOH+Fe(ó“)Ī·Feó“Feó¾O4+2H+▒Ē╩Š.ó┌ĮY║ŽłD 2┐╔ęį┐┤│÷Ż¼└█ėŗ┼ÓB7 d║¾Ż¼│²ī”ššĮM(CK1)═ŌŻ¼Ųõ╦³¾wŽĄųąFe(ó“)totØŌČ╚Š∙│÷¼F┐ņ╦┘Ž┬ĮĄ┌ģä▌Ż¼┼c┤╦═¼ĢrŻ¼Fe(ó¾)totŠ∙│÷¼F▓╗═¼│╠Č╚Ą─╔²Ė▀Ż¼ė╚Ųõ╩Ūč§╗»ĶFŲż ┼cFe(OH)3¾wŽĄŻ¼│÷¼F┴╦Fe(ó¾)totØŌČ╚╝▒äĪ╔²Ė▀Ą─¼FŽ¾.ĮY║Ž¾wŽĄNH+4-NĪóTN Ą─ūā╗»Ż¼┐╔ęį═Ų£y7 d║¾¾wŽĄųąģÆč§░▒č§╗»ū„ė├Ęe└█Ą─NO-3┐╔─▄┤┘▀M┴╦NO-3-ę└┘ćą═Fe(ó“)č§╗»(Nielsen et al., 1998; Ratering et al., 2001)ū„ė├Ą─░l╔·Ż¼īó«a╔·Ą─Fe(ó“)▀Mę╗▓Įč§╗»×ķFe(ó¾).ó█ė╔ė┌īŹ“×▓╔ė├Ą─╚╦╣ż┼õ╦«ųą║¼ėąę╗Č©┴ū╦ß¹}Ż¼Č°┴ū╦ßĖ∙║═ĮŌļxæBĶF╔·│╔Ą─Fe-PĮY║Ž╬’▀Mę╗▓ĮĢ■ą╬│╔Ė³ĘĆČ©æBĄ─ķ]ąŅæB┴ū(╔█┼d╚AŻ¼2005).
ĪĪĪĪ3.2 ▓╗═¼Fe(ó¾)ī”«É╗»ĶF▀ĆįŁ▀^│╠ųąĄ─├ōĄ¬ą¦╣¹ė░Ēæ
ĪĪĪĪ3.2.1 ī”├ōĄ¬ą¦╣¹Ą─ė░Ēæ
ĪĪĪĪī”▓╗═¼Fe(ó¾)▀ĆįŁ¾wŽĄųąNH+4-N╝░TN╚ź│²ą¦╣¹▀MąąĘų╬÷Ż¼ĮY╣¹╚ńłD 3a║═3b╦∙╩Š.ŲõųąŻ¼NH+4-NĪóTN│§╩╝ØŌČ╚Ęųäe×ķ(117.25Ī└8.45)║═(133.49Ī└8.11)mg Īż L-1Ż¼ī”ššĮM(CK1)Ą─NH+4-N╝░TN╗∙▒Šø]ėąūā╗»Ż¼Č°īŹ“×ĮM│÷╦«NH+4-NĪóTNØŌČ╚│╩ŠÅ┬²ĮĄĄ═Ą─┌ģä▌.Ė∙ō■NH+4-NĪóTNØŌČ╚Ą─ūā╗»Ż¼┐╔īóš¹éĆ▀^│╠Ęų×ķ3éĆļAČ╬Ż║0~10 dŻ¼Ė„¾wŽĄ├ōĄ¬ą¦╣¹¤o├„’@▓Ņ«ÉŻ¼▓©äė▌^┤¾;10~16 dŻ¼▓╗═¼Fe(ó¾)¾wŽĄī”NH+4-NĪóTNĄ─╚ź│²Š∙│╩¼FŽ┬ĮĄ┌ģä▌Ż¼Č°č§╗»ĶFŲż¾wŽĄ├ōĄ¬ą¦╣¹┬į║├Ż¼NH+4-NĪóTNØŌČ╚Ęųäeė╔│§╩╝Ą─110.25Īó129.58 mg Īż L-1ĮĄų┴68.56║═76.47 mg Īż L-1;ūŅ║¾ę╗ļAČ╬Ż¼č§╗»ĶFŲż¾wŽĄ├ōĄ¬ąį─▄’@ų°╠ßĖ▀Ż¼ūŅĮKNH+4-N╝░TNĄ─╚ź│²┬╩Ęųäe▀_ĄĮ73.65%Īó74.76%.ŲõųąŻ¼č§╗»ĶFŲż¾wŽĄNH+4-NĪóTN└█ėŗ╚ź│²┴┐ūŅ┤¾Ż¼Ęųäe×ķ75.04║═80.99 mg Īż L-1Ż¼╚▌ĘeTN╚ź│²┬╩×ķ3.88 mg Īż L-1 Īż d-1(ęįNėŗ)(łD 3c).

ĪĪĪĪłD 3 ═Č╝ė▓╗═¼Fe(ó¾)«É╗»▀ĆįŁ▀^│╠ųąĄ─├ōĄ¬ą¦╣¹▒╚▌^(a.░▒Ą¬; b.TN; c.└█ėŗ╚ź│²┴┐)
ĪĪĪĪClementĄ╚(2005)蹊┐░l¼FŻ¼į┌¤oü厧╦ß¹}┤µį┌Ą─Ū░╠ߎ┬Ż¼Fe(ó¾)Ą─┤µį┌─▄ē“ī¦ų┬│┴Ęe╬’║══┴╚└ųąģÆč§░▒č§╗»(ANAMMOX)¼FŽ¾Ą─░l╔·Ż¼┐╔─▄╩Ūė╔ė┌Fe3+/Fe2+Ą─ś╦£╩č§╗»▀ĆįŁļŖ╬╗×ķ770 mVŻ¼Č°č§ät×ķ816 mVŻ¼ā╔š▀ļŖ╗»īWąį─▄ŽÓĮ³Ż¼╚¶¾wŽĄųą╦∙║¼Ą─╝ÜŠ·Š▀ėą║Ž▀mĄ─├ĖŽĄĮy(╚ńGeobacter sulfurreducen║═Aeromonas hydrophilaį┌╚▒觌l╝■Ž┬─▄ē“└¹ė├Fe(ó¾)ū„×ķļŖūė╩▄¾w(Bond et al., 2003; Pham et al., 2003))Ż¼ätFe(ó¾)─▄ē“┤·╠µč§ū„×ķļŖūė╩▄¾wĮė╩▄ļŖūė.┼c┤╦═¼ĢrŻ¼ęčėąčąŠ┐░l¼FģÆ解hŠ│Ž┬NO-3║═NO-2Ą─╔·╬’▀ĆįŁ░ķļSų°Fe(ó“)Ą─č§╗»Ż¼╝┤NO-3-ę└┘ćą═Fe(ó“)č§╗»(Ratering et al.Ż¼ 2002).ę“┤╦Ż¼╗Ņąį╬█─ÓĶF▀ĆįŁŚl╝■Ž┬Ą─├ōĄ¬įŁę“┐╔─▄╩ŪŠC╔Ž╦∙╩÷ČÓĘN╔·╬’▀ĆįŁÅ═║Žū„ė├Ą─ĮY╣¹.
ĪĪĪĪ3.2.2 ┼ÓB▀^│╠ųąNO-2║═NO-3ØŌČ╚Ą─ūā╗»
ĪĪĪĪ×ķ▀Mę╗▓Į┐╝▓ņģÆ解hŠ│ųąĶF░▒č§╗»ū„ė├ī”¾wŽĄ├ōĄ¬─▄┴”žĢ½IĄ─┤¾ąĪŻ¼ęįč§╗»ĶFŲż×ķFe(ó¾)į┤Ż¼═©▀^īŹ“×Ė·█Ö┼ÓB▀^│╠ųąNO-2║═NO-3Ą─ūā╗»Ż¼▓óČ©┴┐Ęų╬÷┴╦NH+4č§╗»┴┐┼cFe(ó“)╔·│╔┴┐ų«ķgĄ─ĻPŽĄŻ¼ī”¾wŽĄīŹļHNH+4/Fe(ó“)─”Ā¢▒╚┼cĶF░▒č§╗»ū„ė├Ą─└ĒšōųĄ▀Mąą┴╦▒╚▌^.
ĪĪĪĪį┌│§╩╝¤oNO-2┤µį┌Ą─Ū░╠ߎ┬Ż¼ūĘ█ÖĶF▀ĆįŁ▀^│╠ųąNO-3║═NO-2ØŌČ╚Ą─ūā╗»Ż¼ĮY╣¹╚ńłD 4╦∙╩Š.┐╔ęŖŻ¼ļSų°┼ÓBĢrķgĄ─čėķLŻ¼ģÆ觌l╝■Ž┬¾wŽĄųą░l╔·«É╗»ĶF▀ĆįŁĄ─═¼Ģr░l╔·┴╦▌^║├Ą─├ōĄ¬ą¦╣¹Ż¼Ūę│÷¼F┴╦NO-2Ą─Č╠Ģ║Ęe└█.NO-2-NØŌČ╚ļS┼ÓBĢrķgĄ─čėķL│╩╔²Ė▀┌ģä▌Ż¼«ö└█Ęe┼ÓBų┴13 dŻ¼NO-2-NØŌČ╚ė╔│§╩╝ųĄ(╬┤Öz£y│÷)į÷╝ėų┴0.251 mg Īż L-1Ż¼▀_ĄĮĘÕųĄ;ŠS│ųų┴Ą┌15 dŻ¼NO-2-NØŌČ╚čĖ╦┘Ž┬ĮĄų┴ĘĆČ©;ų┴45 dŻ¼NO-2-NØŌČ╚│÷¼FĄ┌2éĆĘÕųĄ.Č°NO-3-NØŌČ╚╗∙▒Š│╩│ų└m╔Ž╔²Ą─┌ģä▌Ż¼▀@┼cWooshin Ą╚(2005)Ą─蹊┐ĮY╣¹ŽÓę╗ų┬.ė╔ė┌Ę┤款wŽĄ×ķģÆč§¾wŽĄŻ¼ę“┤╦Ż¼┐╔┼┼│²Ž§╗»ū„ė├«a╔·NO-2ĪóNO-3Ą─┐╔─▄Ż¼ė╔┤╦┐╔ęį═ŲöÓŻ¼│§╩╝ĮėĘN¾wŽĄ╬┤Öz£y│÷NO-2ĪóNO-3Ą─┤µį┌Ż¼Č°┼ÓB▀^│╠ųą░l╔·ā╔ĘN╗∙┘|ØŌČ╚Ą─Ęe└█¼FŽ¾Ż¼│õĘųšf├„┴╦«É╗»ĶF▀ĆįŁŚl╝■Ž┬─▄ē“░l╔·NH+4Ą─č§╗».

ĪĪĪĪłD 4 ╗Ņąį╬█─ÓĶF▀ĆįŁ▀^│╠ųą╗∙┘|ØŌČ╚ļS┼ÓBĢrķgĄ─ūā╗»
ĪĪĪĪ3.3 ÖCųŲ╠Įėæ 3.3.1 NH+4č§╗»┼cFe(ó“)«a╔·ūā╗»ĻPŽĄ
ĪĪĪĪĖ∙ō■ĶF░▒č§╗»Ę┤æ¬╩ĮŻ¼NH+4č§╗»┴┐┼cFe(ó“)«a╔·┴┐ų«ķgĄ─└Ēšō╗»īWėŗ┴┐▒╚×ķ1Ż║6Ż¼×ķ┐╝▓ņĶF▀ĆįŁ▀^│╠±Ņ║ŽNH+4č§╗»ū„ė├╦∙š╝Ą─▒╚└²┤¾ąĪŻ¼ī”┼ÓB▀^│╠ųąNH+4č§╗»┴┐┼cFe(ó“)tot«a╔·┴┐ų«ķgĘųäe░┤ŠĆąį║═āńųĖöĄĘĮ│╠▀Mąą┴╦╗žÜwĘų╬÷Ż¼ĮY╣¹ęŖłD 5.┐╔ęŖŻ¼▓╗═¼┼ÓBĢrķgā╚NH+4č§╗»┴┐┼cFe(ó“)tot«a╔·┴┐Ė³Ę¹║ŽāńųĖöĄĻPŽĄŻ¼R2×ķ0.9521.┴Ē═ŌŻ¼Å─łDųą▀Ć┐╔ęį┐┤│÷Ż¼īŹ“×£yĄ├Ą─NH+4/Fe(ó“)tot─”Ā¢▒╚┼c└ĒšōųĄ(0.1667)ŽÓ▒╚ę¬┤¾Ą─ČÓŻ¼╝┤ĶF▀ĆįŁ▀^│╠ųą▀ĆįŁ«a╔·ę╗Č©┴┐Fe(ó“)Ą─═¼Ģr╦∙č§╗»Ą─NH+4ę¬▒╚└ĒšōųĄĖ▀Ż¼▀@šf├„¾wŽĄųąNH+4Ą─č§╗»▓╗āH╩Ūė╔ĶF░▒č§╗»ū„ė├ī¦ų┬Ż¼Č°Ūę┤µį┌Ųõ╦¹Ą─Ę┤æ¬▀^│╠.ė╔ė┌«É╗»ĶF▀ĆįŁ±Ņ║ŽNH+4č§╗»Ą─═¼ĢrĢ■«a╔·NO-2Ż¼«a╔·Ą─NO-2▀Mę╗▓Į┐╔┼cNH+4░l╔·ANAMMOX¼FŽ¾Ż¼Ž¹║─ę╗▓┐ĘųNH+4-N.ė╔┤╦┐╔ęį═Ų£yŻ¼įō¾wŽĄ┐╔─▄Ģ■░l╔·ANAMMOX¼FŽ¾.

ĪĪĪĪłD 5 NH+4č§╗»┴┐┼cFe(ó“)tot«a╔·┴┐ų«ķgūā╗»ĻPŽĄ
ĪĪĪĪ3.3.2 Å─¤ß┴”īWĮŪČ╚Ęų╬÷
ĪĪĪĪĘ┤æ¬Ą─╝¬▓╝╦╣ūįė╔─▄╩Ū┼ąöÓĖ„ŅÉč§╗»▀ĆįŁĘ┤æ¬─▄ʱūį░l▀MąąĄ─ę└ō■Ż¼▒Ē 2Įo│÷┴╦«É╗»ĶF▀ĆįŁ¾wŽĄųą┐╔─▄░l╔·Ą─č§╗»▀ĆįŁĘ┤æ¬╩Įś╦£╩╝¬▓╝╦╣ūįė╔─▄.ė╔┤╦┐╔ęį┼ąöÓĖ„Ę┤æ¬į┌įō¾wŽĄųąŠ∙ėą┐╔─▄░l╔·.
ĪĪĪĪ▒Ē2 ┐╔─▄░l╔·Ą─č§╗»▀ĆįŁĘ┤æ¬╩Įś╦£╩╝¬▓╝╦╣ūįė╔─▄ūā╗»
ĪĪĪĪ3.3.3 ╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁŚl╝■Ž┬Ą─C-Fe-N±Ņ║Žū„ė├ÖCųŲ
ĪĪĪĪĮY║Ž╔Ž╩÷ĻPė┌¾wŽĄųąFe(ó“)ĪóNH+4-N╝░TN ØŌČ╚Ą─ūā╗»╝░Ęų╬÷Ż¼ī”╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁ¾wŽĄC-Fe-N±Ņ║Žū„ė├ÖCųŲū„╚ńŽ┬═Ų£yŻ¼ĮY╣¹ęŖłD 6.

ĪĪĪĪłD 6 ģÆ解hŠ│Ž┬╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁŚl╝■Ž┬Ą─C-Fe-NĮ╗╗źū„ė├ÖCųŲ╩ŠęŌłD
ĪĪĪĪĖ∙ō■╔Ž╩÷Ą─├ōĄ¬ą¦╣¹╝░įŁę“Ęų╬÷Ż¼╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁŚl╝■Ž┬Ą─├ōĄ¬¾wŽĄųą┐╔─▄┤µį┌ęįŽ┬4éĆĘ┤æ¬▀^│╠.ó┘ĶF░▒č§╗»ū„ė├(▀^│╠I)Ż║įńį┌1997─ĻŻ¼LutherĄ╚(1997)į┌Ė╗Õi║ŻĄū│┴Ęe╬’ųą░l¼FŻ¼«öĄõą═Ą─Ž§╗»/Ę┤Ž§╗»═ŠÅĮČ╠┬ĘĢrŻ¼NH3║═ėąÖCĄ¬Ęųäeį┌║├č§Īó╚▒觌l╝■Ž┬į┌MnO2▀ĆįŁĄ─═¼Ģrč§╗»NO-3×ķN2;ClementĄ╚(2005)į┌Ė╗ĶF║ė░Č│┴Ęe╬’ųą│§┤╬ūC├„┴╦Fe(ó¾)ū„×ķļŖūė╩▄¾w═¼Ģrč§╗»NH+4×ķNO-2Ą─▀^│╠×ķ«a╔·─▄┴┐Ą─╔·╬’▀^│╠;ų«║¾ę▓│÷¼F┴╦į┌žił÷ÅU╦«(Wooshin et al., 2005)ĪóرĄž═┴╚└(Junu et al., 2009; Wendy et al., 2012)Ą╚┤µį┌ĶF▀ĆįŁŚl╝■Ž┬Ą─ģÆč§░▒č§╗»▀^│╠ĘĮ├µĄ─ł¾Ą└.ĮY║ŽłD 4Ż¼ģÆ觌l╝■Ž┬¤oNO-2ĪóNO-3┤µį┌Ą─Ū░╠ߎ┬Ż¼NO-2Ą─Č╠Ģ║Ęe└█▓╗┐╔─▄╩Ūė╔Ž§╗»Š·ū„ė├ī¦ų┬.╚╗Č°«öĘ┤Ž§╗»ū„ė├═Żų╣į┌NO-2╦«ŲĮŻ¼Ģ■ėąNO-2Ęe└█¼FŽ¾░l╔·Ż¼Ą½¤oĘ©«a╔·NO-3(Hulth et al., 1999).ę“┤╦┐╔ęįšf├„Ż¼«É╗»ĶF▀ĆįŁŚl╝■Ž┬─▄ē“░l╔·NH+4Ą─č§╗».ó┌ģÆč§░▒č§╗»ū„ė├(▀^│╠II)Ż║ģÆ觌l╝■Ž┬«É╗»Fe(ó¾)▀ĆįŁ▀^│╠ųą░l╔·NO-2║═NO-3Ą─Ęe└█¼FŽ¾Ż¼═¼Ģr░ķļSų°┴╝║├Ą─├ōĄ¬ą¦╣¹.╝┘įO¾wŽĄųąĄ─├ōĄ¬ą¦╣¹āHė╔ĶF░▒č§╗»ū„ė├ī¦ų┬Ż¼ät«É╗»ĶF▀ĆįŁ▀^│╠ųąĢ■░l╔·NH+4-NĄ─╚ź│²Ż¼Ą½ī”TN¤o├„’@Ą─╚ź│²ą¦╣¹.┤╦═ŌŻ¼ė╔łD 5┐╔ų¬Ż¼NH+4/Fe(ó“)─”Ā¢▒╚īŹ“×ųĄ▌^└ĒšōųĄę¬┤¾Ż¼šf├„«a╔·Ą─NO-2▀Mę╗▓Į┼cNH+4░l╔·ANAMMOXū„ė├Ż¼Ė∙ō■TrimmerĄ╚(2003)ł¾Ą└Ż¼░³║¼╝Ü░¹║Ž│╔į┌ā╚Ą─ANAMMOX▀^│╠į┌╔·│╔N2Ą─═¼Ģrę▓«a╔·ę╗Č©┴┐Ą─NO-3.ó█NO-3-ę└┘ćą═Fe(ó“)č§╗»(▀^│╠ó¾)Ż║įō▀^│╠╩Ūį┌ģÆ觌l╝■Ž┬ęįFe(ó“)×ķ╬©ę╗ļŖūė╣®¾wŻ¼«É╗»▀ĆįŁŽ§╦ß¹}Ą─╔·╬’▀^│╠.StraubĄ╚(1996)ł¾Ą└┴╦ųą£žŠ·Ą─Ž§╦ß¹}ę└┘ćąįFe(ó“)č§╗»Ż¼▀@ą®Ę┤Ž§╗»Š·└¹ė├Fe(ó“)ū„×ķļŖūė╣®¾w▀ĆįŁŽ§╦ß¹}.NielsenĄ╚(1998)į┌╗Ņąį╬█─Óųą░l¼Fįō¼FŽ¾Ą─░l╔·Ż¼ī”├ōĄ¬│²┴ūŠ▀ėą║▄║├Ą─╚ź│²─▄┴”Ż¼═¼ĢrĄ├│÷ūŅ┤¾Fe(ó“)ę└┘ćą═Ž§╦ß¹}▀ĆįŁ┬╩×ķ0.31 mmol Īż g-1 Īż h-1.Į³─ĻüĒŻ¼Ųõū„ė├ÖC└Ēę²Ų┴╦╚╦éāĄ─ĻPūóŻ¼CarlsonĄ╚(2012)Å─ŲĮ║ŌļŖūėöz╚Ī║═├ōČŠĘĮ├µĻU├„┴╦ģÆč§NO-3-ę└┘ćą═Fe(ó“)č§╗»Ą─ū„ė├ÖCųŲ.ģÆ解hŠ│Ž┬Ą─╗Ņąį╬█─Ó«É╗»ĶF▀ĆįŁ¾wŽĄŠ▀éõ┴╦NO-3-ę└┘ćą═Fe(ó“)č§╗»ū„ė├░l╔·Ą─╦∙ėąŚl╝■Ż¼ė╔┤╦┐╔ęį═ŲöÓįōĘ┤æ¬░l╔·Ą─┐╔─▄ąįŻ¼╚╗Č°ī”▀@ę╗▀^│╠Ą─░l╔·▀Ćėą┤²į┌Į±║¾ū÷Ė³╔Ņę╗īėĄ─蹊┐.ó▄Fe(ó¾)Ą─╦«ĮŌū„ė├Ż║Fe(ó¾)Ž╚╚▄ĮŌ║═╬³╦«Ż¼╔·│╔╚²ār╦«║ŽļxūėFe(H2O)63+Ż¼═¼ĢrŻ¼Fe(H2O)63+ Ą─╦«ĮŌĘ┤æ¬ę²░lę╗ŽĄ┴ą▓╗═¼ą╬æBå╬║╦Įj║Ž╬’Ą─ą╬│╔Ż¼▀Mę╗▓Į┐s║Žą╬│╔ČÓ║╦Įj║Ž╬’Fen(OH)m(3n-m)+(n>1Ż¼m=3n)(╚ŅÅ═▓²Ą╚Ż¼1998).
ĪĪĪĪ│Ū╩ą╬█╦«ÅSĄ─╗Ņąį╬█─Ó¾wŽĄ╩Ūę╗éĆ²ŗ┤¾Ą─ČÓĘN╬ó╔·╬’║═ÅU╦«ųąĀIB╬’┘|śŗ│╔Ą─Å═ļs╩│╬’µ£Ż¼ę“┤╦Ż¼ģÆ解hŠ│Ž┬Ą─«É╗»ĶF▀ĆįŁ¾wŽĄ▓╗āH×ķĶF▀ĆįŁŠ·ĪóģÆč§░▒č§╗»Š·╠ß╣®┴╦┴╝║├Ą─╔·ķLŁhŠ│Ż¼═¼Ģrė╔ė┌╗∙┘|ųą║¼ėąūŃē“Ą─Fe(ó“)║═NO-3Ż¼▀@┐╔─▄ę▓×ķNO-3-ę└┘ćą═Fe(ó“)č§╗»╠ß╣®┴╦Ę┤æ¬░l╔·Ą─┐╔─▄.ĻPė┌«É╗»Fe(ó¾)▀ĆįŁ▀^│╠ųą░l╔·├ōĄ¬ą¦╣¹Ą─ū„ė├ÖCųŲĄ╚ĘĮ├µĄ─£╩┤_ĮŌßīŻ¼īóĢ■╗∙ė┌▓╗═¼Š·ī┘Ą─Ė╗╝»┼ÓBĪóĖ·█Ö╠žš„ųĖś╦Ą─ØŌČ╚ūā╗»Ż¼╔§ų┴═¼╬╗╦ž╩Š█ÖĄ╚ĘĮ├µķ_š╣Ė³╔Ņę╗īėĄ─蹊┐.Š▀¾wģóęŖ╬█╦«īÜ╔╠│Ū┘Y┴Ž╗“http://www.jianfeilema.cnĖ³ČÓŽÓĻP╝╝ąg╬─ÖnĪŻ
ĪĪĪĪ4 ĮYšō
ĪĪĪĪ1)IRBī”▓╗═¼ą╬╩ĮFe(ó¾)Ą─└¹ė├Ūķør▓╗═¼Ż¼Ė³╚▌ęū└¹ė├▒╚▒Ē├µĘe┤¾Ą─ĘŪŠ¦¾w╝░╚▄ĮŌæBĶF(╚ńFe(OH)3)Ż¼čąŠ┐▒Ē├„Ż¼č§╗»ĶFŲż╩Ūę╗ĘN▌^ęū▒╗╬ó╔·╬’▀ĆįŁĄ─┴«ārĄ─Fe(ó¾)į┤Ż¼┐╔ęį╠µ┤·│Żė├Ą─Fe(OH)3Ż¼▓ó─▄▀_ĄĮęįÅUų╬ÅUĄ──┐Ą─.
ĪĪĪĪ2)«É╗»ĶF▀ĆįŁ▀^│╠ųą├ōĄ¬ą¦╣¹┼c«a╔·Ą─Fe(ó“)╝░Fe(ó¾)ØŌČ╚Š▀ėą▌^║├Ą─ĻP┬ōąįŻ¼ŲõųąŻ¼č§╗»ĶFŲż¾wŽĄ├ōĄ¬ąį─▄’@ų°Ż¼ūŅĮKNH+4-N╝░TNĄ─╚ź│²┬╩Ęųäe▀_ĄĮ73.65%Īó74.76%.NH+4-NĪóTN└█ėŗ╚ź│²┴┐Ęųäe×ķ75.04║═80.99 mg Īż L-1Ż¼╚▌ĘeTN╚ź│²┬╩×ķ3.88 mg Īż L-1 Īż d-1.
ĪĪĪĪ3)Å─Ė„Ę┤æ¬Ą─ś╦£╩╝¬▓╝╦╣ūįė╔─▄ūā╗»ĮŪČ╚üĒ┐┤Ż¼ģÆ解hŠ│Ž┬«É╗»ĶF▀ĆįŁŚl╝■Ž┬┐╔─▄┼╝┬ō░l╔·ĶF░▒č§╗»ū„ė├ĪóģÆč§░▒č§╗»ū„ė├╝░NO-3-ę└┘ćą═Fe(ó“)č§╗»Ę┤æ¬Ż¼╣▓═¼ū„ė├ī¦ų┬¾wŽĄŠ▀ėą▌^║├Ą─├ōĄ¬ąį─▄.ŲõųąŻ¼ęįIRB×ķų„Ą─ĶF░▒č§╗»ū„ė├š╝ų„ꬥž╬╗.